Clear Sky Science · sv
En praktisk guide till riktade enkelcells-RNA-sekvenseringstekniker
Varför det spelar roll att se enskilda celler
Varje cell i din kropp bär samma DNA, men olika celler beter sig mycket olika. De gör det genom att slå på eller av specifika gener och genom att redigera RNA-molekyler på subtila sätt. Modern enkelcells-RNA-sekvensering kan läsa vilka RNA som finns i tusentals celler samtidigt, men den missar i dagsläget större delen av budskapet. Denna översikt förklarar var dagens tekniker förlorar information och hur nya ”riktade” metoder utvecklas för att zooma in på de viktigaste delarna av RNA-molekyler för forskning, diagnostik och behandlingsdesign.
Var dagens metoder brister
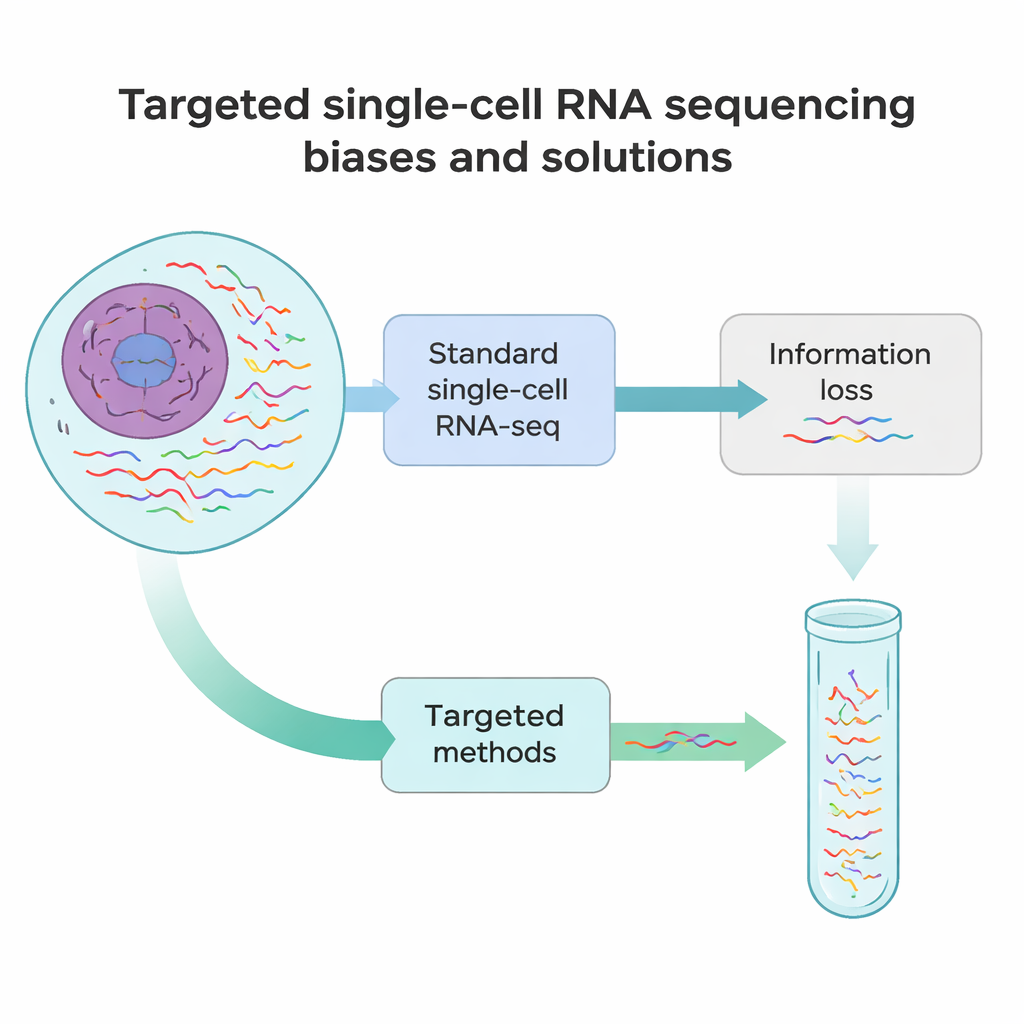
Standardmetoder för enkelcells-RNA-sekvensering liknar lite att ta en snabb ögonblicksbild av varje budskap i en cell snarare än en fullängdsfilm. I de flesta experiment upptäcks bara omkring 10–40 % av alla RNA i en cell, och bara deras början eller slut läses. Det innebär att många sällsynta men viktiga RNA — såsom markörer som definierar en cells identitet, eller genvarianter som bär sjukdomsframkallande mutationer — lätt missas. Utöver det inför flera tekniska steg, från att dela upp vävnader i enskilda celler till att kopiera RNA till DNA och förstärka det, systematiska snedvridningar. Vissa RNA kapas tidigt, vissa överrepresenteras och andra försvinner helt från datan.
Varför interna RNA-detaljer är viktiga
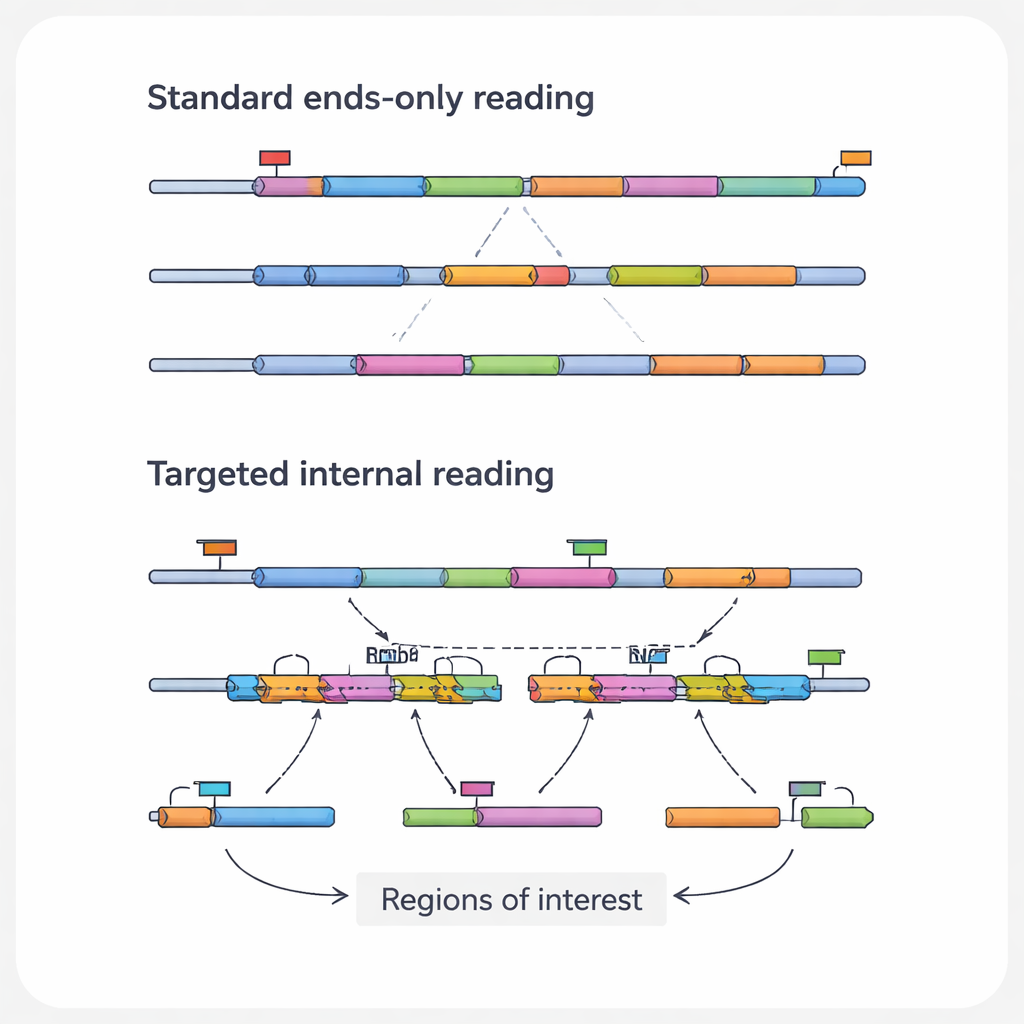
Den mest medicinskt relevanta informationen i en RNA-molekyl ligger ofta i dess interna regioner, inte i ändarna som standardmetoder ser. Dessa inre sektioner kan innehålla punktmutationer som driver cancer, fusionspunkter där två gener onormalt har förenats, eller splitsningsjunctioner som skapar olika proteinalternativ från samma gen. De kan också bära spår av genredigeringsverktyg som CRISPR. Författarna kallar dessa specifika funktioner för ”intresseområden” och de RNA som bär dem för ”transkript av intresse”. Eftersom vanliga höggenomströmningplattformar främst läser RNA:ns ändar förbiser de rutinmässigt dessa avgörande detaljer, särskilt i långa eller låg-abundans-transkript.
Nya sätt att rikta strålkastaren
För att övervinna dessa blinda fläckar har forskare utvecklat en familj av riktade enkelcells-RNA-sekvenseringsmetoder. Istället för att försöka läsa alla RNA lika, berikar dessa metoder medvetet utvalda transkript eller regioner. Vissa strategier bygger om fångstkulorna så att de hakar i interna RNA-sekvenser snarare än bara svansen, och drar ut valda budskap till biblioteket redan i första steget. Andra tillsätter skräddarsydda primrar som börjar kopiera vid en intern punkt, eller extra PCR-steg som specifikt amplifierar en kort lista gener från ett befintligt bibliotek. Ytterligare en grupp använder DNA-prober som hybridiserar till målen eller deras kopior och sedan fiskar ut dem, ofta med enkla kemiska taggar. Varje kategori väger av känslighet, antal celler, antal mål och kostnad, men alla har samma mål: att återvinna mer meningsfull detalj från samma eller färre sekvenseringsläsningar.
Användningsområden från virus till tumörer
Dessa riktade metoder omformar redan flera områden inom biologi och medicin. Vid infektioner kan de äntligen fånga virala eller bakteriella RNA som saknar de poly(A)-svansar som standardprotokoll förväntar sig, och avslöja vilka värdceller de finns i och hur de förändrar värdgeners aktivitet. Inom cancer kan riktad enkelcells-sekvensering lokalisera vilka celltyper som bär specifika mutationer eller fusionsgener och koppla dessa till förändrade genprogram, vilket hjälper till att förklara varför vissa celler blir resistenta mot behandling. Andra metoder fokuserar på alternativ splitsning och kartlägger vilka celltyper som använder vilka isoformer, eller på sällsynta cellpopulationer och subtila markörer som annars skulle ligga under detektionsgränsen. I poolade CRISPR-skärmar ger förbättrad fångst av guidande RNA forskare möjlighet att koppla varje genetisk störning till dess exakta cellulära svar.
Välja rätt verktyg och vad som väntar framöver
Eftersom det nu finns ett stort verktygslåda av riktade tillvägagångssätt föreslår författarna ett beslutsdiagram för att hjälpa forskare välja metod. Nyckelfrågor inkluderar om full transkriptomprofilering behövs, hur många gener eller regioner som måste riktas, hur långt dessa regioner ligger från RNA-ändarna och hur många celler som kan bearbetas. Framöver menar de att de största vinsterna kommer från att förbättra de allra första fångststegen, att utvidga smarta probe-baserade strategier och att kombinera riktning med framväxande långläsnings- och direkt-RNA-sekvenseringsplattformar. Tills det blir praktiskt att läsa varje RNA i varje cell från ände till ände kommer riktad enkelcells-RNA-sekvensering att förbli oumbärlig för att se de delar av det cellulära budskapet som betyder mest för biologi och sjukdom.
Citering: Moro, G., Brunner, E. & Basler, K. A practical guide to targeted single-cell RNA sequencing technologies. Commun Biol 9, 250 (2026). https://doi.org/10.1038/s42003-026-09675-y
Nyckelord: enkelcells-RNA-sekvensering, riktad sekvensering, transkriptomik, cancermutationer, rumslig transkriptomik