Clear Sky Science · sv
Aktivering av cytomegaloviruskodade G-proteinkopplade receptorn UL33 av en inre N-terminal peptid
Hur ett vanligt virus omprogrammerar våra celler
Humant cytomegalovirus (HCMV) infekterar tyst de flesta människor på jorden och förblir vanligen outtalat. Ändå kan det hos nyfödda, transplantationspatienter och andra med försvagat immunsystem ge allvarlig sjukdom. Denna studie visar på molekylär nivå hur ett viralt protein kallat UL33 fungerar som en inbyggd brytare som ständigt driver infekterade celler att gynna viruset. Att förstå denna dolda brytare hjälper till att förklara hur HCMV kvarstår livet ut och pekar på nya sätt att oskadliggöra det utan att skada normal cellsignalering.
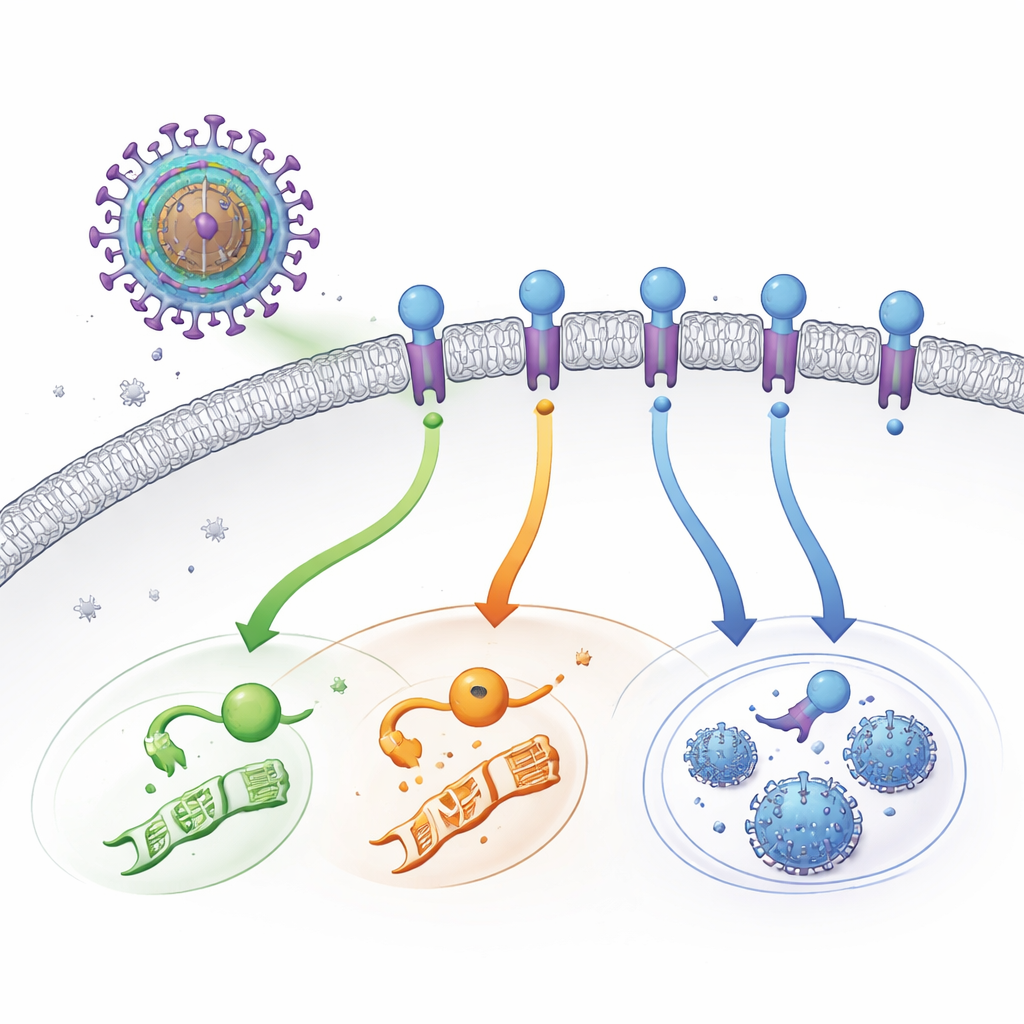
En förklädd viral brytare på cellytan
HCMV bär sina egna varianter av cellytans receptorer—proteiner som normalt känner av hormoner eller immunsignaler. UL33 är en av dessa virala receptorer. Till skillnad från typiska receptorer, som väntar på en extern signal, är UL33 ”alltid på”. När den väl har placerats i det infekterade cellens yttre membran kan den koppla in sig i flera av cellens huvudkommunikationsvägar samtidigt. Dessa vägar styr processer som genaktivitet, ämnesomsättning och beslutet att gå i vila eller producera mer virus. Under lång tid visste forskare att UL33 var aktiv men inte vad som satte på den, särskilt eftersom ingen extern aktiverande molekyl (ligand) någonsin hade hittats.
En självgående startmotor: receptorn som bär sin egen nyckel
Med avancerad kryo-elektronmikroskopi fångade författarna tredimensionella ögonblicksbilder av UL33 bunden till en av cellens signalpartners, ett G-protein kallat Gs. Bilderna visar att själva början av UL33-proteinet—dess korta N-terminala svans—viker tillbaka in i en ficka på receptorn själv, ungefär som en nyckel som lämnas kvar i ett lås. Denna ”fästa” svans ligger i en liten sidoficka som i besläktade mänskliga receptorer normalt skulle ta emot en del av ett immunsignalprotein kallat en kemokin. Genom att ockupera denna ficka från början blockerar UL33 externa kemokiner från att binda alls, vilket förklarar varför den beter sig som en ”föräldralös” receptor som inte svarar på normala värdbudbärare.
Avgörande atomer i den virala på-bryttaren
För att bekräfta att denna inbyggda svans verkligen är utlösaren ändrade teamet systematiskt individuella byggstenar i UL33 i humana celler. De fokuserade på de första aminosyrorna i svansen och matchande punkter inne i fickan som greppar den. När de bytte ut dessa nyckelrester mot mer neutrala sådana eller tog bort en av dem helt, sjönk UL33:s förmåga att signalera till nära noll—även om de förändrade receptorerna fortfarande nådde cellytan i normala mängder. Med andra ord var proteinet närvarande men tyst. Detta visar att svansen inte bara är strukturell dekoration; den är den avgörande självaktiverande delen som håller UL33 påslagen.
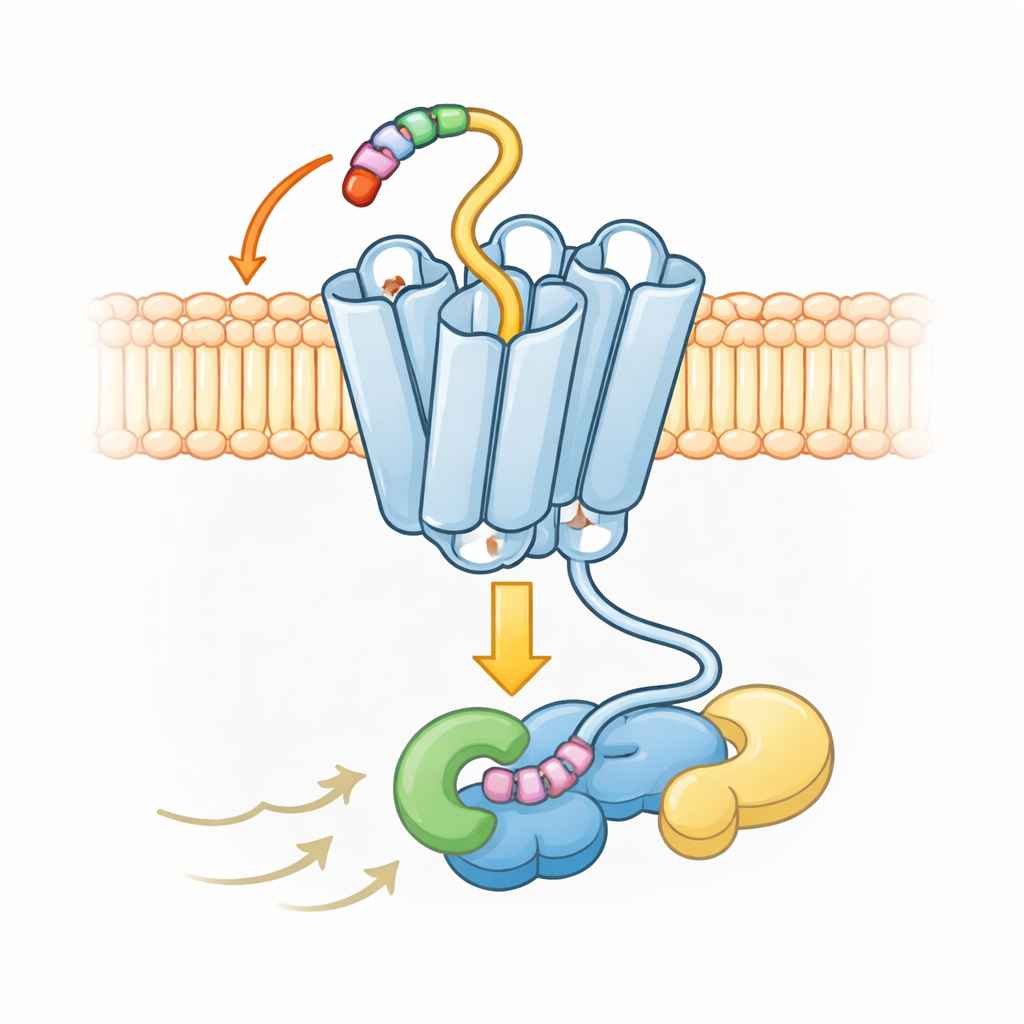
En ovanlig form för bred men kontrollerad signalering
Strukturkartorna visar också att UL33 antar en något annorlunda aktiv form jämfört med typiska humana receptorer. I de flesta receptorer i denna familj svänger en av de sju helixarna nära insidan av cellen dramatiskt utåt när receptorn aktiveras, vilket öppnar en stor kavitet för G-proteiner att docka i. I UL33 håller sig den helixen mycket närmare centrum och skapar en tajtare passform. Trots det kan UL33 fortfarande engagera flera typer av G-proteiner—Gs, Gq och Gi—genom att göra precisa kontakter med spetsen av G-proteinet som fäster i receptorn. Dessa kontakter gynnar vissa G-proteiner och utesluter andra, såsom G12/13-gruppen, vilket tillåter viruset att snedvrida cellens svar utan att släppa lös okontrollerad signalering.
Nya sårbarheter för ett gammalt virus
Genom att kombinera strukturbilder med funktionella tester målar studien upp en tydlig bild: UL33 är en självstartande viral receptor vars egen svans fungerar som en permanent fäst aktivator. Denna konstruktion låter HCMV varsamt men beständigt finjustera värdcellens signalering för att stödja viral replikation och reaktivering, särskilt genom att förstärka vägar som slår på virala gener. Samtidigt blottlägger arbetet svaga punkter som läkemedel skulle kunna utnyttja, såsom en smal tunnel som leder in till fickan där svansen binder. Molekyler utformade för att kilas in i detta område eller lossa svansen kan tysta UL33:s aktivitet och minska viral skada, samtidigt som kroppens normala receptorer lämnas i fred. För patienter i riskzonen från HCMV kan riktning mot denna virala ”mästarebrytare” en dag erbjuda ett mer precist sätt att hålla viruset i schack.
Citering: Drzazga, A.K., Suzuki, S., Wouters, C. et al. Activation of cytomegalovirus-encoded G protein-coupled receptor UL33 by an innate N-terminal peptide. Commun Biol 9, 415 (2026). https://doi.org/10.1038/s42003-026-09660-5
Nyckelord: cytomegalovirus, viralt GPCR, cellsignalering, cryo-EM-struktur, läkemedelsmål