Clear Sky Science · sv
Undersökning av Salmonella-biofilms svar på antibiotikabehandling med optisk fototermisk infraröd spektroskopi
Varför klibbiga bakteriestäder spelar roll
Många sjukdomsalstrande bakterier föredrar att leva i tätt packade samhällen kallade biofilmer, där cellerna fäster vid varandra och vid ytor i kroppen eller på medicintekniska material. Inom dessa slemmiga ”städer” kan mikrober undkomma antibiotika som normalt skulle döda dem. Denna studie presenterar ett nytt sätt att titta in i biofilmer på detaljnivå, och visar vilka celler som aktivt växer och hur de reagerar när kraftfulla läkemedel tillsätts. Att förstå dessa osynliga aktivitetsmönster kan hjälpa läkare att utforma behandlingar som slutligen bryter biofilmens seglivade försvar.
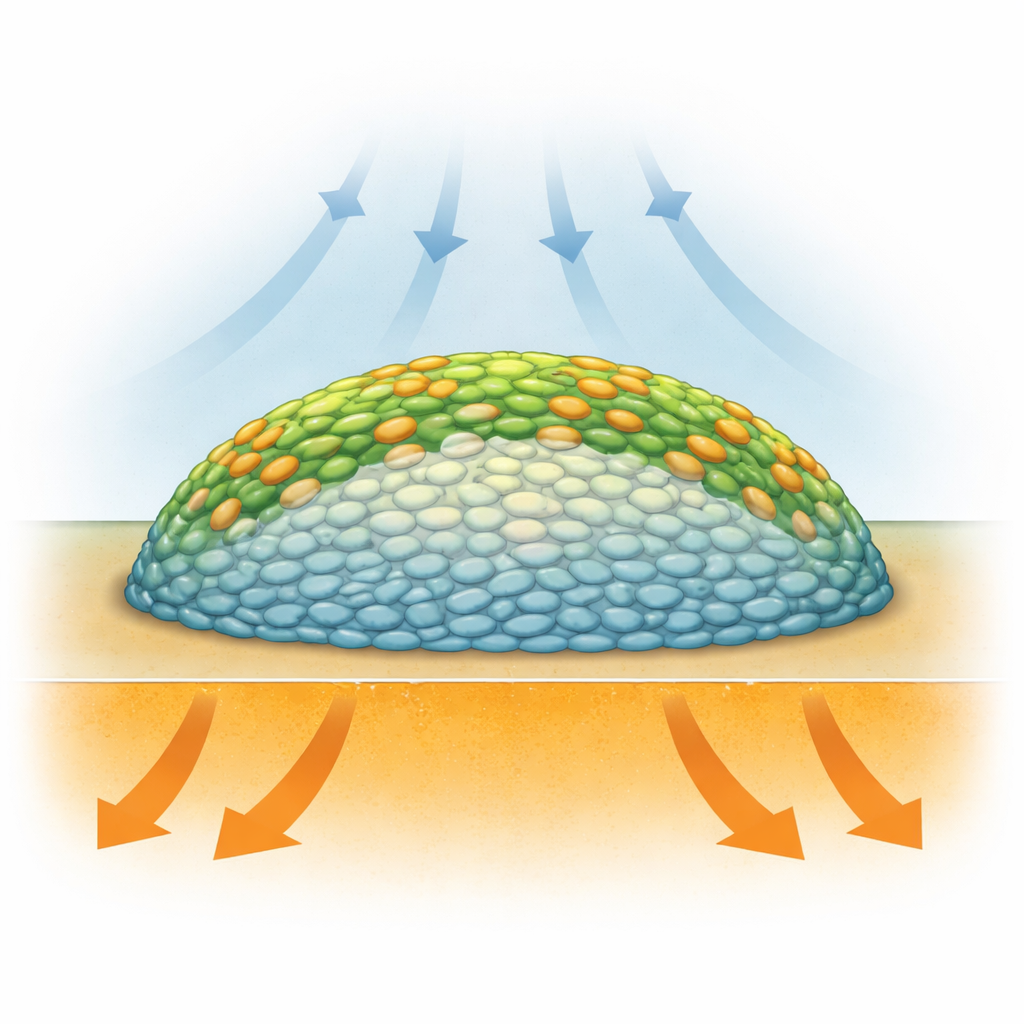
Det dolda livet i bakteriestäder
Biofilmer är inte bara slumpmässiga klumpar av bakterier: de är flerskiktade strukturer där bakterier lever i mycket olika förhållanden beroende på var de sitter. Celler i yttre lager har bättre tillgång till syre från luften, medan de som är begravda i centrum får syrebrist och kan sakta ner eller gå in i viloläge. Tidigare metoder som fluorescensmikroskopi kunde visa struktur, men krävde ofta tillsatta färgämnen eller genetiska markörer som kunde störa biologin, och de mätte inte direkt vad cellerna gjorde kemiskt. Forskare behövde ett sätt att ”se” kemin i levande biofilmer, skikt för skikt, utan att riva sönder dem eller kraftigt förändra dem.
Se kemin med osynligt ljus
Gruppen använde en teknik kallad optisk fototermisk infraröd (O-PTIR) spektroskopi, som använder pulser av osynligt infrarött ljus och en synlig laser för att detektera mycket små vibrationer i molekyler. Dessa vibrationer fungerar som fingeravtryck för viktiga cellulära komponenter, såsom proteiner, fetter och DNA. För att följa metabolismen—cellernas aktiva användning av näringsämnen—matade de Salmonella Typhimurium-biofilmer med en särskild form av socker där kolatomerna var något tyngre än vanligt (en stabil isotop känd som kol-13). När celler är aktiva och gör nya proteiner bygger de in dessa tyngre atomer i sina strukturer, vilket orsakar subtila men detekterbara förskjutningar i det infraröda signalen. Genom att kryossnittsa biofilmen och skanna tunna tvärsnitt skapade forskarna kemiska kartor som visade var i biofilmen detta tunga kol hade inkorporerats.
Aktivitetsringar och tysta kärnor
Infraröd avbildning av obehandlade Salmonella-biofilmer visade ett slående mönster: de yttre regionerna och ytskikten visade stark inkorporering av det tunga kolet, medan en stor central kärna visade mycket lite. Med andra ord betedde sig biofilmen som en ring av aktiva celler som omger ett tyst inre. Statistisk analys av de infraröda spektren bekräftade att signaler från proteinrelaterade vibrationer försköts mer i de yttre lagren än i centrum, vilket indikerar högre proteintillverkning i kanterna. Dessa resultat stöder idén att syretillgång, som är störst nära ytan, är den främsta drivande faktorn för metaboliska ”varmzoner” i denna kolonimodell, även om näringsämnen flödar inifrån underifrån. Studien gav en av de klaraste, högupplösta bilderna hittills av hur metabolismen är uppdelad inuti en biofilm.
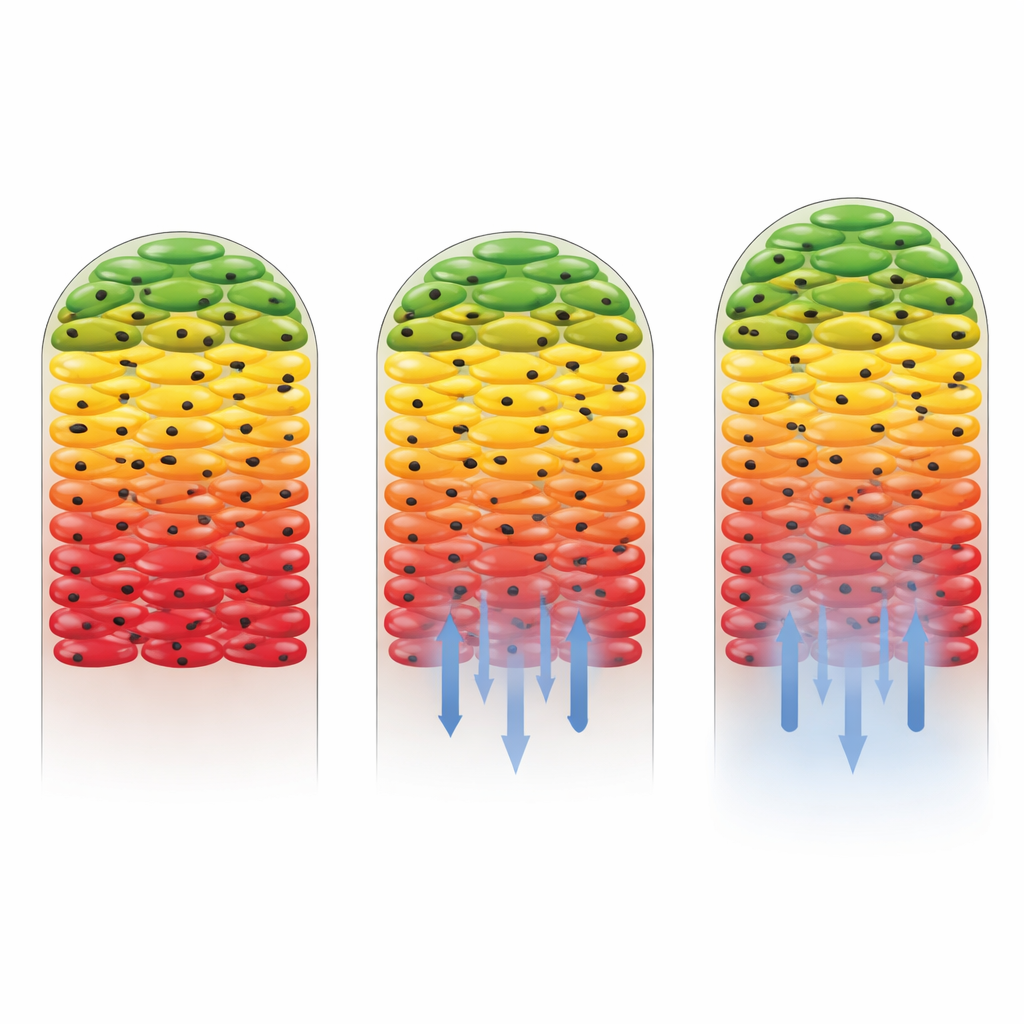
Hur olika antibiotika omformar biofilmaktiviteten
Forskarnas nästa fråga var vad som händer när antibiotika tillsätts. De använde två läkemedel: kanamycin, som Salmonella-stammen är känslig för, och gentamicin, mot vilket stammen hade konstruerats för att vara i stort sett icke-känslig. När gentamicin var närvarande ändrades det övergripande mönstret av aktiva yttre lager och en tyst kärna knappt alls, vilket visar att resistenta celler fortsatte växa och inkorporera tungt kol i stora delar av biofilmen. Däremot minskade kanamycin dramatiskt den metaboliska aktiviteten, särskilt nära botten av biofilmen där läkemedelskoncentrationen var högst. Endast ett tunt band av celler längst bort från antibiotikakällan visade fortfarande tecken på kolupptag. Detta visade inte bara att läkemedlet var effektivt, utan också att biofilmstrukturen i sig hjälpte till att skydda vissa celler genom att försvaga läkemedlet när det diffunderade inåt.
Nya fönster för behandling av svåra infektioner
Ur ett icke-specialistiskt perspektiv är huvudbudskapet att detta arbete erbjuder ett kraftfullt ”kemiskt mikroskop” för att iaktta hur bakteriesamhällen lever och överlever behandling i tre dimensioner. Genom att kombinera en icke-destruktiv infraröd avbildningsmetod med en säker tung form av kol kunde forskarna lokalisera var bakterier aktivt växte och hur den aktiviteten skiftade under olika antibiotika. Deras resultat bekräftar att biofilmer rymmer en blandning av upptagna och nästan vilande celler, och att effektiva läkemedel ändå kan dämpas av biofilmens fysiska barriär. I framtiden skulle detta angreppssätt kunna användas för att testa nya terapier, utforska hur olika arter samarbetar eller delar resistens i blandade biofilmer, och i slutändan hjälpa till att utforma smartare strategier för att rensa envisa infektioner.
Citering: Smaje, D., Zhu, X., Hinton, J.C.D. et al. Investigating Salmonella biofilm responses to antibiotic treatment using optical photothermal infrared spectroscopy. Commun Biol 9, 405 (2026). https://doi.org/10.1038/s42003-026-09655-2
Nyckelord: biofilmer, Salmonella, antibiotikaresistens, infraröd avbildning, stabil isotopspårning