Clear Sky Science · sv
Agentbaserad modellering av cellära dynamiker i adoptiv cellterapi
Varför datorframställda celler spelar roll för cancerbehandling
Cancerterapier som använder levande immunceller förändrar medicinen, men att pröva varje ny idé i djur och människor är långsamt, kostsamt och ibland riskfyllt. Denna studie presenterar ABMACT, ett virtuellt laboratorium som bygger "digitala" cancer‑ och immunceller och låter dem interagera på en datorskärm. Genom att spela upp och utvidga verkliga experiment hjälper ABMACT forskare att se vilka egenskaper hos NK‑cellsterapier som betyder mest, och hur behandlingsscheman kan finjusteras långt innan kliniska försök.
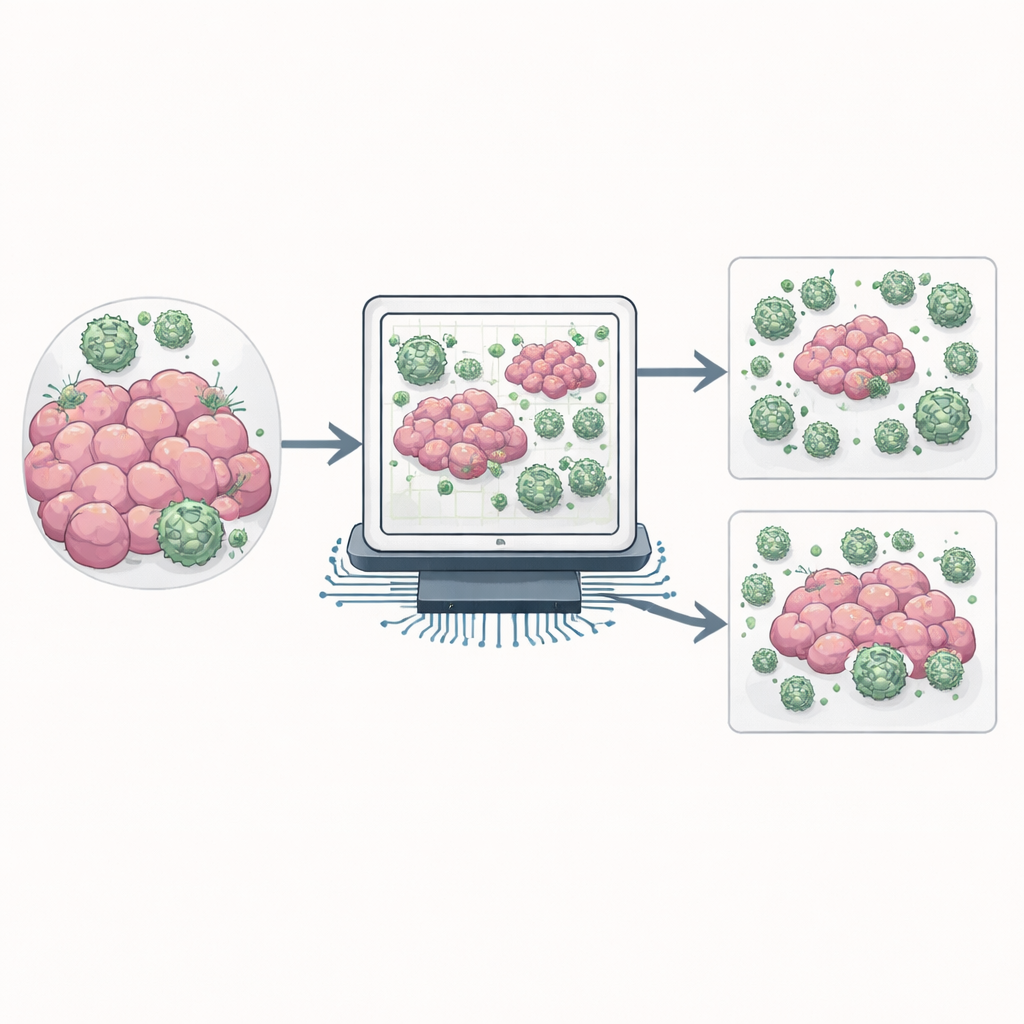
Att förvandla celler till digitala aktörer
ABMACT bygger på agentbaserad modellering, en teknik där varje cell blir sin egen lilla mjukvaruagent som kan röra sig, dela sig, dö eller angripa grannar enligt enkla regler. Författarna designade fyra huvudaktörer: tumörceller, aggressiva NK‑celler som kan döda tumörer, utmattade NK‑celler som förlorat sin kraft, och "vaksamma" NK‑celler som ligger lågt men kan rycka upp sig. Regler för hur dessa celler växer, tröttas ut, migrerar och byter tillstånd hämtas från befintliga laboratorie‑ och djurstudier och kodas in i simuleringen så att tusentals virtuella celler kan spela upp en miniatyr behandlingsförlopp.
Att lägga in cellens inre kopplingar
Modern enkelcellssekvensering avslöjar vilka gener som är aktiva i varje NK‑cell, men denna molekylära detalj är svår att översätta till beteende i hela organismen. ABMACT tar itu med detta genom att länka genaktivitetsmönster till praktiska egenskaper som hur sannolikt det är att en NK‑cell dödar en tumörcell eller hur många mål den kan eliminera innan utmattning. Teamet använde gen‑ och signalvägsdata från lymfom‑ och hjärntumörmodeller hos möss för att uppskatta hur specifika gener skjuter NK‑celler mot starkare eller svagare tumörkontroll. Dessa genbaserade effekter tilldelas slumpmässigt till individuella virtuella NK‑celler, vilket skapar en digital population som speglar den naturliga blandningen av starka och svaga mördare som ses i faktiska experiment.
Spela upp och utvidga djurexperiment
Forskarna testade ABMACT mot flera experiment där konstruerade NK‑celler användes för att behandla blodcancer och glioblastom hos möss. I lymfommodeller reproducerade simulatorn korrekt den förbättrade tumörkontrollen hos NK‑celler som konstruerats att uttrycka både en tumörigenkännande receptor och tillväxtsignalen IL‑15, jämfört med enklare produkter eller okonstlade celler. Den matchade inte bara uppmätta tumörstorlekar vid några tidpunkter, utan fyllde också i dag‑för‑dag‑ökningen och minskningen i tumörbörda, NK‑cells‑expansion, utmattning och uppkomsten av vaksamma celler. I glioblastommodeller följde ABMACT åter observerad tumörkontroll och förutsade till och med resultat i en separat kotillväxtstudie utan omkalibrering, vilket tyder på att dess regler fångar generella egenskaper i NK‑tumör‑strider.
Testa "tänk om"‑behandlingsval i kisel
Eftersom ABMACT körs på en dator kan det undersöka frågor som vore svåra eller dyra att testa i djur. Författarna varierade systematiskt cellegenskaper och doser för att ta reda på vilka spakar som mest påverkar tumörkontroll. De fann att förhållandet mellan NK‑celler och tumörceller, varje NK‑cells förmåga att upprepade gånger döda många mål, och deras grundläggande dödskraft betyder mer än att bara hålla cellerna vid liv längre. Simulerade uppföljningsbehandlingar visade att tidigare extra doser och produkter med högre dödskraft kan förhindra tumöromgång mer effektivt än sena, blygsamma förstärkningar. Modellen utforskade också hur dålig homing av NK‑celler, trånga vävnader eller låga syrefickor kan fördröja möten med tumörer och främja behandlingsmisslyckande.
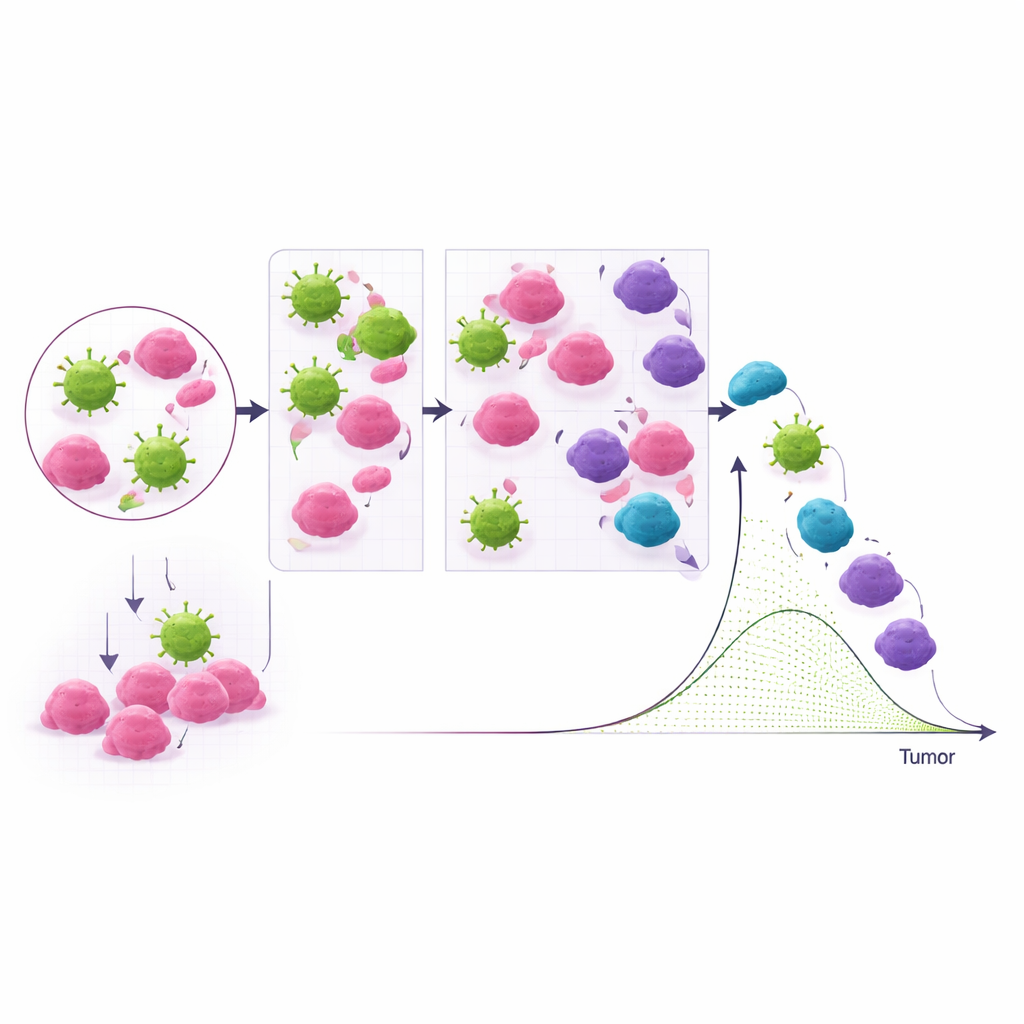
Vad detta betyder för framtida cellterapier
För en icke‑specialist kan ABMACT ses som en högupplöst flygsimulator för NK‑cellscancerterapier. Genom att förankra sina digitala celler i verkliga genetiska och experimentella data förklarar ramen varför vissa konstruerade NK‑produkter presterar bättre än andra och varför högre doser inte alltid ger bättre resultat. Den pekar på praktiska designregler: skicka tillräckligt många NK‑celler till tumören, gör dem till potenta seriemördare, och schemalägg behandlingar tidigt och genomtänkt i stället för att bara öka dosen. Även om sådana modeller inte kan ersätta laboratorie‑ och kliniska tester kan de begränsa antalet alternativ, minska beroendet av djurstudier och med tiden bidra till att skräddarsy cellterapier efter den enskilde patientens biologi.
Citering: Wang, Y., Casarin, S., Daher, M. et al. Agent-based modeling of cellular dynamics in adoptive cell therapy. Commun Biol 9, 409 (2026). https://doi.org/10.1038/s42003-026-09653-4
Nyckelord: adoptiv cellterapi, naturliga mördarceller, agentbaserad modellering, cancerimmunterapi, CAR‑NK