Clear Sky Science · sv
Modellval i preklinisk forskning på nukleinsyra‑terapier
Att omvandla gener till läkemedel
Nukleinsyra‑terapier är en ny typ av läkemedel som inte verkar genom att blockera proteiner, som de flesta läkemedel gör, utan genom att gå ett steg tidigare till nivån för våra genetiska budskap. Denna översikt förklarar hur forskare väljer rätt laboratorie‑ och djurmodeller för att testa dessa RNA‑inriktade läkemedel innan de når patienter. En allmän läsare kan ha intresse av detta eftersom genomtänkta modellval kan innebära snabbare, säkrare och mer effektiva behandlingar för genetiska sjukdomar, inklusive sällsynta barndomsrubbningar och vanligare tillstånd som hjärtsjukdom.
Vad gör dessa genetiska läkemedel annorlunda?
Nukleinsyra‑terapier (NATs) inkluderar korta strängar kallade antisense‑oligonukleotider (ASO) och små interfererande RNA (siRNA). I stället för att förlita sig på formen och kemin hos proteintargets känner dessa läkemedel igen sina mål via basparningsregler—samma A‑T och G‑C‑matchning som ligger till grund för DNA. Det gör dem programmerbara: när du vet vilken RNA‑sekvens du vill påverka kan du ofta designa många kandidatläkemedel snabbt utan år av traditionell kemi. Den svåra delen är inte längre "Kan vi skapa en aktiv förening?" utan "Hur mäter vi om den verkligen fungerar i en realistisk biologisk miljö?" Eftersom även en enda bokstavsskillnad i sekvensen kan avgöra aktivitet blir valet av rätt testsystem avgörande.
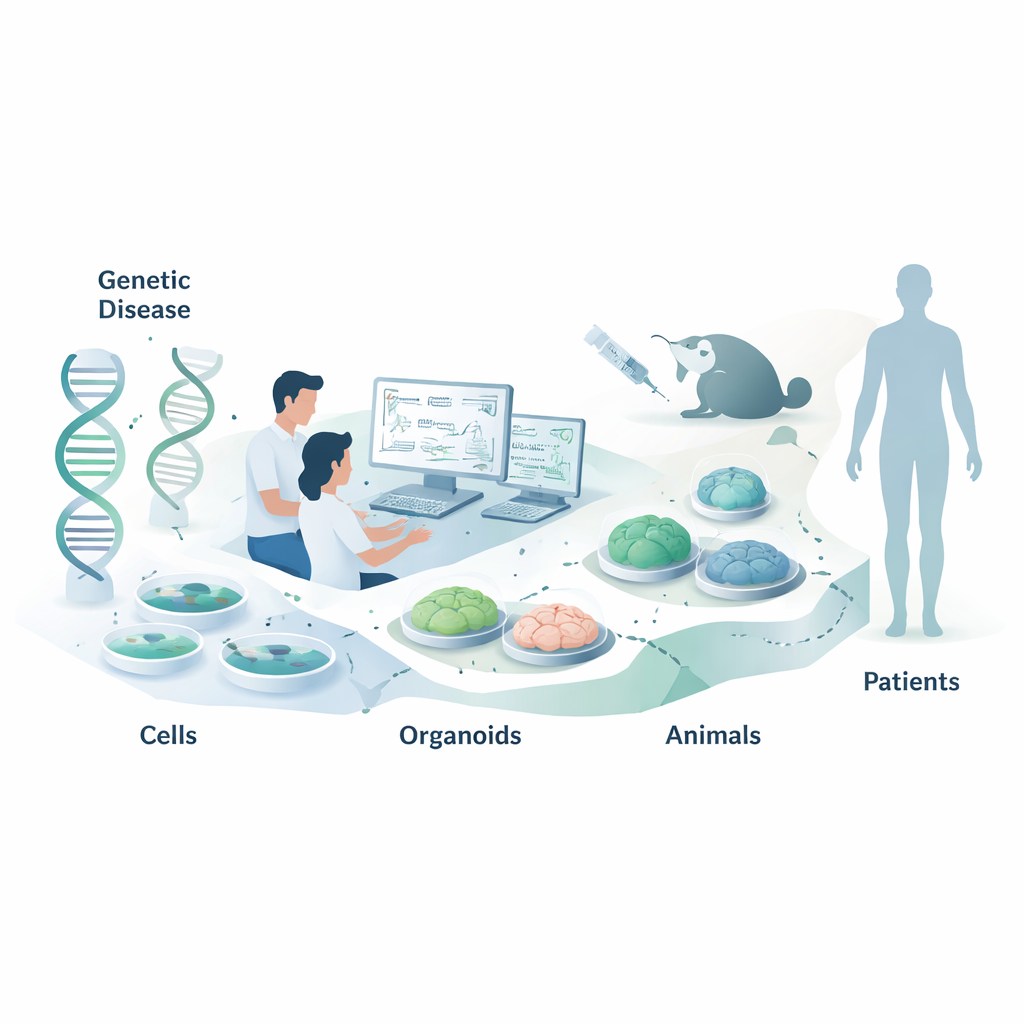
Enkla celltester: snabba men inte hela bilden
Första stoppet för de flesta NATs är en panel av relativt lättodlade cellinjer, som HeLa eller HEK293‑celler, som redan uttrycker mål‑RNA:t. Forskare tillsätter stora bibliotek av kandidat‑ASO:er eller siRNA:er och mäter sedan hur mycket mål‑RNA och dess protein minskar, med tekniker som PCR och Western blot. De kan också arbeta med celler härledda från patienter, vilket bättre fångar en persons exakta genetiska bakgrund och möjliggör tester av "allelselektiva" läkemedel som bara tystar den felaktiga kopian av en gen. När den naturliga genen inte uttrycks lämpligt inför forskare ibland konstgjorda mini‑gener eller reportarplasmider som lyser när RNA:t klipps eller korrekt splitsas. Dessa system är kraftfulla för att jämföra många designer snabbt, men de kan missa viktiga detaljer, såsom naturlig RNA‑struktur eller celltypsspecifik bearbetning, så resultaten måste bekräftas i mer realistiska sammanhang.
Från molekylära korrigeringar till verkligt cellbeteende
Många NATs syftar inte bara till att förstöra felaktigt RNA utan att reparera det genom att förändra splitsningen, processen som syr ihop bitar av genbudskapet. Noggrant designade ASO:er kan få celler att hoppa över ett skadligt exonn, återställa en saknad bit eller förhindra insättning av ett "pseudo‑exon" som bryter koden. För att se om sådana förändringar faktiskt förbättrar cellfunktionen går forskare bortom enkla avläsningar av RNA‑ och proteinnivåer. I patient‑härledda celler testar de om enzymaktivitet återkommer, om jontransport i lungceller normaliseras eller om signalvägar i immunceller svarar korrekt. I allt större utsträckning använder de tredimensionella organoider—mini‑vävnader odlade från patienters stamceller—som kan efterlikna hjärtslag, hjärnans nätverksaktivitet eller andra komplexa beteenden. Dessa 3‑D‑modeller ligger närmare verkliga organ men är svårare, långsammare och dyrare att använda, så team måste väga realism mot genomströmning.
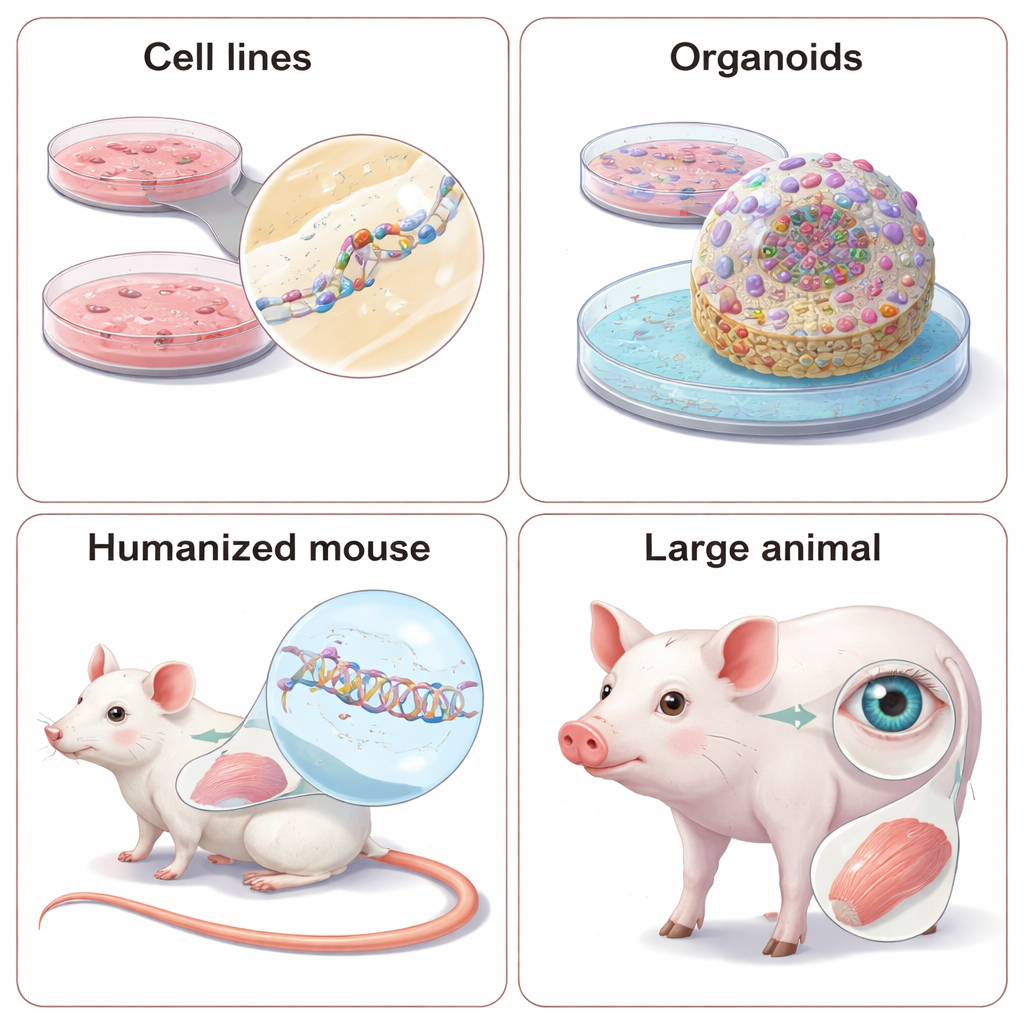
Varför djur fortfarande är viktiga—och hur man humaniserar dem
Vissa sjukdomsdrag, såsom helkroppsmetabolism, organ‑till‑organ‑interaktioner eller beteende, kan helt enkelt inte fångas i odlingar. För detta testas NATs i levande djur. Eftersom dessa läkemedel är beroende av exakta RNA‑sekvenser står forskare inför ett val: designa "surrogat"‑läkemedel som matchar djurets version av genen, eller omkonstruera djuret så att det bär mänskliga genetiska sekvenser. Surrogat‑ASO:er och siRNA:er kan visa om sänkning av en gen förbättrar symptom i väletablerade musmodeller, men de efterliknar inte perfekt det kliniska läkemedlet som riktar sig mot människor. Humaniserade modeller—möss eller till och med minigrisar med delar eller hela kopior av mänskliga gener—möjliggör testning av den verkliga kliniska kandidaten men kräver avsevärd tid och kostnad, och subtila skillnader i genreglering mellan arter kan fortfarande ge överraskningar. Översikten lyfter också fram ökad användning av stora djur, särskilt för sjukdomar i öga och muskel, där anatomien mer liknar människans.
Framåtblick: smartare modeller och mindre gissningar
Författarna drar slutsatsen att det inte finns en enda "bästa" modell för nukleinsyra‑läkemedel; i stället behöver varje projekt en skräddarsydd väg som börjar med snabba, enkla analyser och går vidare mot mer komplexa, mänskligt relevanta system. Eftersom tillsynsmyndigheter och finansiärer driver på för att minska djuranvändning förväntas sofistikerade organoider, organ‑på‑chip‑enheter och datormodeller ta en större del av bördan, särskilt i kombination med maskininlärningsverktyg som förutspår vilka sekvenser och kemier som fungerar bäst. I slutändan, genom att förstå styrkor och blinda fläckar hos varje modell—och genom att dela bästa praxis och data i hela fältet—kan forskare mer pålitligt omvandla programmerbara genetiska idéer till säkra, effektiva läkemedel för patienter.
Citering: Oliver, P.L., Hill, A.C. Model selection in preclinical nucleic acid therapeutics research. Commun Biol 9, 200 (2026). https://doi.org/10.1038/s42003-026-09650-7
Nyckelord: nukleinsyra‑terapier, antisense‑oligonukleotider, siRNA, prekliniska modeller, genterapi