Clear Sky Science · sv
Selektiv bindning av tvåvärt katjoner omformar nukleosommekanik och frigör histonsvansars dynamik
Hur små joner hjälper till att hantera vårt DNA
Inne i varje cell måste meter av DNA vikas, packas och ändå vara åtkomligt vid behov. Denna artikel undersöker hur två vanliga mineralkatjoner i våra celler, magnesium och kalcium, subtilt omformar hur DNA lindas runt proteiner och påverkar hur tätt vårt genetiska material är paketerat och hur lätt det kan läsas. Genom att simulera dessa interaktioner i atomär detalj visar författarna att förändringar i jonnivåer kan göra lokala DNA-strukturer styvare eller mer avslappnade och ändra beteendet hos flexibla proteintails som hjälper till att organisera kromosomer.
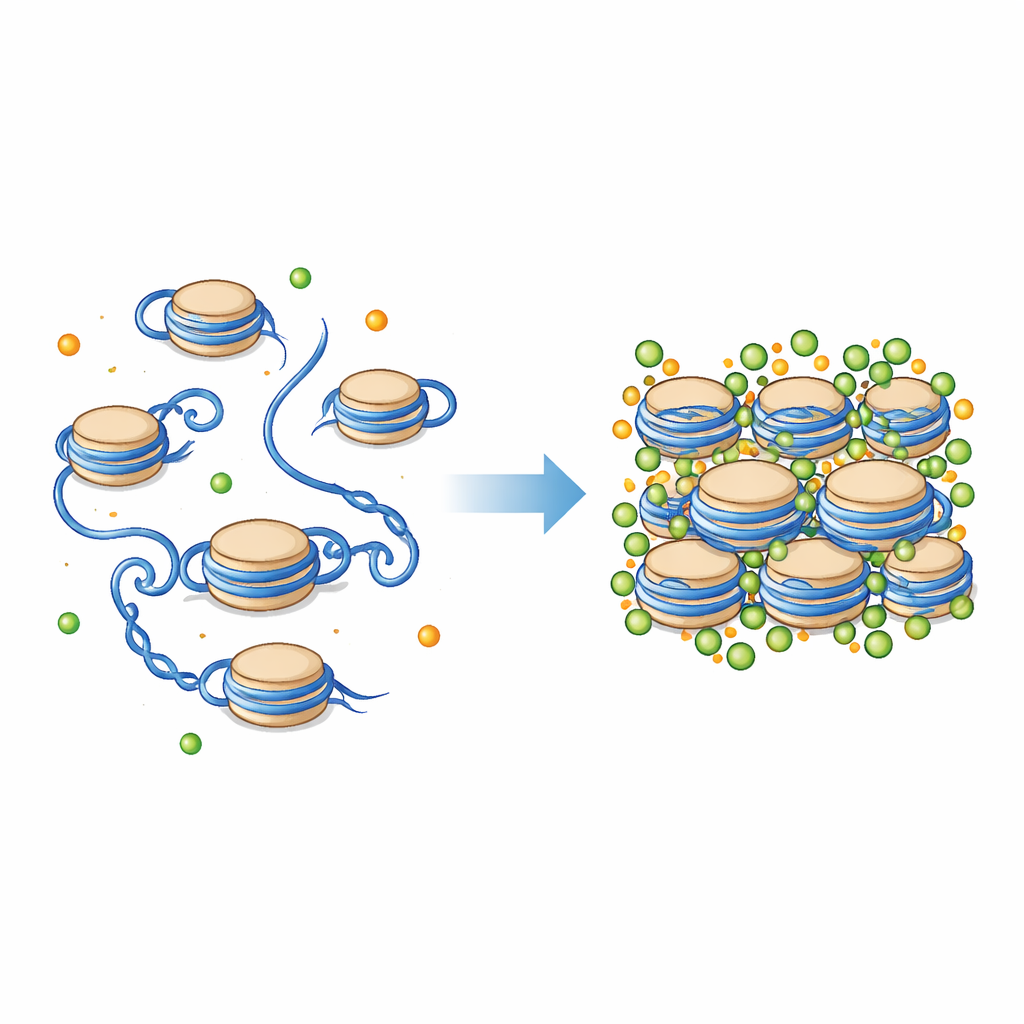
Kulan i hjärtat av kromatinpackningen
DNA i våra celler ligger inte löst; det är lindat runt proteinspolar som kallas nukleosomer. Varje nukleosom är en kort DNA-sträcka lindad runt en kluster av histonproteiner, med flexibla svansar som sträcker sig utåt. Tillsammans bildar dessa enheter den grundläggande "pärlor på en tråd"-strukturen i kromatin, som sedan kan vikas till tätare fibrer. Miljön runt nukleosomer är full av laddade partiklar, inklusive magnesium (Mg²⁺) och kalcium (Ca²⁺). Dessa joner är kända för att hjälpa kromosomer att kondensera, men exakt hur de påverkar de mycket små mekaniska detaljerna hos nukleosomer och deras histonsvansar har varit svårt att se direkt.
Simulera en trång atomvärld
För att avslöja dessa detaljer körde författarna 81 mikrosekunder av storskaliga datorsimuleringar där varje atom av DNA, protein, vatten och joner uttryckligen modellerades. De varierade systematiskt magnesium- och kalciumnivåer, testade olika sätt att beskriva jonernas beteende i simuleringarna och studerade nukleosomer med och utan sina histonsvansar. Genom att jämföra de simulerade jonbindningsmönstren med experimentella mätningar identifierade de en förfinad modell som bäst överensstämde med hur verkliga nukleosomer attraherar dessa joner, där magnesium föredrar DNA-gropar och kalcium oftare greppar DNA-ryggraden och vissa sura proteinplatser.
Hur joner trycker ihop DNA och gör kärnan styvare
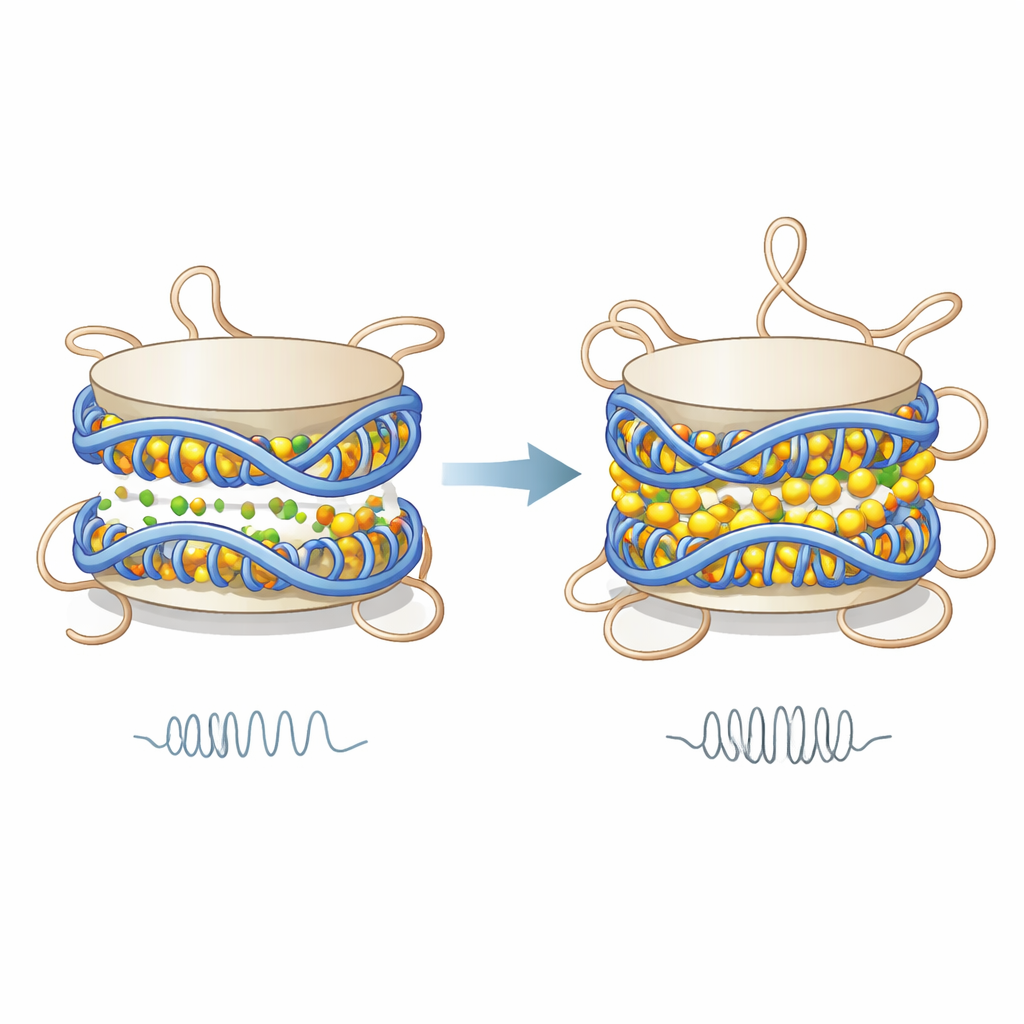
Simuleringarna visar att tvåvärda joner klustrar sig längs DNA-ytan och i det smala utrymmet mellan de två varven av DNA som vänder runt varje nukleosom. Genom att delvis neutralisera DNAs starka negativa laddning minskar dessa joner den elektriska repulsionen mellan närliggande DNA-varv. Resultatet är att de två DNA-spolarna dras närmare varandra, nukleosomen blir något kortare och dess mekaniska styvhet ökar, mätt med en modell som behandlar nukleosomen som en liten elastisk cylinder. Denna ökade styvhet beror inte på att DNA faller av eller större avlindningar; i stället uppstår den från subtila förändringar i avstånd och mer koordinerade rörelser i specifika DNA-regioner, som rör sig tillsammans som en mer stel enhet.
Frigörelse av de flexibla proteintailsen
Medan DNA-kärnan blir mer kompakt och styv, reagerar de flexibla histonsvansarna på motsatt sätt. Under förhållanden med få joner klänger positivt laddade aminosyror i dessa svansar sig fast vid det negativt laddade DNA och bildar många stabila kontakter. När magnesium eller kalcium binder längs DNA skärmar de av dessa laddningar och försvagar attraktionskrafterna mellan svansar och DNA. Författarna finner att kontakter mellan svansar—särskilt de från H3-histonen—och DNA minskar, uppehållstiderna på DNA blir kortare och svansarna provar ett bredare spektrum av positioner. Det betyder att svansarnas interaktioner med DNA blir mer frekventa men kortvariga, vilket gör dem mer dynamiska och potentiellt friare att nå intilliggande nukleosomer.
Vad detta betyder för genkontroll och kromatintillstånd
Tillsammans skisserar dessa fynd en dubbel roll för magnesium och kalcium i kromatin. Genom att dra åt DNA-inpackningen och öka nukleosomens styvhet främjar de mer kompakt, mindre flexibelt kromatin. Samtidigt, genom att luckra upp kontakterna mellan histonsvansar och DNA och öka svansarnas rörelser, blottar de viktiga platser som kan kemiskt modifieras eller kännas igen av reglerande proteiner. Eftersom jonkoncentrationer i kärnan fluktuerar med signaler och energianvändning, antyder detta arbete att små kemiska förändringar i den cellulära miljön kan ställa in både nukleosomernas mekaniska karaktär och åtkomsten till deras reglerande svansar, och därigenom hjälpa till att öppna eller stänga fönster av möjligheter för genaktivitet.
Citering: Hu, G., Zhang, H., Xu, W. et al. Selective binding of divalent cations reshapes nucleosome mechanics and unlocks histone tail dynamics. Commun Biol 9, 365 (2026). https://doi.org/10.1038/s42003-026-09648-1
Nyckelord: kromatin, nukleosommekanik, magnesium- och kalciumjoner, histonsvansar, genreglering