Clear Sky Science · sv
Tbr2-beroende parallella vägar reglerar utvecklingen av distinkta ipRGC-subtyper
Hur våra ögon mäter tid och form
Utöver att skapa bilder håller våra ögon också tyst kroppens klocka i takt, reglerar hur mycket pupillerna öppnar sig och hjälper oss att uppfatta allmän ljusstyrka. En liten population av specialiserade retinala nervceller, kallade intrinsically photosensitive retinal ganglion cells (ipRGCs), sköter mycket av detta arbete. De svarar på ljus med hjälp av ett pigment som heter melanopsin och skickar signaler djupt in i hjärnan. Den här studien ställer en grundläggande fråga med stora följder: hur delar en tidig grupp av utvecklande nervceller upp sig i flera olika ipRGC-typer, var och en kopplad till en särskild funktion?
En huvudströmbrytare, många ljussinnande celltyper
I musretinan härstammar alla sex kända ipRGC-subtyper från en tidig population av ganglieceller som aktiverar genen Tbr2. Denna gen fungerar som en huvudströmbrytare, som slår på program behövliga för att bilda ipRGCs och för att hålla melanopsingenen Opn4 aktiv. Men en enda huvudströmbrytare kan inte ensam förklara hur sex olika ipRGC-varianter uppstår, var och en med unika former, ljussvar och hjärnmål. Författarna använde RNA-sekvensering av utvecklande musretinas för att leta efter gener vars aktivitet beror på Tbr2. Bland en liten uppsättning kandidater utmärkte sig två: Irx1 och Tbx20, båda kända som regulatorer av cellidentitet i andra delar av kroppen. 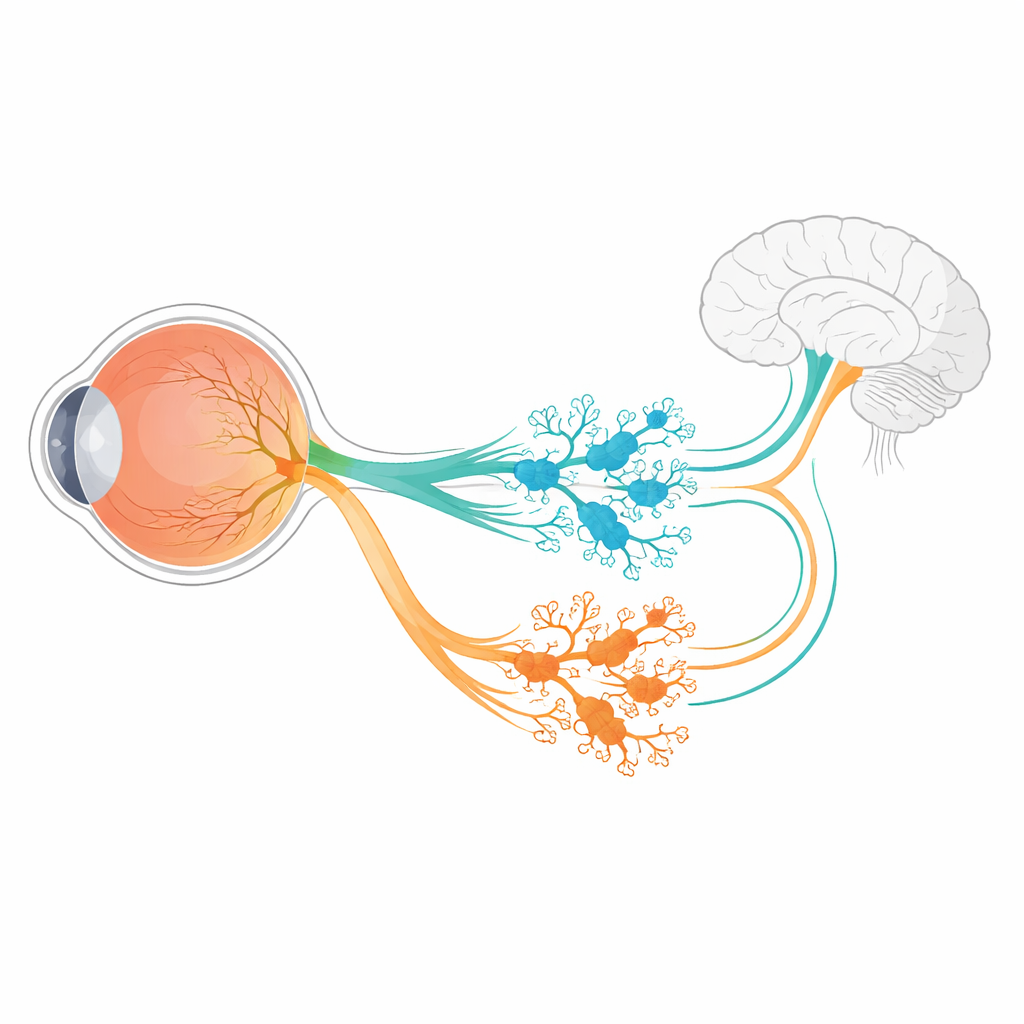
Två förgrenande vägar i retinan
Med nykonstruerade muslinjer som märker Irx1- och Tbx20-producerande celler med fluorescerande eller enzymatiska markörer följde forskarna var och när dessa faktorer slås på. De fann att Irx1 och Tbx20 uppträder i överlappande grupper av unga retinala ganglieceller kring mitten av dräktigheten, men snabbt sorterar sig i nästan helt separata uppsättningar hos vuxna. Irx1 finns mest i tre ipRGC-typer märkta M3, M4 och M5, medan Tbx20 koncentreras i M1, M2 och M6-celler, med endast liten överlappning i några M3- och M5-celler. Detaljerad bildtagning, elektriska inspelningar och spårning till hjärnan visade att varje faktor markerar en distinkt samling ipRGCs med karakteristiska dendritiska uppställningar, ljussvar och projektioner till specifika hjärnregioner som är inblandade i klockinställning, reflexer och visuell bearbetning.
Strömbrytare som finjusterar ljuskänslighet och cellsurvival
Teamet undersökte sedan vad som händer när vardera faktorn tas bort. När Irx1 slogs ut i utvecklande retina förblev antalet och den grundläggande strukturen hos Irx1-märkta ipRGCs i stort sett intakt, men deras melanopsinnivåer sjönk kraftigt. Med andra ord visade sig Irx1 vara nödvändig för att fullt ut slå på Opn4-ljusmätningsprogrammet i M3-, M4- och M5-celler, men inte för att bilda dessa celler i första hand. Tbx20 uppvisade ett annat beteende. Att ta bort Tbx20 minskade inte bara Opn4-uttrycket utan halverade också ungefär antalet Tbx20-positiva ipRGCs och senare minskade överlevnaden av dessa celler. Detta tyder på att Tbx20 hjälper både till att bygga och underhålla särskilda ipRGC-subtyper, särskilt M1, M2 och M6, samtidigt som den stödjer deras melanopsinbaserade ljuskänslighet. 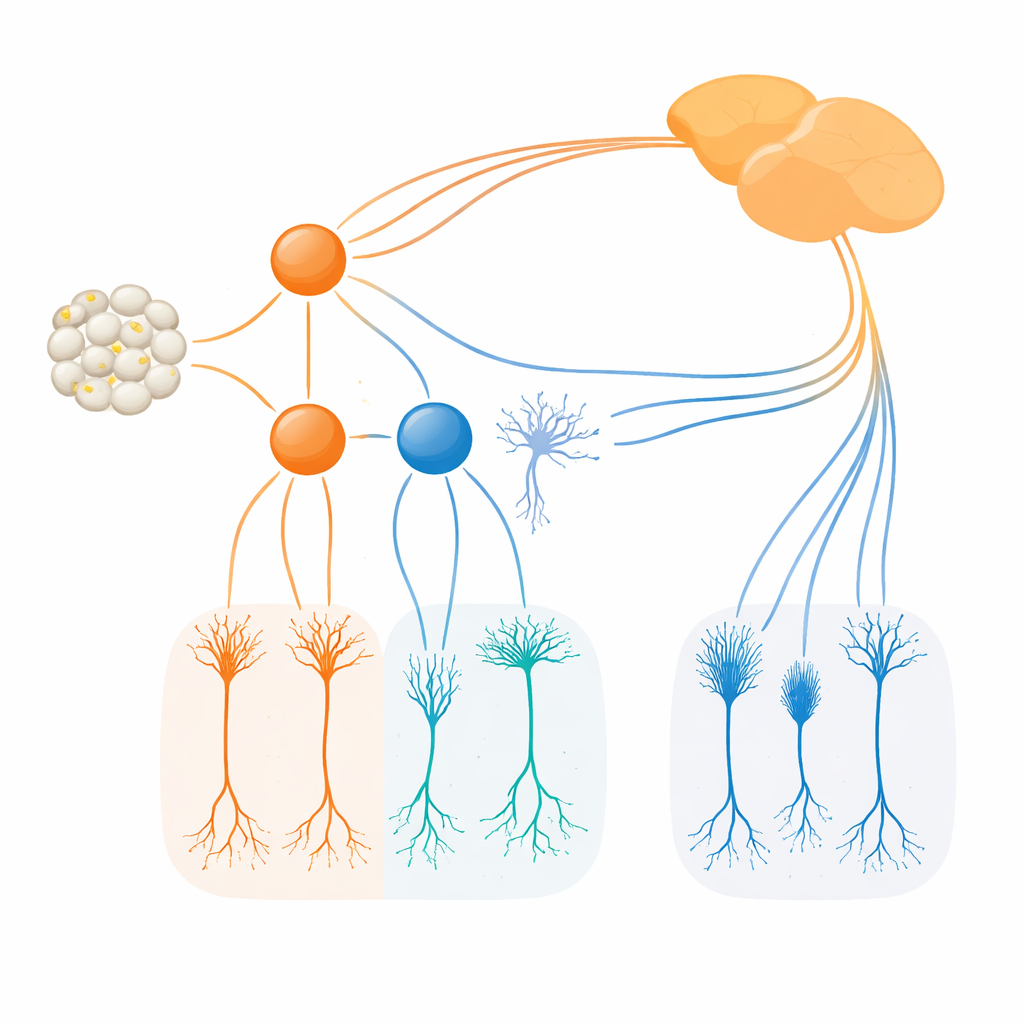
Tajma uppdelningen i distinkta cellfamiljer
Genom att tillfälligt aktivera genetiska rapportörer vid precisa embryonala dagar kunde författarna ”tidstämpla” celler som uttryckte Irx1 eller Tbx20 och följa deras öden in i vuxen ålder. Dessa experiment visade att Tbx20-märkta celler bestämmer sin slutgiltiga ipRGC-identitet något tidigare än Irx1-märkta celler, med de flesta beslut fastställda strax före födseln. Under ett kort fönster kan både Irx1 och Tbx20 samexistera i vissa celler, och dubbel-knockout-möss som saknar båda generna visade en mycket starkare förlust av melanopsin-positiva ipRGCs än någon av singlemutanterna. Detta tyder på att de två vägarna samarbetar övergående, för att sedan avvika och styra olika delmängder av ipRGCs längs separata utvecklingsspår.
Vad detta betyder för förståelsen av syn och hälsa
För en icke-specialist är huvudbudskapet att en enda tidig gen, Tbr2, inte verkar ensam. Istället matar den in i två parallella kontrollvägar, en centrerad kring Irx1 och den andra kring Tbx20. Dessa vägar bestämmer vilken typ av ipRGC en ung cell kommer att bli, finjusterar hur starkt den uppfattar ljus och avgör om den kopplar till hjärnregioner för kroppsklocksreglering, pupillreflexer eller andra visuella roller. Arbetet erbjuder ett tydligare kopplingsschema för hur våra interna "ljusmätare" byggs och lyfter fram specifika genetiska steg som kan vara inblandade när dessa celler går förlorade eller fungerar fel, med potentiell relevans för sömnstörningar, säsongsbundna humörförändringar och sjukdomar som skadar retinan.
Citering: Kiyama, T., Chen, CK., Altay, H.Y. et al. Tbr2-dependent parallel pathways regulate the development of distinct ipRGC subtypes. Commun Biol 9, 347 (2026). https://doi.org/10.1038/s42003-026-09645-4
Nyckelord: retinala ganglieceller, melanopsin, neuronal utveckling, circadianska rytmer, transkriptionsfaktorer