Clear Sky Science · sv
Strukturanalys visar att vattenmolekyler medierar självaktivering av GPR99
Varför denna receptor är viktig för inflammation
Våra luftvägar och andra vävnader känner ständigt av kemiska signaler som talar om infektion eller irritation. En sådan sensor, ett protein kallat GPR99 som sitter på cellens yta, framträder som en viktig brytare i inflammatoriska sjukdomar som astma och näspolypper. Denna studie förklarar, på atomnivå, hur GPR99 kan slå på sig själv även utan en yttre kemisk trigger — och hur små kluster av vatten hjälper till att göra det — vilket ger ledtrådar för design av nya antiinflammatoriska läkemedel.
En inbyggd på-knapp inne i en cellsensor
GPR99 tillhör en stor familj av cellytproteiner som förmedlar budskap från utsidan till insidan av cellen, ofta genom att ändra form och rekrytera partnerproteiner kallade G‑proteiner. Till skillnad från de flesta sådana receptorer är GPR99 ovanligt aktiv även när inget signalmolekyl är bundet. Författarna visar att en flexibel slinga på receptorens yttre sida, känd som den andra extracellulära loopen, beter sig som en intern nyckel: den viks in i det vanliga bindningsfacket, imiterar en aktiverande signal och slår på receptorn på egen hand.
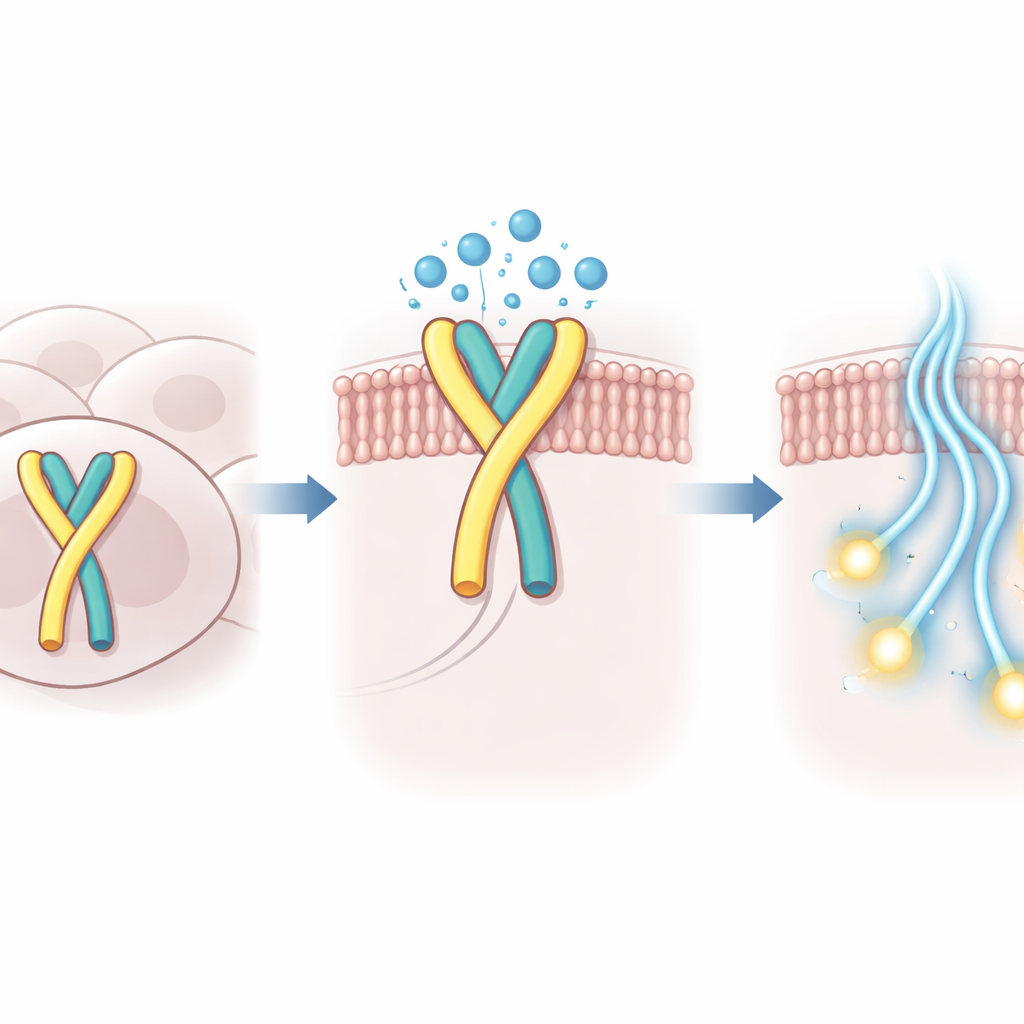
Hur vatten hjälper till att hålla brytaren på plats
Med högupplöst kryoelektronmikroskopi fångade forskarna den tredimensionella strukturen av mänskligt GPR99 bundet till sitt G‑proteinpartner i detta självaktiverade tillstånd. I bindningsfacket där externa molekyler normalt skulle sitta observerade de inte bara den inskjutna loopen utan också ett litet kluster av ordnade vattenmolekyler. Dessa vattenmolekyler bildar en polär bro mellan loopen och det omgivande proteinet, vilket kompenserar för loopens grundare inskjutning och stabiliserar receptorens aktiva form. När nyckelaminosyror i loopen eller i det närliggande facket förändrades så att dessa vattenmedierade kontakter försvagades, sjönk GPR99:s inbyggda aktivitet kraftigt i cellbaserade tester.
Omarbetning av det inre maskineriet för konstant signalering
Teamet jämförde sin självaktiverade struktur med andra familjemedlemmar, inklusive en närbesläktad receptor som binder den metabola biprodukten succinat och en aktiv form av GPR99 bunden till metaboliten 2‑oxoglutarat. De fann att GPR99 i frånvaro av någon extern ligand redan är fullt inställd i en aktiv konformation: flera bevarade ”mikrobrytare” i dess helixkärna antar former som normalt ses först när dessa receptorer stimuleras. Kritiska positioner som vanligtvis hjälper till att hålla receptorer i ett avstängt tillstånd ersätts eller omorienteras i GPR99, vilket lösgör interna spärrar och gynnar den öppna konfiguration som välkomnar G‑proteinpartnern.
Vidarebefordra budskapet in i cellen
På membranets inre sida visar strukturen hur GPR99 greppar det Gq‑typ G‑protein som förmedlar dess signal. En helixformad svans av G‑proteinet vilar i en klyfta som öppnas av att en av GPR99:s helixar svänger utåt och bildar ett nätverk av polära och hydrofoba kontakter med receptorens inre slingor och svans. Mutationer som stör detta gränssnitt minskar också signaleringen, vilket bekräftar att självaktiveringen som skapas av den yttre loopen och vattenklustret effektivt kopplas till intracellulära partner. Tillsammans kopplar dessa strukturella ögonblicksbilder förändringar vid receptorens yta till de kalciumvågor i cellerna som den utlöser.
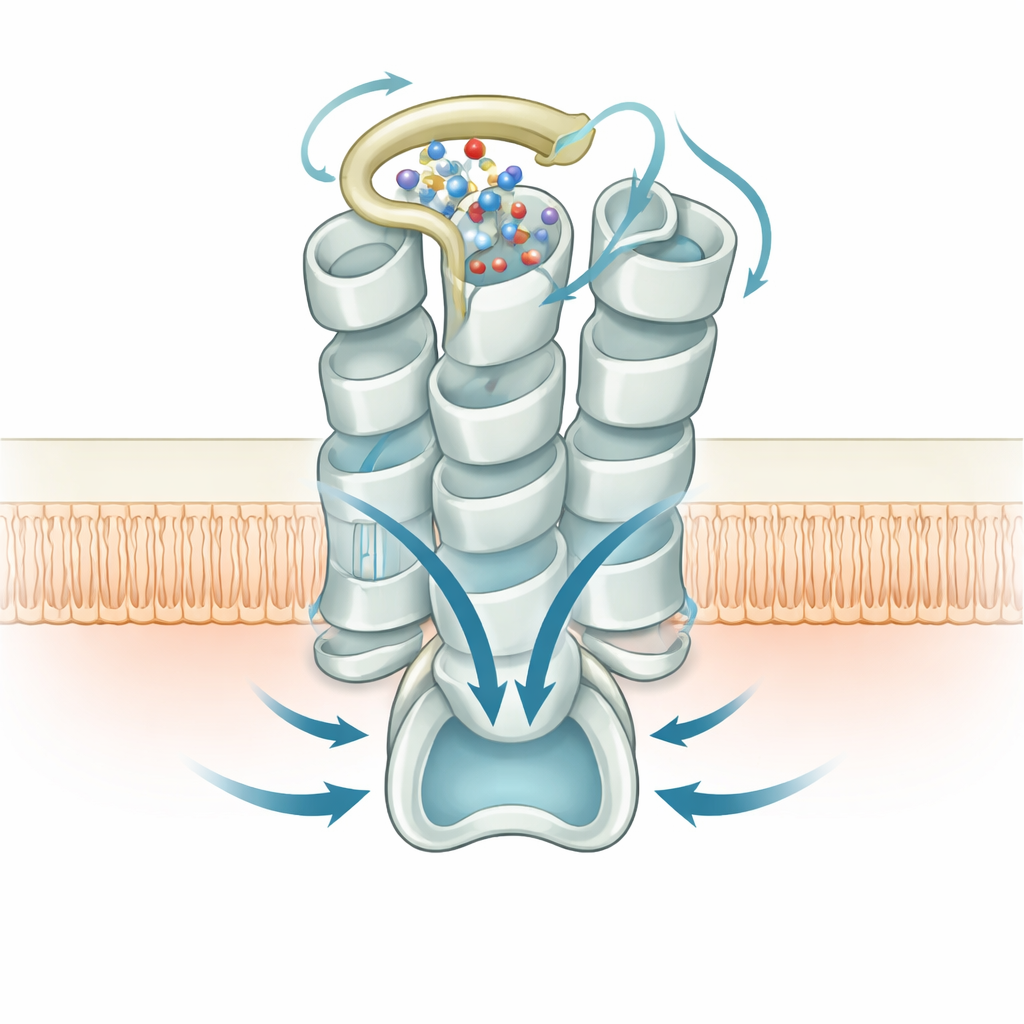
Konsekvenser för andning och vidare
Författarna föreslår att GPR99:s inbyggda aktivitet, förstärkt av strukturella vattenmolekyler, kan hålla luftvägsvävnader i ett ”standby”-läge — beredda att frisätta slem och sätta igång ett immunförsvar när inflammatoriska lipider eller metabola förändringar dyker upp. Eftersom GPR99 är mycket aktiv även utan externa signaler, och eftersom dess aktivering förlitar sig på en specifik loop‑och‑vatten‑arrangemang, erbjuder dessa strukturella insikter konkreta mål för läkemedelsdesign. Små molekyler som stör denna interna brytare eller dess vattennätverk skulle kunna dämpa överdriven inflammation, medan föreningar som finjusterar interaktionen kan utnyttja GPR99:s känslighet för terapeutisk nytta.
Citering: Xiao, M., Bao, X., Guo, Y. et al. Structural analysis reveals that water molecules mediate self-activation of GPR99. Commun Biol 9, 342 (2026). https://doi.org/10.1038/s42003-026-09644-5
Nyckelord: GPR99, GPCR-aktivering, strukturell biologi, inflammation, vattenmedierad signalering