Clear Sky Science · sv
Strukturell mekanism för anti-MHC-I-antikroppars blockering av inhibitoriska NK-cellsreceptorer i tumörimmunitet
Att låsa upp kroppens tysta cancermördare
Vårt immunsystem har en uppsättning kraftfulla väktare kallade naturliga mördarceller (NK-celler) som kan upptäcka och förstöra cancer- och virusinfekterade celler. Ändå lär sig tumörer ofta att tysta dessa väktare. Denna artikel visar, på atomär nivå, hur en speciellt utformad antikropp kan ta bort den där "mute-knappen" och återväcka NK-celler så att de angriper tumörer mer effektivt. Arbetet kombinerar banbrytande strukturbiologi med musförsök för att visa hur en antikropp kan komplettera befintliga cancerimmunoterapier.
Immunsystemets ID-brickor på våra celler
Varje cell i vår kropp visar molekylära "ID-brickor" på sin yta som kallas MHC klass I-molekyler. Dessa brickor hjälper immunceller att skilja normal vävnad från farliga celler som blivit cancerceller eller infekterade av virus. NK-celler skannar ständigt dessa brickor. När de känner igen normala mönster skickar inhibitoriska receptorer på NK-celler en lugnande signal som förhindrar angrepp. Tumörer behåller ofta dessa brickor synliga och använder dem som en skyddande sköld: så länge den inhibitoriska signalen flödar, håller NK-cellerna tillbaka och cancern kan växa.
En antikropp som griper skölden
Forskarna studerade en monoklonal antikropp kallad B1.23.2 som binder starkt till många mänskliga varianter av MHC klass I på tumörceller. Med hjälp av kryoelektronmikroskopi och röntgenkristallografi kartlade de exakt hur denna antikropp positionerar sig på MHC-ytan. B1.23.2 fäster vid en bevarad kam på MHC-molekylen—en α2-helix—utan att röra vid dess lätta kedjepartner och bara svagt påverkas av den presenterade peptiden. Det innebär att antikroppen kan känna igen ett brett spektrum av mänskliga MHC-A, -B och -C-molekyler med mycket hög affinitet, samtidigt som den är relativt okänslig för de specifika små proteinfragment som MHC presenterar.
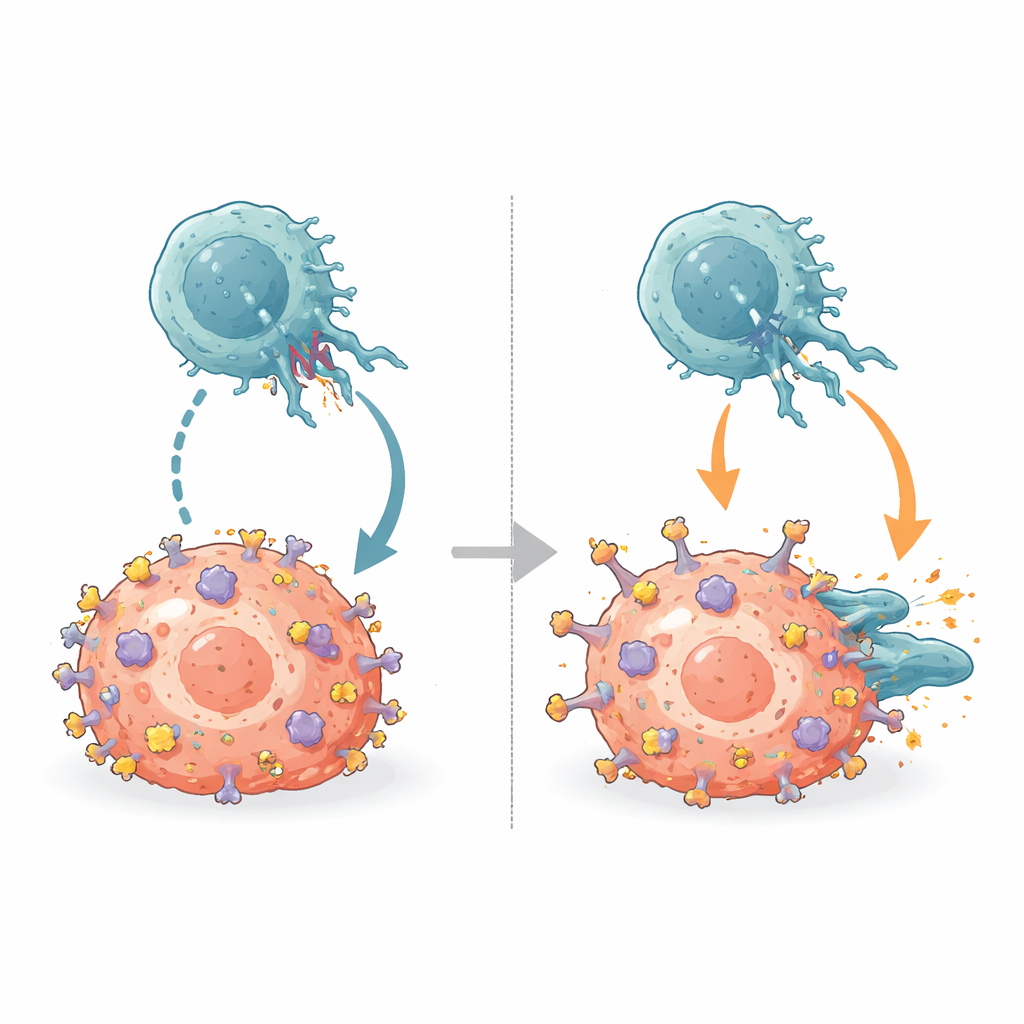
Att slå ut immunsystemets bromsar
NK-celler bär inhibitoriska receptorer kallade KIRs som normalt binder till samma α2-kam på MHC. Genom att jämföra de nya antikropp–MHC-strukturerna med kända KIR–MHC-strukturer visade teamet att B1.23.2 fysiskt ockuperar just den yta på MHC som KIRs behöver greppa. Antikroppens bindningsställe och KIRs fotavtryck överlappar så omfattande att båda helt enkelt inte kan binda samtidigt. B1.23.2 binder dessutom tätare till MHC än KIRs gör, vilket innebär att den vinner detta molekylära dragkamp. Som ett resultat, när antikroppen täcker tumörcellernas MHC-molekyler, kan inte KIRs på NK-celler längre leverera sina inhibitoriska signaler, och balansen skiftar mot NK-cellernas aktivering.
Finjustering av passformen och bred räckvidd
Även om B1.23.2 främst riktar sig mot den bevarade MHC-ytan fann författarna att små skillnader i den MHC-bundna peptiden subtilt kan justera antikroppens styrka. Genom att systematiskt byta ut en enskild aminosyraposition i peptiden visade de måttliga förändringar i bindningen—vanligtvis inom ungefär tiofaldiga skillnader—utan att förlora den övergripande igenkänningen. De undersökte också varför vissa vanliga MHC-typer, såsom HLA-A*02:01, undgår bindning. Genom att transplantera nyckelkontaktresiduer från en responsiv MHC-variant till HLA-A*02:01 konstruerade teamet versioner som antikroppen nu kunde känna igen, vilket bekräftade exakt vilka positioner som bildar den kritiska dockningsytan. Dessa insikter antyder att framtida antikroppsvarianter kan designas för att täcka ännu fler MHC-typer eller selektivt undvika andra.
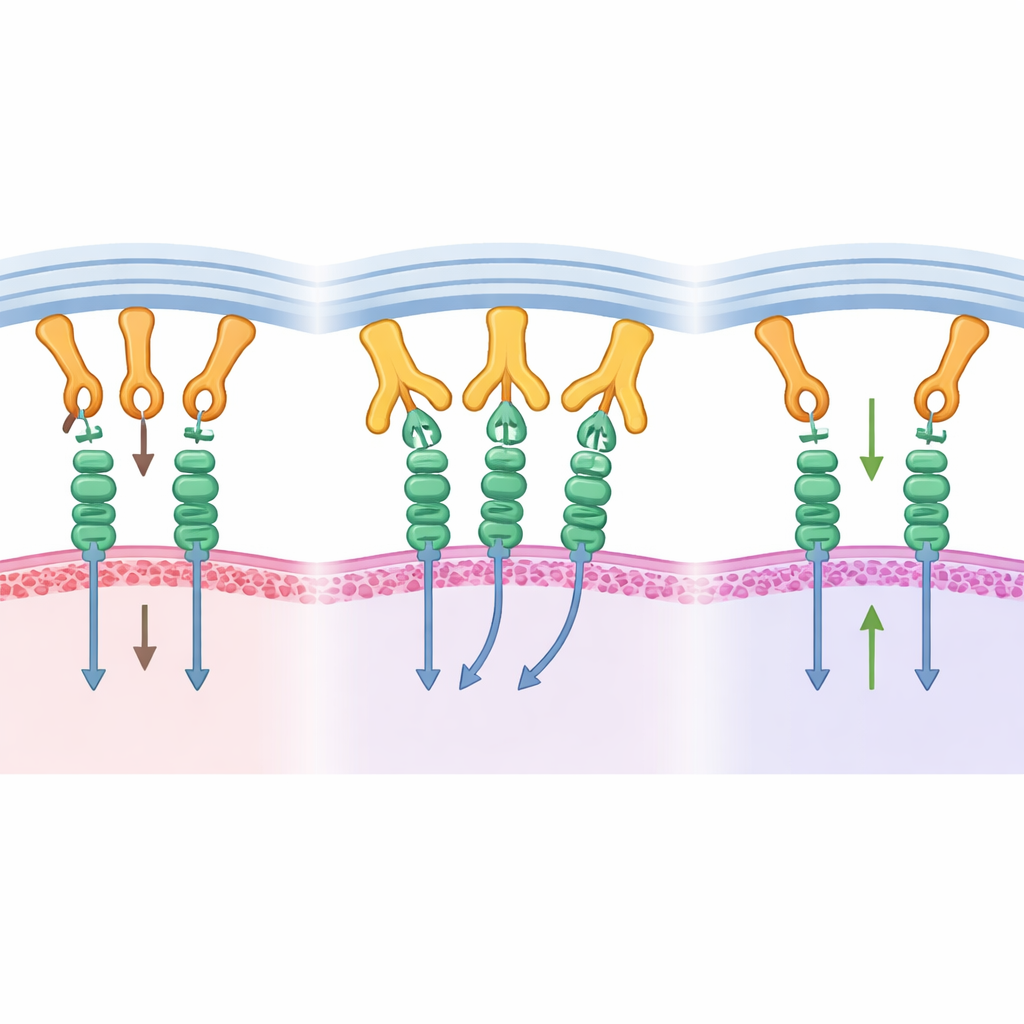
Att omsätta strukturell insikt i tumörkontroll
Hjälper denna molekylära blockering verkligen till att bekämpa tumörer? För att testa detta använde forskarna en humaniserad musmodell med en mänsklig pankreascancer. De konstruerade en form av B1.23.2 som inte kan signalera via sin egen Fc-ändstycke, så eventuella effekter skulle huvudsakligen komma från blockeringen av MHC–KIR-interaktionen. När mössen fick antikroppen tillsammans med mänskliga NK-celler växte tumörerna mycket långsammare. NK-celler uppvisade ökad proliferation, högre aktivitet i tillväxt- och signalvägar samt större produktion av inflammatoriska molekyler kopplade till död av cancerceller. Inuti tumörerna visade NK-celler fler aktiverande receptorer, i linje med att de frigjorts från konstant inhibitorisk påverkan.
Vad detta kan innebära för framtida cancerterapier
Med enkla ord visar denna studie hur en enda antikropp kan glida in mellan tumörceller och immunsystemets bromsar och stoppa den "attackera inte"-signal som normalt tystar NK-celler. Genom att kartlägga interaktionen i atomär upplösning och bekräfta dess effekter i djur erbjuder arbetet en ritning för en ny klass behandlingar: antikroppar som binder tumörens ID-brickor snarare än immunsystemets receptorer själva. Sådana medel skulle kunna kombineras med befintliga checkpoint-hämmare eller cellterapier för att mobilisera både NK-celler och T-celler, och ge immunsystemet en ytterligare angreppsvinkel mot svårbehandlade cancerformer.
Citering: Jiang, J., Panda, A.K., Natarajan, K. et al. Structural mechanism of anti-MHC-I antibody blocking of inhibitory NK cell receptors in tumor immunity. Commun Biol 9, 350 (2026). https://doi.org/10.1038/s42003-026-09641-8
Nyckelord: naturliga mördarceller, MHC klass I, cancerimmunterapi, monoklonala antikroppar, inhibitoriska receptorer