Clear Sky Science · sv
Periodisk trängd cellmigration driver partiellt reversibel kromatinomorganisation i cancercellinjer
Hur ihoppressade cancerceller minns att de utsatts för stress
Cancerceller som lossnar från en tumör måste krypa genom små springor i kroppens vävnader och blodkärl. För att göra det pressar de sina mjuka inre delar — och särskilt kärnan, som rymmer DNA — genom utrymmen som ibland är mindre än kärnan själv. I den här studien undersöks vad som händer med DNA:s förpackning under de upprepade ihoppressningarna och ställs en avgörande fråga: spänner kärnan helt enkelt tillbaka till det normala, eller kvarstår någon form av "mekaniskt minne" som kan underlätta att cancer sprids?
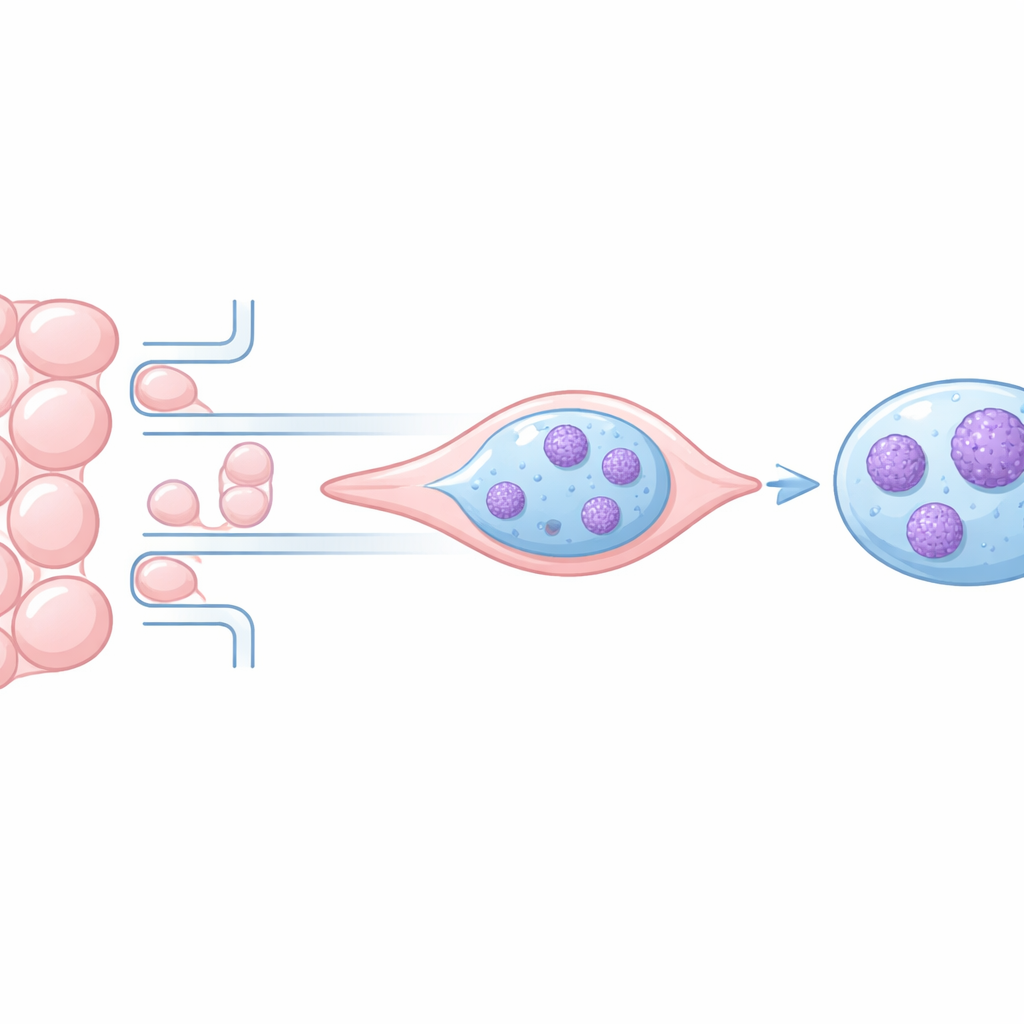
Varför DNA-packning betyder något när celler rör sig
Inuti kärnan är DNA lindat runt proteiner och vikt i kromatin, som kan vara löst packat eller tätt kondenserat. Lösare regioner tenderar att vara aktiva och hysa gener som ofta används, medan tätt packade regioner är mer tysta. När celler migrerar genom smala utrymmen deformeras kärnan, och tidigare arbete har visat att detta tillfälligt kan kompakta kromatin och till och med skada DNA. Men det var oklart om dessa förändringar helt återgår eller lämnar bestående spår som kan påverka hur aggressiva cancerceller blir.
En liten labyrint för att pressa enskilda cancerceller
Forskarna byggde en specialanpassad mikrofluidisk enhet — en genomskinlig chip med dussintals mikroskopiska kanaler som växlar upprepade gånger mellan breda och smala segment. Två olika cancercellinjer, båda konstruerade så att deras kromatin lyser under mikroskopet, leddes att krypa genom dessa kanaler med hjälp av ett kemiskt attraktant. Högupplöst tidsförloppavbildning gjorde det möjligt för teamet att följa varje cellkärna när den rörde sig, mäta kärnans yta och kartlägga ljusa, starkt kondenserade kromatinkluster bild för bild i mer än 100 individuella celler.
Vad som händer med kärnan under tryck
När en cell gick in i en smal trång passage krympte dess kärna abrupt i projicerad area, vilket speglade en reversibel minskning av kärnvolymen. Samtidigt ökade andelen av kärnan som upptogs av starkt kondenserat kromatin kraftigt — ofta två- till trefaldigt — för att sedan sjunka tillbaka till utgångsvärdet när cellen kom ut i ett bredare avsnitt. Detta mönster upprepades över flera på varandra följande trånga passager och i båda cancercelltyperna, vilket tyder på att den totala mängden tät kromatin är ett flexibelt, kortsiktigt svar på mekanisk stress snarare än en permanent förändring. En närmare granskning av fluorescensmönstren visade dock att pixlar med både mycket hög och mycket låg intensitet ökade under ihoppressningen, vilket anspelade på en mer komplex intern omorganisation än en enkel, enhetlig komprimering.
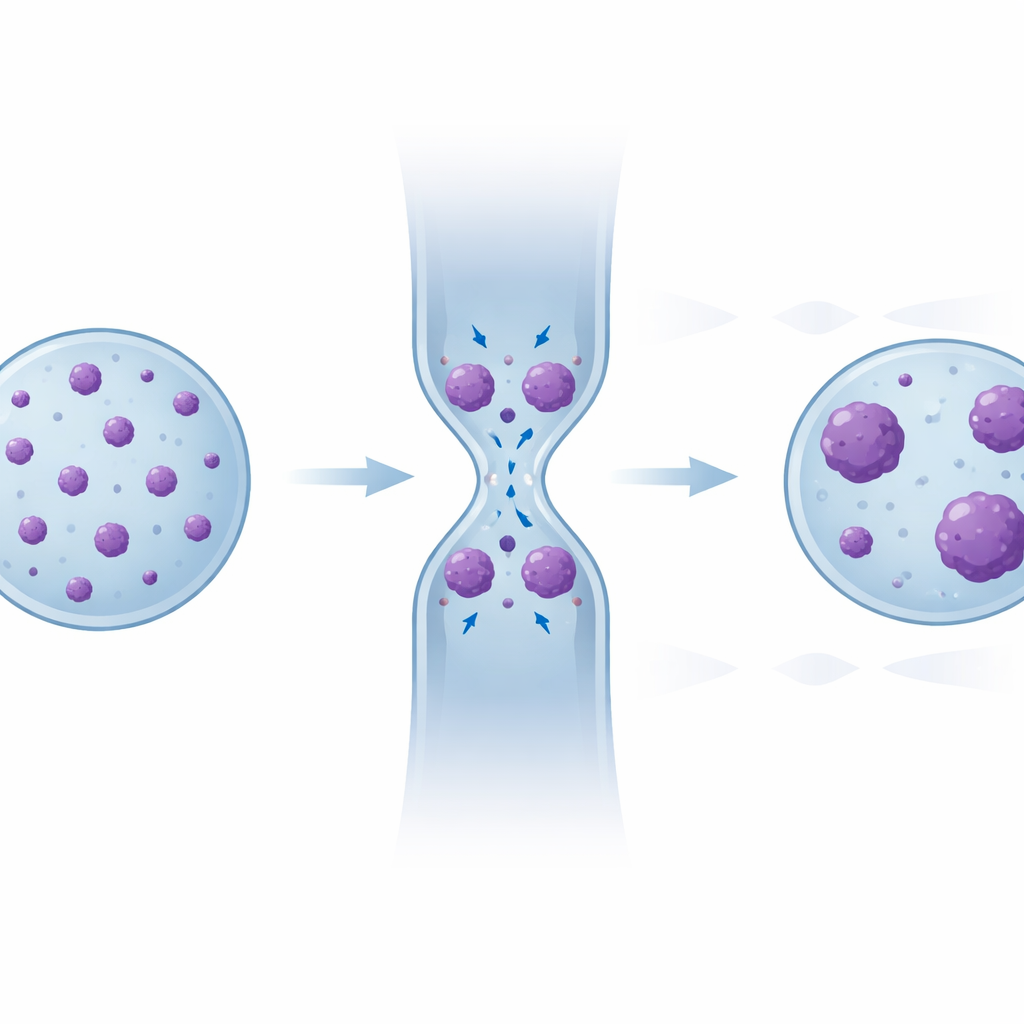
Dolt minne i mönstret av DNA-kluster
För att avslöja den dolda omorganiseringen undersökte teamet varje enskilt kondenserat kromatinkluster — dess storlek och hur många sådana kluster varje kärna innehöll — före, under och efter trängseln. Under ihoppressningen tenderade små kluster att gå samman till större. Efter att kärnan återhämtat sig återvände den totala kondenserade ytan till sin ursprungliga nivå, men mönstret gjorde det inte: jämfört med starttillståndet visade celler som passerat flera trånga passager färre kluster totalt sett, förskjutna mot större storlekar. Statistiska jämförelser bekräftade att fördelningarna i senare "återhämtnings"-regioner gradvis liknade de som observerats under trängseln. Immunofluorescensfärgning visade dessutom att många av dessa täta regioner överlappade med etablerade "tysta" kromatinmarkörer, och en datorbaserad modell av kromatin som en interagerande polymer återskapade denna partiella men inte fullständiga återhämtning enbart utifrån fysiken hos klibbiga DNA-segment som förts samman genom deformation.
Vad detta betyder för cancerspridning och framtida terapier
I vardagliga termer visar studien att när cancercellkärnor upprepade gånger pressas uppträder deras DNA-packning som en stressboll med minne. Kärnan kan återfå sin storlek, och den totala mängden tät packning kan återställas, men det detaljerade mönstret av täta DNA-kluster återgår inte fullt ut till ursprungstillståndet. Efter många ihoppressningscykler får kärnan färre, större täta regioner, vilket potentiellt förändrar vilka gener som blir lättare eller svårare att nå. Detta "mekaniska minne" skulle kunna hjälpa cancerceller att bättre tåla framtida deformationer när de invaderar nya vävnader. Att förstå och så småningom rikta in sig på denna koppling mellan fysiska krafter och DNA-organisation kan öppna nya vägar för att begränsa metastas genom att störa hur cancerceller anpassar sig till mekanisk stress.
Citering: Blazquez-Romero, M.d.V., Mendivil-Carboni, M., Sarasquete-Martinez, M. et al. Periodic confined cell migration drives partially reversible chromatin reorganization in cancer cell lines. Commun Biol 9, 366 (2026). https://doi.org/10.1038/s42003-026-09637-4
Nyckelord: trängd cellmigration, kromatinkondensering, nukleär mekanik, mekaniskt minne, cancermetastas