Clear Sky Science · sv
PTBP1 stöder musens spermatogenes genom att underlätta cytoskelettets organisation via mTORC2–PKCα-vägen i Sertoliceller
Varför denna studie är viktig för manlig fertilitet
Manlig infertilitet kan ofta te sig gåtfull, men i grunden bygger den på ett fint avvägt samspel mellan de utvecklande spermierna och de ”nurse”‑celler som stödjer dem. Denna studie undersöker en av de dolda molekylära medhjälparna inne i dessa stödjeceller och visar hur dess bortfall kan stoppa spermieproduktionen. Att förstå detta dolda kontrollager kan peka mot nya diagnostiska metoder eller behandlingar för vissa former av manlig infertilitet.
Stödcellerna som gör spermier möjliga
Spermier bildas inne i långa, slingrande tubuli i testikeln som kallas seminifera tubuli. Längs dessa tubuli ligger Sertoliceller, en specialiserad stödkelltyp som omsluter utvecklande germceller, ger dem näring och vägleder dem när de delar sig och mognar till spermier. Sertoliceller bygger också en skyddande barriär kallad blod–testis‑barriären, som skiljer tidiga celler från immunsystemet. För att utföra allt detta förlitar de sig på ett internt skelett av aktinfilament och mikrotubuli som ständigt ombyggs när vågor av germceller rör sig genom tubuli. Om detta skelett störs läcker barriären och mognande germceller kan lossna eller dö, vilket hotar fertiliteten.
En liten RNA‑chef med ett stort uppdrag
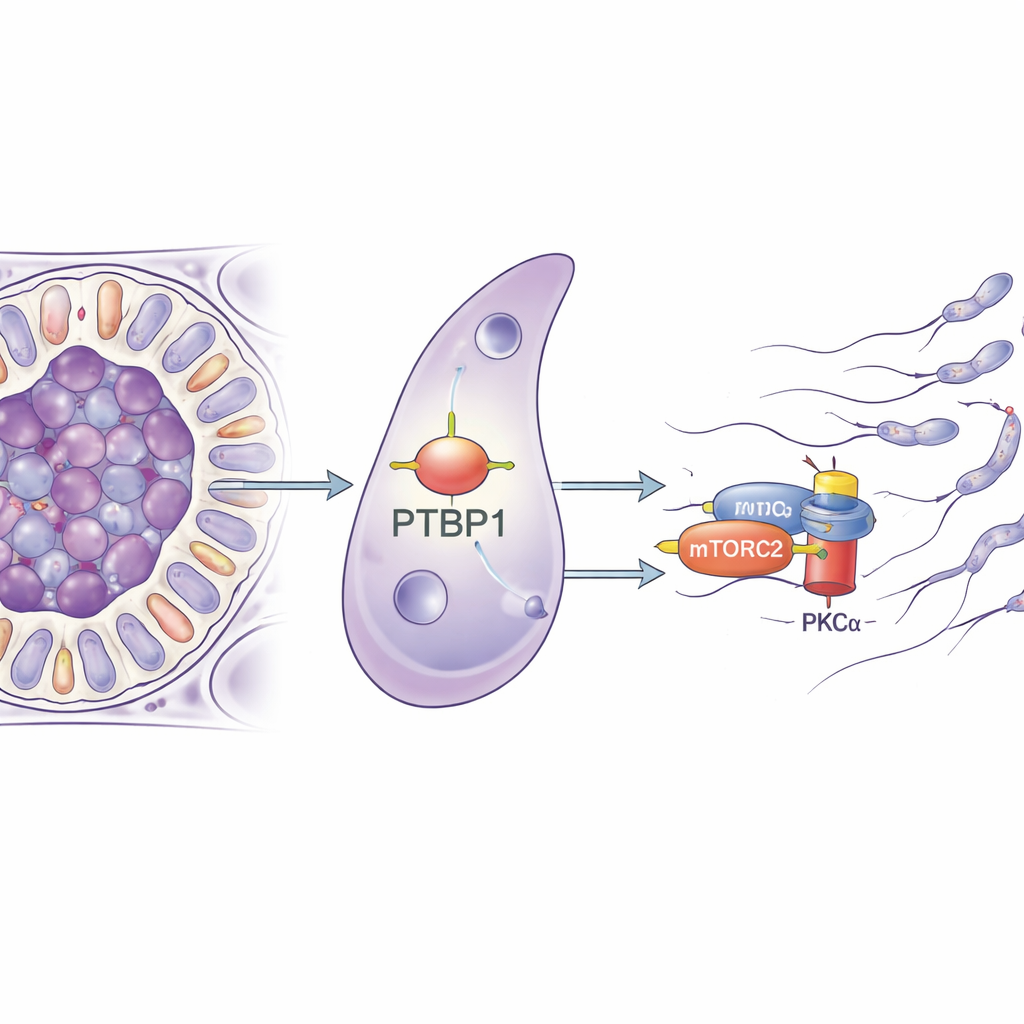
Forskarna fokuserade på ett protein kallat PTBP1, mest känt för sin roll i hanteringen av RNA‑molekyler i celler — att bestämma hur gener splitsas, hur stabila deras budskap är och hur effektivt de översätts till protein. PTBP1 är rikligt i både germceller och Sertoliceller, och tidigare studier visade att borttagning av det från germceller försämrar spermieproduktionen. I denna studie tog teamet bort PTBP1 specifikt i Sertoliceller hos möss. Vid en första anblick verkade de unga mössen normala, men när de nådde sexuellt vuxen ålder krympte testiklarna, antalet spermier i bitestikeln rasade och inga hannar kunde få avkomma, vilket visade en fullständig förlust av fertilitet.
När den cellulära stommen faller samman
Mikroskopisk undersökning av testiklarna från dessa möss visade att spermatogenesen avstannade halvvägs. Många tubuli innehöll tomma utrymmen, onormala klumpar av sammanfuse germcellkärnor och en brist på fullt förlängda spermier. Sertolicellernas kärnor, som normalt ligger intill tubulins yttre vägg, var ofta förskjutna mot mitten, vilket tyder på att dessa stödjeceller tappade sitt grepp om omgivningen. Färgning för viktiga junction‑komponenter och strukturella proteiner bekräftade att blod–testis‑barriären försvagats och att de vanliga täta buntarna av aktinfilament ersatts av oorganiserade, överintense stråk som sträckte sig från basen till tubulins centrum. En spårmolekyl som normalt stannar på ”blodsidan” av barriären läckte i stället djupt in i tubuli, vilket direkt demonstrerar barriärens sammanbrott.
Spåra felet tillbaka till en signalväg
För att förstå hur ett RNA‑bindande protein kunde leda till sådana mekaniska problem renade teamet Sertoliceller och analyserade vilka gener som förändrade sin aktivitet när PTBP1 saknades. Många av de påverkade generna var involverade i kontrollen av cellens skelett och i hur celler adhererar till varandra, vilket pekar på ett brett ombyggnadsfel. Forskarna drog sedan ner de RNA‑molekyler som fysiskt binder PTBP1 och fann att det fäster vid budskapet för Rictor, en kärnkomponent i ett signaleringskomplex kallat mTORC2. Detta komplex aktiverar i sin tur ett enzym kallat PKCα som formar aktinfilamenten. I Sertoliceller utan PTBP1 minskade mängden RICTOR‑protein och PKCα var mycket mindre aktivt, även om den underliggande Rictor‑RNA‑nivån knappt förändrades. Detta tyder starkt på att PTBP1 hjälper Sertoliceller att producera tillräckligt med RICTOR‑protein från dess RNA‑budskap och därigenom håller mTORC2–PKCα‑vägen igång.
Återställa stommen genom att återupprätta signalen
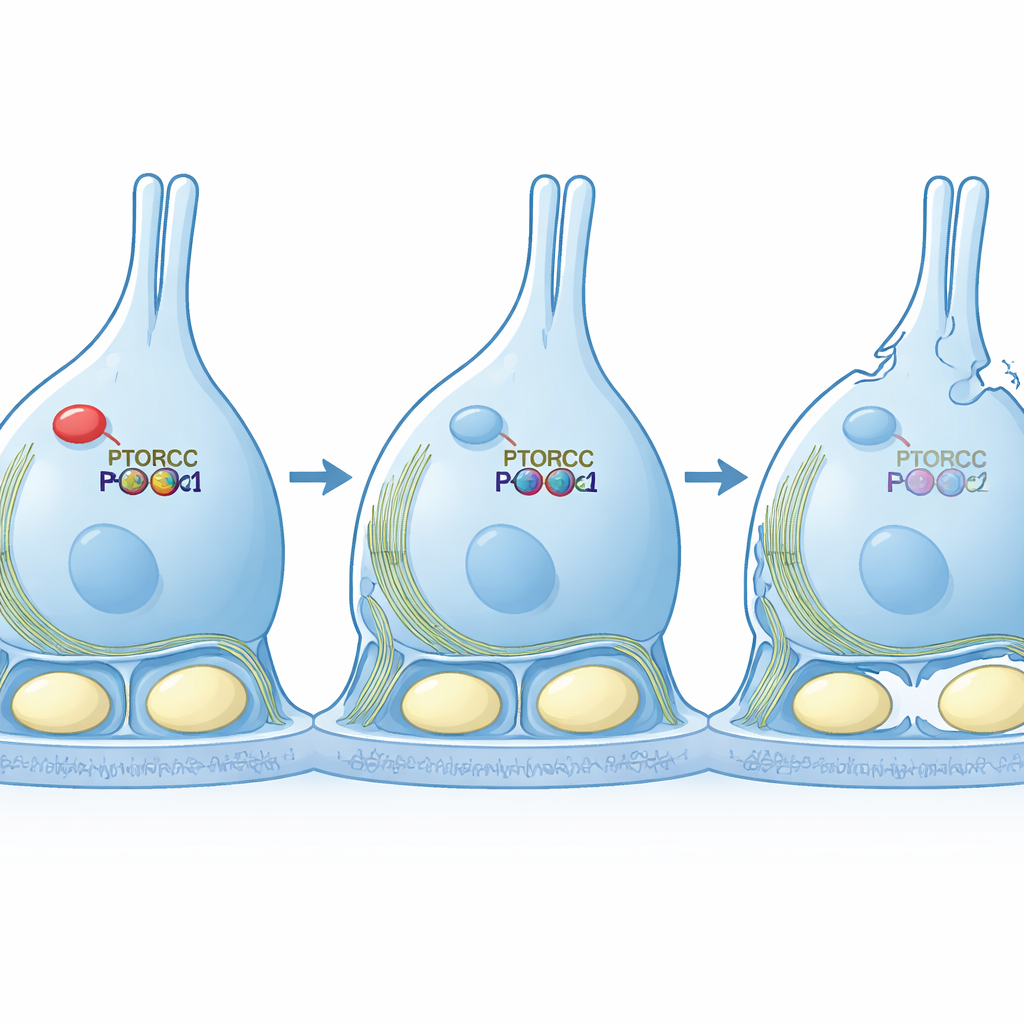
Teamet gick sedan vidare till cellkulturmodeller för att testa kausalitet. När de minskade PTBP1 i en Sertoli‑lik cellinje sträckte sig cellerna ut i långa, tunna former och visade ett rotat aktinnätverk — kännetecken för försvagad mTORC2‑signalering. Viktigt är att när de tvingade dessa celler att producera en permanent aktiv version av PKCα återfick cellerna sin normala, kompakta form och mer ordnade aktinstrukturer, även om RICTOR i sig förblev låg. Detta räddningsexperiment visar att PTBP1:s huvuduppgift i detta sammanhang är att hålla mTORC2–PKCα‑vägen tillräckligt aktiv för att organisera cellens interna skelett.
Vad detta betyder för förståelsen av infertilitet
Enkelt uttryckt avslöjar detta arbete en beroendekedja inne i testikeln: PTBP1 hjälper Sertoliceller att bygga en viktig signaleringsnod; den noden ordnar deras inre skelett; och ett intakt skelett gör att de kan hålla fast och skydda utvecklande spermier. Bryt kedjan vid PTBP1 och Sertoliceller tappar sin struktur, den skyddande barriären sviktar och spermieutvecklingen kollapsar, vilket resulterar i manlig infertilitet. Även om forskningen är gjord i möss finns samma molekyler hos människor, vilket väcker möjligheten att subtila defekter i RNA‑kontroll i Sertoliceller kan ligga bakom vissa oförklarade fall av manlig infertilitet och erbjuder en ny uppsättning molekylära mål för framtida studier.
Citering: Ozawa, M., Taguchi, J., Mori, H. et al. PTBP1 supports mouse spermatogenesis by facilitating cytoskeletal organization through the mTORC2–PKCα pathway in Sertoli cells. Commun Biol 9, 341 (2026). https://doi.org/10.1038/s42003-026-09636-5
Nyckelord: manlig fertilitet, Sertoliceller, spermatogenes, cytoskelett, RNA-bindande proteiner