Clear Sky Science · sv
Negativ reglering av NF-κB‑vägen av ubiquitinligasen Nedd4-1(NE)
Varför det är viktigt att stänga av inflammation
Vårt immunsystem förlitar sig på snabba inflammationstoppar för att bekämpa infektioner och läka skador, men samma krafter kan skada vävnader och främja cancer om de förblir aktiverade för länge. Denna artikel undersöker hur mänskliga och andra primatceller undviker den risken genom att använda en nykaraktäriserad inbyggd "broms" som dämpar ett av kroppens centrala larm-system när dess uppgift är slutförd.
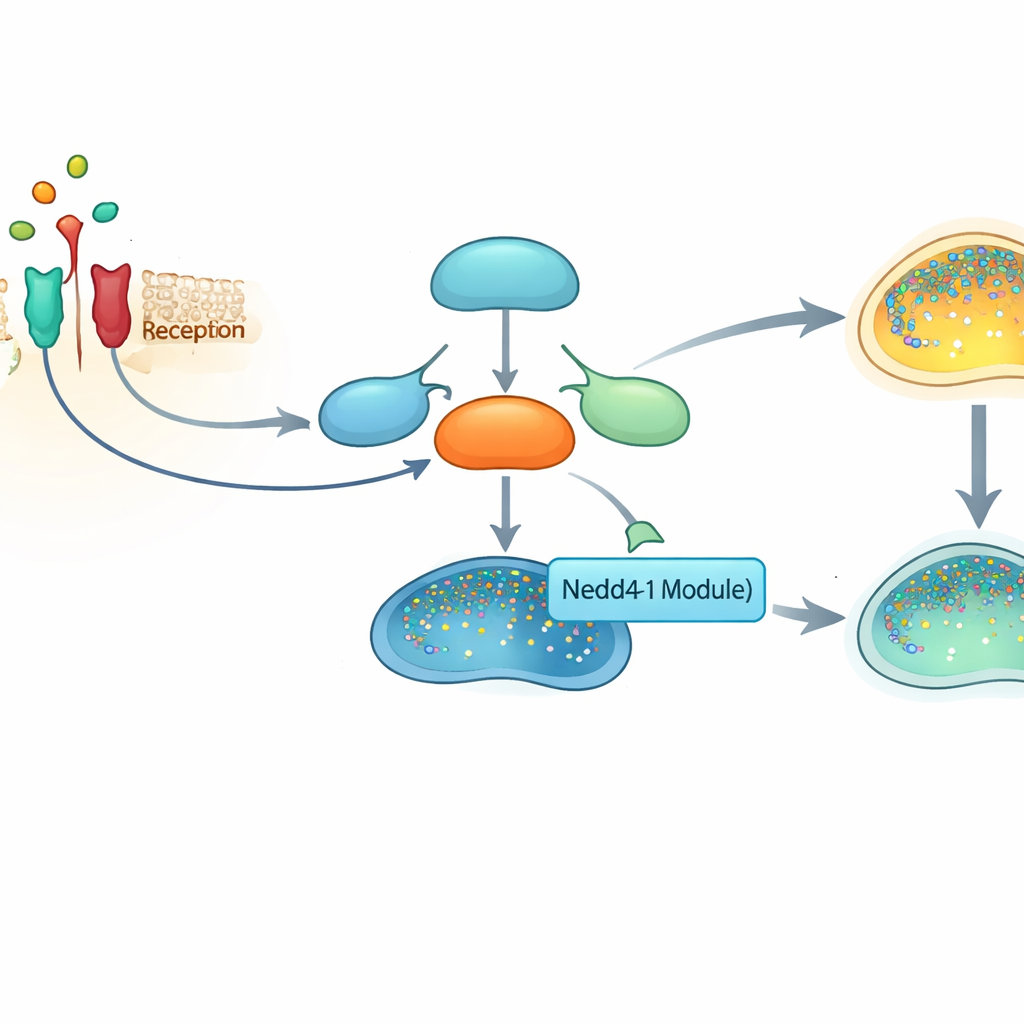
En central larmbrytare i våra celler
I centrum för den här berättelsen står NF-κB, en familj proteiner som fungerar som en huvudbrytare för hundratals gener involverade i inflammation, cellsöverlevnad och immunitet. När celler uppfattar stressignaler som den inflammatoriska molekylen TNFα, frigör en kedja av händelser NF‑κB från dess proteinkomplex i cellens vätskeomgivning och tillåter det att röra sig in i kärnan, där det aktiverar proinflammatoriska och proöverlevnads‑gener. Eftersom denna väg är så kraftfull måste cellerna finjustera både dess aktivering och avstängning. Misslyckande att stänga av den har kopplats till kroniska inflammatoriska sjukdomar och många cancerformer.
En broms som bara finns hos primater
Forskningen fokuserade på Nedd4-1, en medlem av en stor familj enzymer som märker andra proteiner med en liten molekyl kallad ubiquitin. Denna märkning signalerar ofta att proteiner ska brytas ner eller flyttas inom cellen och omformar signalnätverk. En tidigare upptäckt splice‑variant av Nedd4-1, kallad Nedd4-1(NE), finns endast hos primater och bär på ett långt extra segment i sin främre ände som ändrar var den lokaliseras i cellen och vad den känner igen. I kontrast till standardformen av Nedd4-1, som faktiskt kan öka NF‑κB‑aktivitet via andra partners, fann teamet att Nedd4-1(NE) har motsatt effekt: den dämpar NF‑κB‑signalering, särskilt efter långvarig exponering för TNFα.
Två sätt att hålla NF-κB i schack
För att avslöja hur denna broms fungerar använde författarna proximetsmärkning och protein pull‑down‑metoder för att se vilka molekyler som fysiskt associerar med Nedd4-1(NE). De identifierade nyckelkomponenter i NF‑κB‑vägen, inklusive kinaset IKKβ och NF‑κB‑prekursorproteinet NF‑κB1 (även kallat p105). Uppföljande experiment visade att Nedd4-1(NE) tillsätter ubiquitinmärken på IKKβ, vilket leder till dess nedbrytning. Med mindre IKKβ tillgängligt fosforyleras och degraderas inte dess vanliga mål IκBα lika effektivt. Som ett resultat förblir IκBα mer stabilt och håller den aktiva NF‑κB‑subenheten p50 sequestrerad i cytosolen, vilket förhindrar att den går in i kärnan för att aktivera inflammatoriska gener.
En adapterstyrd överlämning till bromsen
Nedd4-1(NE) agerar också längre ner i kaskaden genom att begränsa nivåerna av NF‑κB1 själv. Här arbetar enzymet inte ensam: det samarbetar med ett annat ubiquitin‑märkningsprotein kallat KPC1. KPC1 hjälper till att bearbeta NF‑κB1‑prekursorn p105 till den aktiva formen p50 och finns i cellulära fack kända som sena endosomer, där även Nedd4-1(NE) lokaliseras. Forskarna visade att Nedd4-1(NE) kan ubiquitinera KPC1 och att denna modifierade KPC1 fungerar som en adapter som rekryterar NF‑κB1 till Nedd4-1(NE) på sena endosomer. Detta trepartscomplex främjar destabilisering av både p105 och p50, vilket återigen minskar mängden NF‑κB som kan nå kärnan.
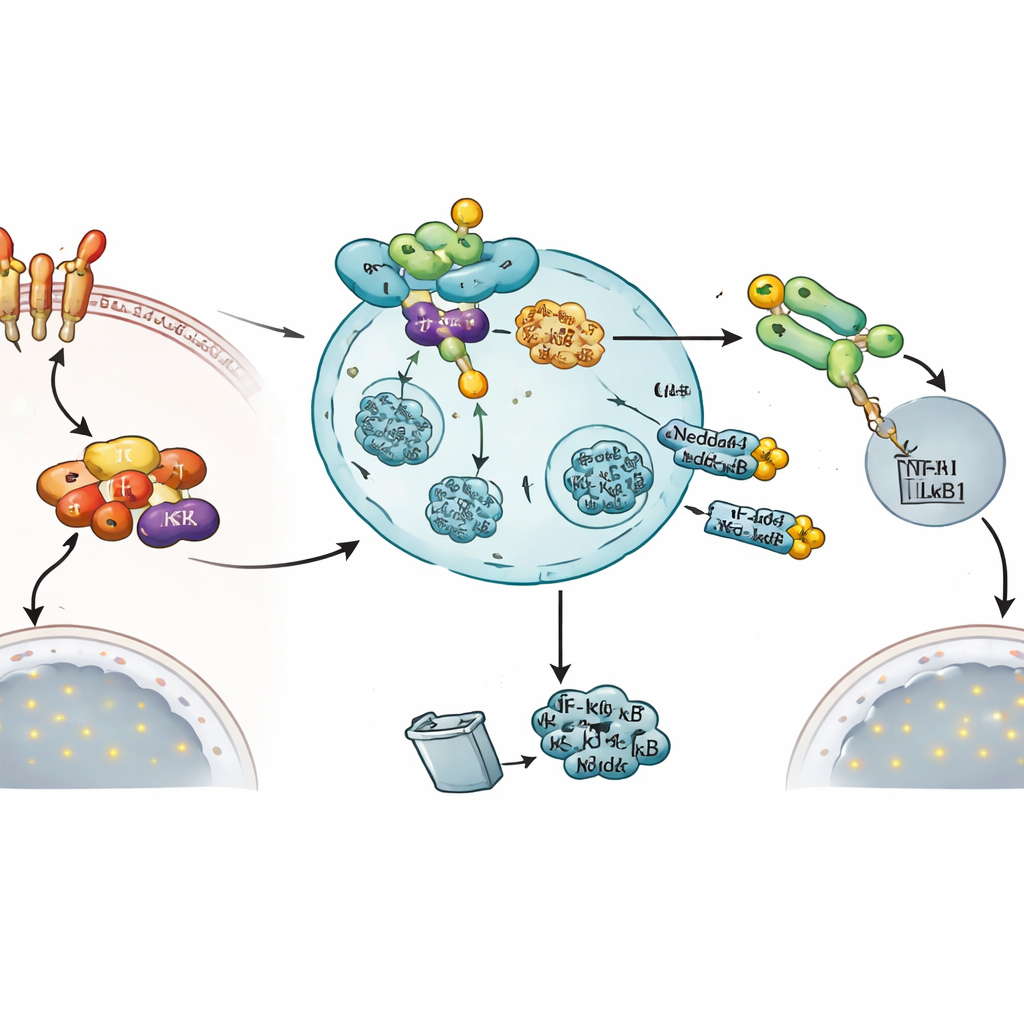
En inbyggd negativ återkopplingsslinga för att avsluta signalen
Slående nog verkar samma signal som aktiverar NF‑κB också inducera denna broms. När celler behandlades med TNFα steg nivåerna av Nedd4-1(NE) budbärar‑RNA dramatiskt, medan standardformen av Nedd4-1 inte förändrades. Funktionella mätningar stödde idén att Nedd4-1(NE) är en avstängningsventil: ökad aktiv Nedd4-1(NE) minskade förflyttningen av NF‑κB1 till kärnan, sänkte aktiviteten hos en NF‑κB‑responsiv rapportergen och minskade uttrycket av en NF‑κB‑reglerad inflammatorisk gen, TNFAIP3. Tillsammans skisserar dessa fynd en negativ återkopplingsslinga där aktivering av NF‑κB‑vägen så småningom ökar Nedd4-1(NE), som sedan riktar in sig på två kritiska noder—IKKβ och NF‑κB1—för att dra ned den inflammatoriska responsen.
Vad detta betyder för hälsa och sjukdom
För en allmän publik är huvudbudskapet att våra celler införlivar en extra, primat‑specifik säkerhetsmekanism för att hindra att inflammatorisk signalering går överstyr. Genom att selektivt märka och beskära kärnkomponenter i NF‑κB‑systemet hjälper Nedd4-1(NE) till att avsluta responsen på TNFα och kan bidra till långsiktig immunbalans. Att förstå denna inbyggda broms kan öppna nya vägar för att behandla sjukdomar där NF‑κB är kroniskt överaktiv, såsom autoimmuna störningar och vissa cancerformer, genom att peka på sätt att efterlikna eller förstärka denna naturliga avstängningsprocess.
Citering: Persaud, A., Kefalas, G., Shteiman, A. et al. Negative regulation of the NF-κB pathway by the ubiquitin ligase Nedd4-1(NE). Commun Biol 9, 374 (2026). https://doi.org/10.1038/s42003-026-09634-7
Nyckelord: NF-kB signalering, inflammation, ubiquitinligas, Nedd4-1(NE), TNF alfa