Clear Sky Science · sv
Notch3 reglerar pericyters fenotypiska plasticitet vid kolorektal cancer
Varför blodkärlen runt tumörer spelar roll
Kolorektal cancer är en av de vanligaste och mest dödliga cancerformerna globalt, men de flesta behandlingar riktar sig direkt mot tumörceller och förbiser ofta det omgivande stödsystem som hjälper tumörer att växa. Denna artikel fokuserar på en mindre känd grupp stödjeceller kallade pericyter, som omsluter små blodkärl. Genom att avslöja hur en signalväg kallad Notch3 ändrar pericyters beteende visar författarna hur tumörens blodförsörjning kan drivas mot antingen läckande, kaotiska kärl som gynnar cancer eller mer normala kärl som kan bromsa sjukdomen och förbättra behandlingar. 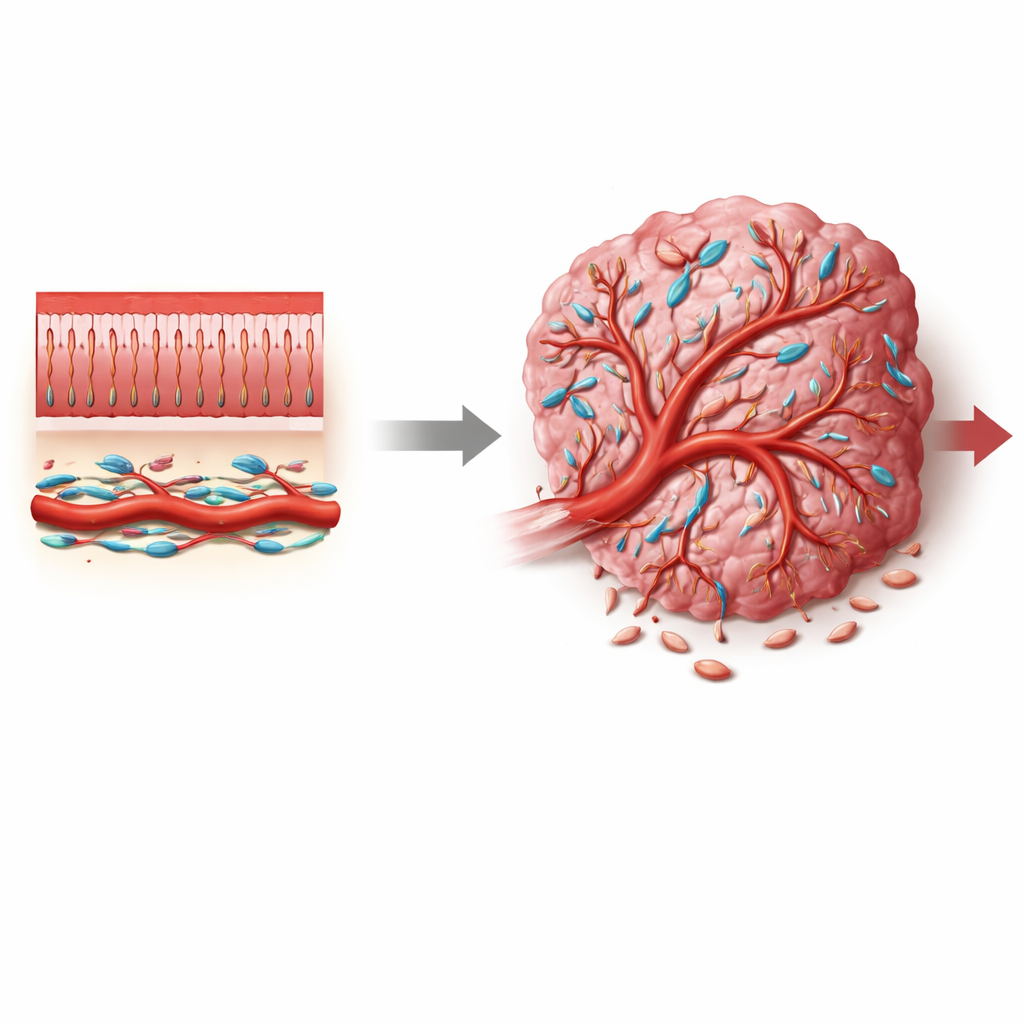
De dolda hjälparna runt tumörkärlen
Blodkärl är mer än bara ihåliga rör. I friska vävnader sitter små kärl tätt omslutna av pericyter—specialiserade celler som stabiliserar kärlväggar, kontrollerar blodflödet och håller läckage i schack. I tumörer ser pericyterna däremot ofta annorlunda ut och beter sig annorlunda: de kan lossna, föröka sig eller ändra identitet, vilket bidrar till den onormala, läckande vaskularitet som är typisk för cancer. I kolorektala tumörer, där mikromiljön är fylld av fibroblaster, immunceller och kärlceller, har det varit oklart var tumörassocierade pericyter kommer ifrån, vilka tillstånd de antar och vilka molekylära signaler som driver dem mot roller som främjar tumören.
Spåra pericyter när tumörer bildas
För att följa pericyter över tid använde forskarna musemodeller för kolitassocierad kolorektal cancer där de genetiskt kunde "märka" specifika celltyper och följa deras öde. De visade att de pericyter som finns i tumörer till stor del härstammar från normala, vävnadsresidenta pericyter som expanderar och prolifererar när cancer utvecklas, snarare än att komma från avlägsna källor som benmärgen. Med avancerad enkelcells-RNA-sekvensering katalogiserade de tiotusentals stromaceller från mus-tumörer och normal tarm och fann att pericyter är signifikant berikade i tumörmikromiljön. De identifierade också liknande pericytexpansion i flera humana dataset för kolorektal cancer, vilket understryker att detta inte bara är ett musfenomen.
En molekylär brytare som förändrar pericyters beteende
Teamet frågade sedan vilka signaler som formar pericyters beteende i tumörer och fann att Notch3—en receptor som gör att celler kan kommunicera med sina grannar—är särskilt aktiv i tumörpericyter. Beräkningsbaserad analys av cell–cell-kommunikation antydde att pericyter både sänder och tar emot Notch-relaterade signaler, särskilt via partner på blodkärlsceller. Genom att konstgjort slå på Notch3 i pericyter såg forskarna att dessa celler prolifererade mer men uttryckte färre kontraktila proteiner som vanligtvis förknippas med kärlstabiliserande funktion. Tumörernas blodkärl hos dessa möss blev större, mer läckande och kantades av fler prolifererande endotelceller, vilket indikerar mindre stabil vaskularitet. Omvänt ledde borttagning av Notch3 till minskad endotelcellproliferation, krympte kärlens storlek och minskade läckaget, vilket tyder på en förskjutning mot mer normaliserade blodkärl utan dramatiska förändringar i tidigt tumörantal eller -storlek. 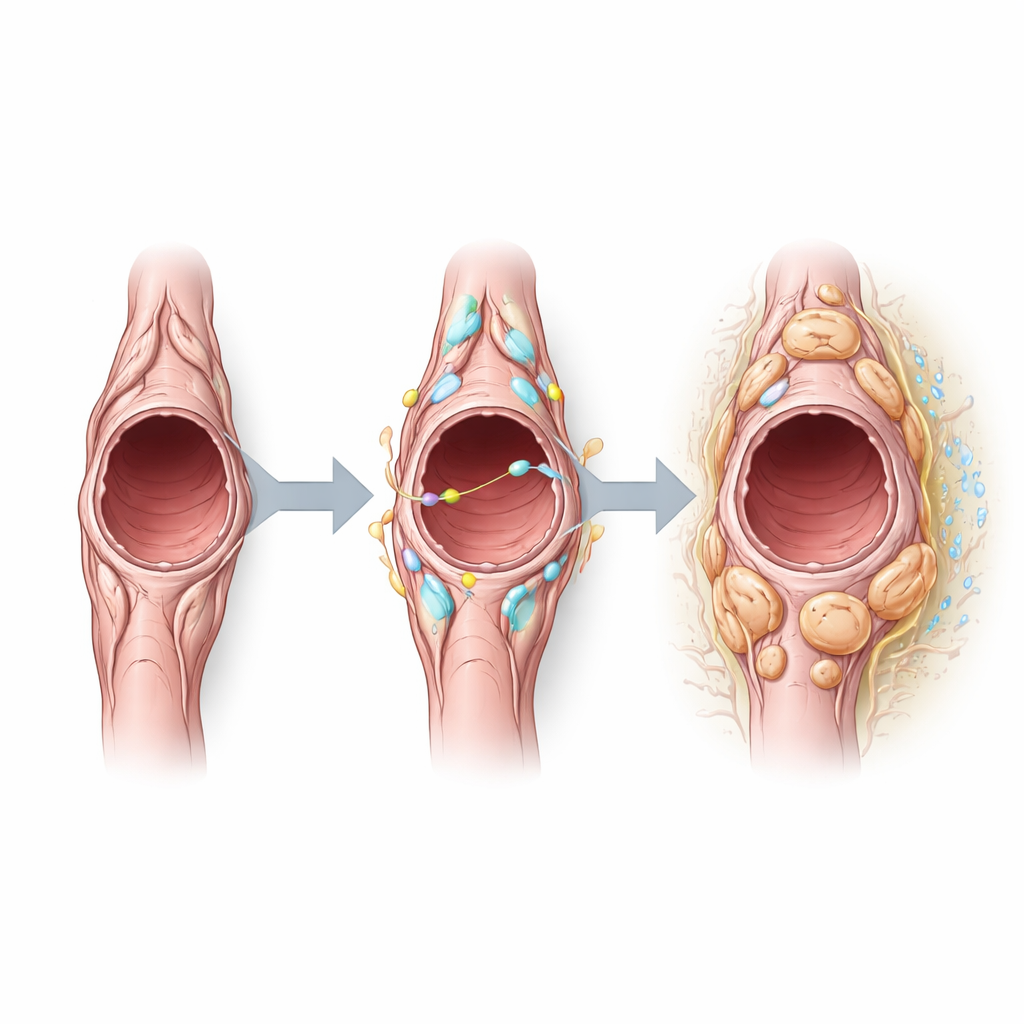
Många ansikten hos pericyter inuti tumörer
Bortom enkla av- och på-förändringar visade studien att tumörpericyter förekommer i flera distinkta tillstånd. Vissa undergrupper visade drag av höggradigt kontraktila celler, andra producerade stora mängder extracellulär matrix, vissa uppvisade inflammatoriska egenskaper och en del bar signaturer som vanligtvis ses i endotelceller. Notch3-aktiviteten var inte jämnt fördelad: den var rikligare i en "syntetisk" eller matrixproducerande pericytpopulation och låg i den mer kontraktila undergruppen. Trajektoriaanalyser föreslog att pericyter kan skifta från ett kontraktilt tillstånd mot ett syntetiskt, proliferativt sådant när Notch3-aktiviteten ökar. När författarna undersökte humana data för kolorektal cancer fann de ett jämförbart spektrum av pericyttillstånd och såg återigen högre aktivitet av en Notch3-målgen i tumörassocierade och prolifererande pericyter, vilket speglar musresultaten.
Göra kärlkaos till en terapeutisk möjlighet
Sammanfattningsvis framställer arbetet Notch3 som en viktig ratt som ställer in pericytidentitet och genom dem strukturen och funktionen hos tumörblodkärl. Hög Notch3-aktivitet driver pericyter mot ett proliferativt, mindre kontraktilt tillstånd kopplat till förstorade, läckande kärl som gynnar tumörprogression. Låg Notch3-aktivitet förknippas med mer kontraktila pericyter, lugnare endotelceller och en mer normaliserad vaskularitet som kan hämma tumörtillväxt och förbättra läkemedelsleverans. Genom att rikta in sig specifikt på Notch3 i pericyter kan framtida terapier styra tumörkärl bort från kaos och mot stabilitet, och därigenom erbjuda en ny vinkel för att behandla avancerad kolorektal cancer i kombination med befintliga läkemedel.
Citering: Chalkidi, N., Stavropoulou, A., Arvaniti, VZ. et al. Notch3 regulates pericyte phenotypic plasticity in colorectal cancer. Commun Biol 9, 343 (2026). https://doi.org/10.1038/s42003-026-09629-4
Nyckelord: kolorektal cancer, tumörmikromiljö, pericyter, Notch3-signalering, tumörblodkärl