Clear Sky Science · sv
Endotelialt TRIM47 reglerar blod‑hjärnbarriärens integritet och kognition via KEAP1/NRF2‑signalvägen hos möss
Varför det är viktigt att skydda hjärnans små kärl
Cerebral small vessel disease är en tyst störningskälla i hjärnan. Den skadar de allra minsta blodkärlen, ökar risken för stroke och urholkar gradvis minne och tänkande, samtidigt som det saknas behandlingar som angriper de underliggande biologiska orsakerna. Denna studie undersöker ett specifikt protein, TRIM47, som finns i cellerna som bekläder hjärnans blodkärl, för att ställa en enkel men avgörande fråga: hjälper det till att bevara blod‑hjärnbarriärens integritet, och spelar det någon roll för kognition?
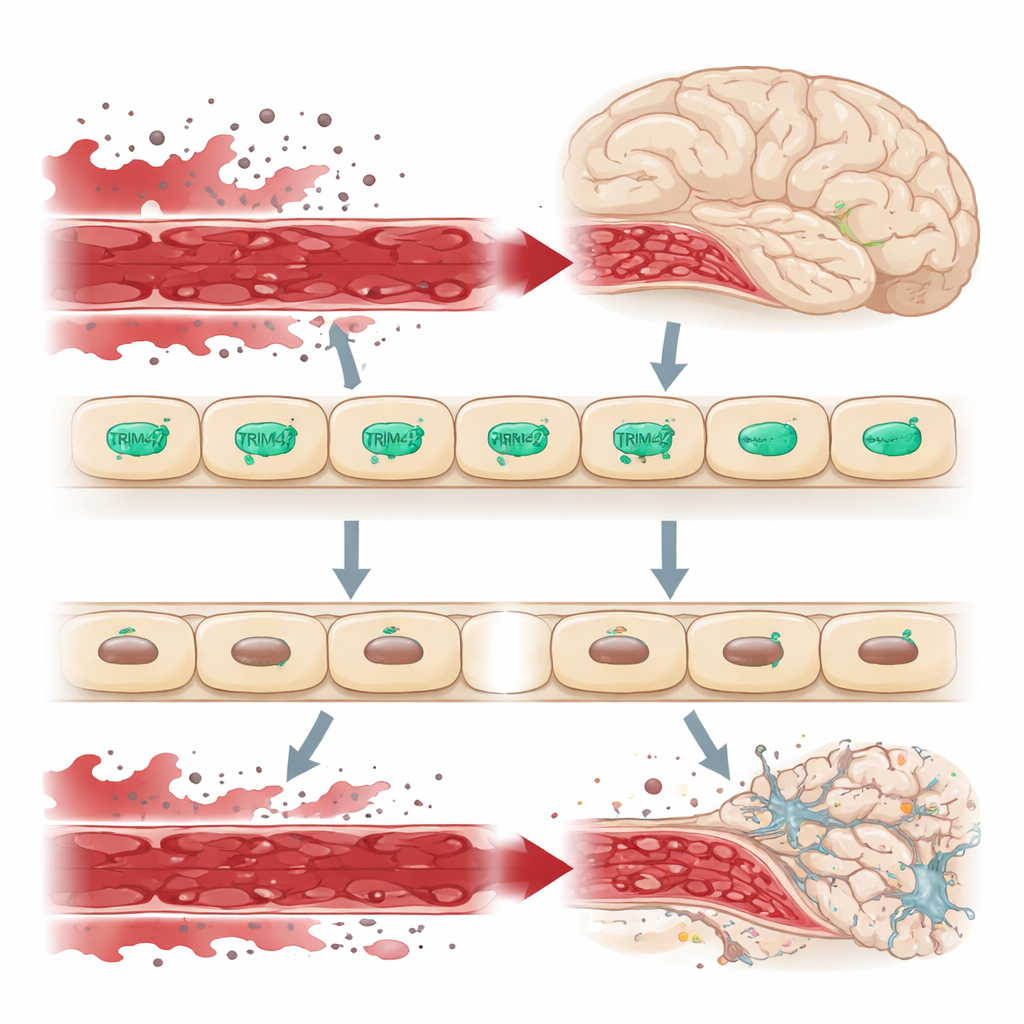
En grindvakt vid hjärnans gräns
Hjärnan skyddas från resten av kroppens cirkulation av blod‑hjärnbarriären, ett tätt slutet lager av endotelceller som strikt kontrollerar vad som får passera in i hjärnvävnaden. När denna barriär läcker, sipprar skadliga molekyler från blodet in i hjärnan, vilket stressar nervceller och stödjeceller och bidrar till tillstånd som demens. Genetiska studier i stora människopopulationer har pekat ut en DNA‑region som innehåller TRIM47‑genen som en riskregion för cerebral small vessel disease. TRIM47 är särskilt aktivt i hjärnans endotelceller, vilket antyder att det kan vara en viktig väktare av denna barriär.
Hur TRIM47 rustar celler mot oxidativ stress
Författarna studerade först humana hjärnendotelceller odlade i laboratoriet och sänkte TRIM47‑nivåerna med RNA‑interferens. Detta utlöste omfattande förändringar i genaktivitet, där det mest påverkade nätverket kretsade kring NRF2, en huvudregulator av cellens antioxidantförsvar. Under normala förhållanden hålls NRF2 i schack av ett annat protein, KEAP1, som riktar det mot nedbrytning. Teamet visade att TRIM47 binder till KEAP1 och hjälper till att förhindra att NRF2 bryts ner. Med TRIM47 närvarande kan NRF2 ackumuleras, förflytta sig till cellkärnan och slå på gener som avgiftar reaktiva syreradikaler. När TRIM47 förloras, sjunker NRF2‑nivåerna, antioxidantgener blir mindre aktiva och endotelceller blir mer sårbara för oxidativ stress.
Från läckande kärl till minnesproblem hos möss
För att se hur denna mekanism ter sig i en levande hjärna konstruerade forskarna möss som saknade Trim47‑genen i hela kroppen, samt en annan stam där Trim47 kunde tas bort endast i endotelceller. Vuxna djur i båda modellerna utvecklade tydliga problem i spatialt lärande och minne och misslyckades i tester som Y‑labyrinten och Morris vattenlabyrinten trots normal rörlighet. Undersökning av deras hjärnor visade att blod‑hjärnbarriären blivit läckande: små fluorescerande spårämnen och blodproteiner läckte från kärl ut i omgivande vävnad. Centrala "tätande" proteiner som bildar täta och adherens‑kontakter mellan endotelcellerna, särskilt Claudin‑5 och Occludin, var minskade. Närliggande astrocyter, de stjärnformade stödjeceller som reagerar snabbt på skada, blev aktiverade, även om det fanns få tecken på utbredd inflammation eller nervcellsförlust i detta skede.
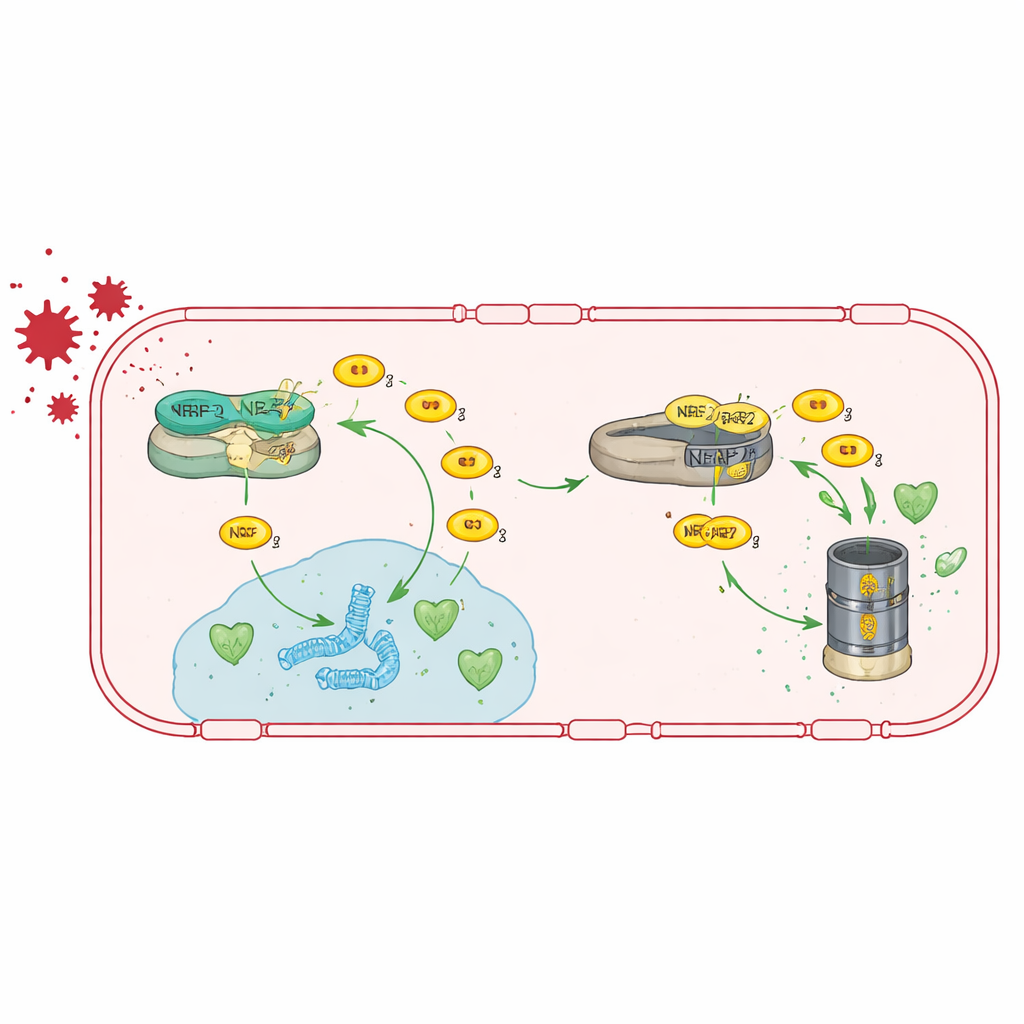
Att slå på antioxidantriktningen igen
Eftersom TRIM47 verkar främst genom att förstärka NRF2‑aktivitet testade teamet om de kunde kringgå dess frånvaro genom att direkt stimulera NRF2. De fodrade Trim47‑deficienta möss med en diet innehållande tert‑butylhydrokinon (tBHQ), en förening känd för att stabilisera NRF2 och slå på dess målgenen. Denna behandling återställde antioxidantgeners aktivitet i hjärnendotelceller, återförde uttrycket av gener för täta junctions mot det normala och minskade läckaget över blod‑hjärnbarriären. Anmärkningsvärt nog normaliserade det också astrocytaktiveringen och räddade djurens prestation i minnestester, vilket tyder på att förstärkning av denna antioxidantväg kan vända både vaskulära och kognitiva problem, åtminstone hos möss.
Ledtrådar från mänskligt blod och nästa steg
För att länka sina musexperiment till mänsklig sjukdom analyserade forskarna proteiner relaterade till NRF2‑vägen i blodprover från tusentals personer som haft hjärn‑MRI. Nivåer av flera NRF2‑reglerade proteiner var kopplade till bilddiagnostiska markörer för small vessel‑sjukdom, såsom förstorade perivaskulära utrymmen och förändringar i vitt substans. Detta stödjer idén att förändrad TRIM47–NRF2‑signalering är relevant hos människor, inte bara i experimentella djur, och att dessa proteiner kan fungera som biomarkörer för sjukdomens svårighetsgrad eller progression.
Vad detta betyder för hjärnhälsan
Sammantaget framträder TRIM47 som en molekylär livvakt som hjälper hjärnans blodkärl att stå emot oxidativ skada genom att stabilisera NRF2‑antioxidantsystemet. När TRIM47 saknas eller är nedsatt försvagas blod‑hjärnbarriären, subtila hjärnskador ackumuleras och minnet börjar svikta. Återaktivering av NRF2‑vägen kan laga barriären och återställa kognitionen hos möss, vilket framhäver denna signalaxel som ett lovande terapeutiskt mål för vaskulära former av demens. Medan tBHQ i sig inte är lämpligt som läkemedel för människor, kan säkrare NRF2‑stimulerande föreningar eller strategier som efterliknar TRIM47:s skyddande roll en dag hjälpa till att bevara hjärnhälsan genom att stärka dess minsta, mest ömtåliga kärl.
Citering: Delobel, V., Grenier, C., Boulestreau, R. et al. Endothelial TRIM47 regulates blood-brain barrier integrity and cognition via the KEAP1/NRF2 signalling pathway in mice. Commun Biol 9, 399 (2026). https://doi.org/10.1038/s42003-026-09628-5
Nyckelord: cerebral small vessel disease, blood–brain barrier, TRIM47, NRF2 pathway, vascular dementia