Clear Sky Science · sv
En inter-subenhetsväg krävs för entropidriven och negativt kooperativ bindning av cykliska nukleotider i HCN2-kanalen
Hur hjärtats lilla pacemakerswitch känner av kemiska signaler
Varje hjärtslag och många hjärtrytmer beror på mikroskopiska kanaler som öppnas och stängs i våra cellmembran. Dessa kanaler, kallade HCN-pacemakerrkanaler, styrs inte bara av elektrisk spänning utan också av små budbärarmolekyler kända som cykliska nukleotider. Denna studie ställer en bedrägligt enkel fråga med långtgående konsekvenser: hur binder dessa små molekyler koordinerat till HCN2-kanalen, och hur kan subtila fel i den processen bidra till sjukdomar som epilepsi?
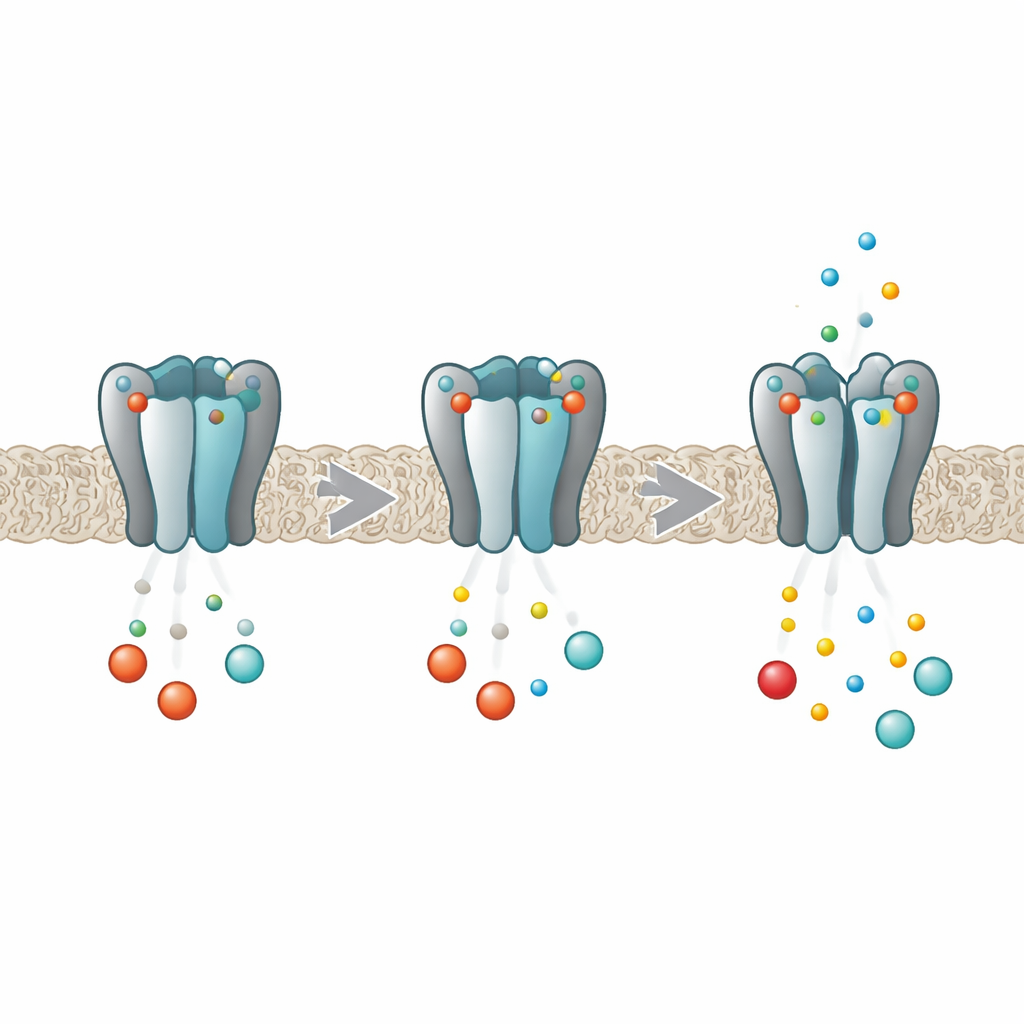
En molekylär dimmer för kroppens rytmer
HCN-kanaler fungerar som dimrar för elektrisk aktivitet i hjärt- och hjärnceller. Varje kanal byggs av fyra identiska proteinenheter som tillsammans bildar en central por genom vilken joner flödar. Djupt inne i varje subenhet finns en ficka som kan fånga cykliska nukleotider som cAMP och cGMP. När dessa budbärare binder gör de det lättare för poren att öppnas, vilket ökar pacemakerströmmen. Tidigare arbete visade att i HCN2-varianten sker bindningen inte oberoende vid varje ficka; istället påverkar de fyra platserna varandra så att den första molekylen binder lättare än de efterföljande, ett beteende känt som negativ kooperativitet. Det nya arbetet syftade till att ta reda på exakt hur de fyra subenheterna "pratar" med varandra under denna process.
Subenheter som känner av sina grannar
Forskarna kombinerade computersimuleringar med laboratoriemätningar på isolerade delar av HCN2-kanalen. Genom långa molekyldynamiksimuleringar iakttog de hur kanalens svansregion—the delen som innehåller fickorna för cykliska nukleotider och den så kallade C-länkaren som kopplar till poren—böjde sig och svajade när olika antal cAMP- eller cGMP-molekyler var bundna. De fann att när en budbärare låste in sig i en subenhet stabiliserade den inte bara den subenheten ensam. Istället förändrade den subtilt stabiliteten hos sina grannar, ibland gjorde dem mer styva, ibland mer flexibla, trots att hela proteinets form knappt ändrades. Dessa grann-till-grann-påverkan berodde på hur många platser som var ockuperade och var de satt runt ringen, i överensstämmelse med vad man kan förvänta sig av negativ kooperativitet.
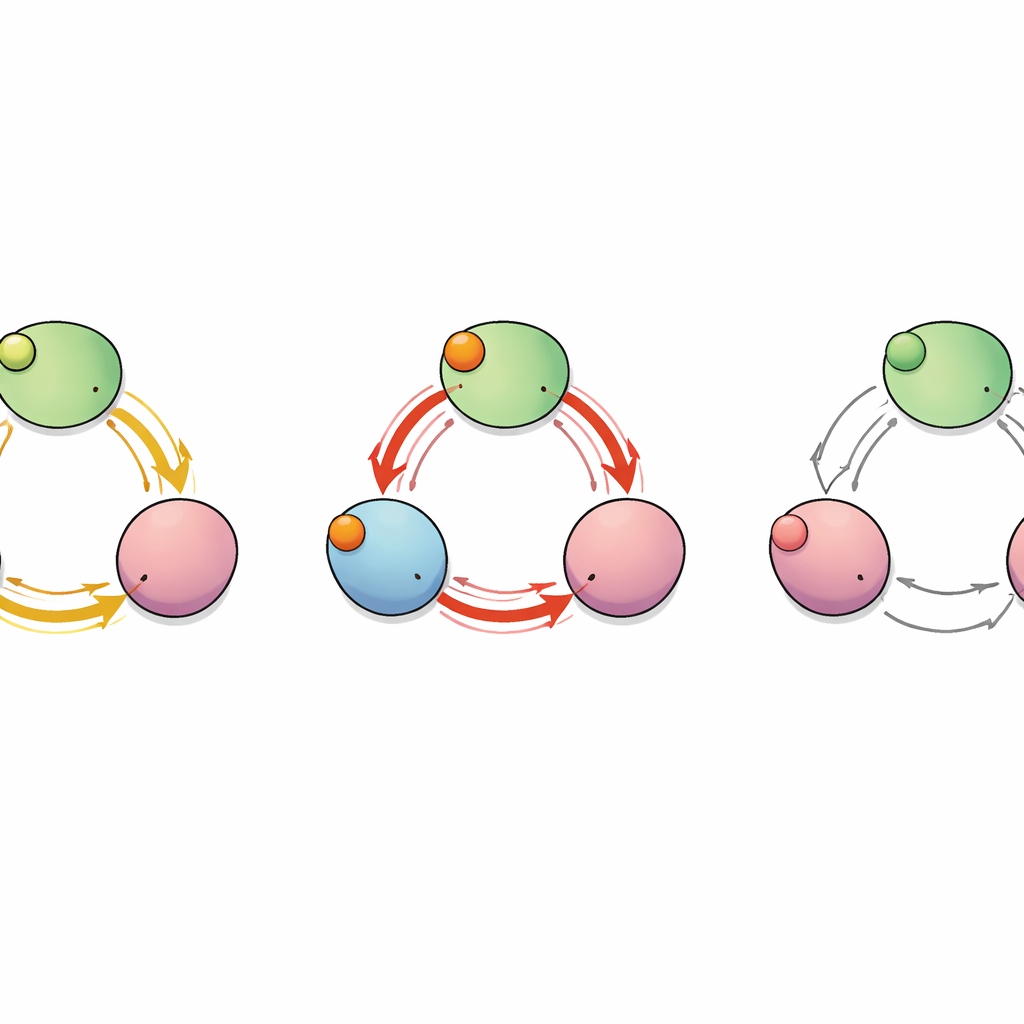
En dold väg mellan subenheter
För att kartlägga hur bindnings"signalen" färdas genom proteinet behandlade teamet kanalen som ett nätverk av interagerande aminosyror. De beräknade vilka rester som rörde sig korrelerat under simuleringarna och använde grafteoretiska verktyg för att identifiera de kortaste och mest effektiva kommunikationsvägarna från bindningsfickorna till C-länkarna som kontrollerar poren. Denna analys avslöjade flera möjliga rutter, men två stack ut: en som håller sig inom en enskild subenhet och en annan som hoppar från en subenhet till dess granne. Längs denna inter-subenhetsrutt fungerade en enskild rest—glutamat vid position 488 (E488)—som en kritisk knutpunkt genom vilken många av de kortaste vägarna passerade, vilket antyder att den kan vara en nyckelrelaypunkt för kooperativ bindning.
Mutationer som bryter samtalet
Författarna gick sedan vidare till experiment med renade kanalsvansar för att testa betydelsen av denna väg. De förändrade E488 och den närliggande tyrosinen 459 (Y459), som ligger på den grannsubenhet dit vägen anländer. Med hjälp av dynamisk ljusspridning bekräftade de att mutantproteinerna fortfarande sattes ihop till fyrsubenhetskomplex, men de visade inte längre den starka ligandinducerade sammandragningen mellan subenheter som sågs i det normala proteinet. Isoterm titrerkalorimetri, som följer de små värmeförändringarna vid bindning, avslöjade en ännu större förändring: vildtyp-HCN2 visade två distinkta bindningsevenemang, ett högaffinitetssteg som i huvudsak drevs av en ökning i entropi (större intern rörelse), följt av tre steg med lägre affinitet. I kontrast visade mutanter vid E488 eller Y459 endast en enda, måttlig-affinitetsbindning som saknade denna gynnsamma entropiboost och förlorade den karakteristiska negativa kooperativiteten.
Varför subtila entropiförändringar spelar roll
När man sätter ihop dessa delar målar studien upp bilden av HCN2-kanalen som en dynamisk ring av fyra subenheter förbundna av specifika "samtalsvägar." När den första cykliska nukleotiden binder, finjusterar den rörelserna i avlägsna delar av ringen via E488 och Y459, vilket gör senare bindningsevenemang mindre gynnsamma och ställer in hur poren svarar. Denna effekt drivs inte av stora strukturella omställningar utan av skift i intern flexibilitet—ändringar i entropi som är osynliga i statiska ögonblicksbilder men avgörande för funktionen. Mutationer som stör de nyckelrester som ligger längs denna inter-subenhetsväg tystar samtalet, avskaffar negativ kooperativitet och kopplas till sjukdomar som idiopatisk generaliserad epilepsi. För en lekmannaläsare är slutsatsen att livsviktiga brytare i hjärta och hjärna förlitar sig på välkoreograferade molekylära "viskningar" mellan proteinsubenheter, och att förstå dessa viskningar hjälper oss att förklara både normala rytmer och vad som händer när de går fel.
Citering: Costa, F., Ng, L.C.T., Chow, S.S. et al. An inter-subunit path is required for entropically-driven and negatively cooperative binding of cyclic nucleotides in the HCN2 channel. Commun Biol 9, 362 (2026). https://doi.org/10.1038/s42003-026-09626-7
Nyckelord: HCN2-jonkanal, bindning av cykliska nukleotider, negativ kooperativitet, allosterisk kommunikation, epilepsimutation