Clear Sky Science · sv
En liten molekyl allosteriskt aktiverar SecA‑beroende sekretion
Att sätta bakteriers lastkaj i övervarv
Bakterier överlever genom att ständigt exportera proteiner genom små portar i sina membraner. Dessa exporter hjälper dem bygga cellväggar, utsöndra toxiner och anpassa sig till stress — processer som ligger i grunden för många infektioner. Denna studie rapporterar en liten kemisk förening, kallad HSI#6, som gör något ovanligt: istället för att blockera exportmaskineriet, växlar den det till ett hyperaktivt, mindre selektivt läge. Att förstå hur denna omkoppling fungerar kan både avslöja nya antibakteriella strategier och ge biotekniken ett sätt att öka proteinsekretion på begäran.
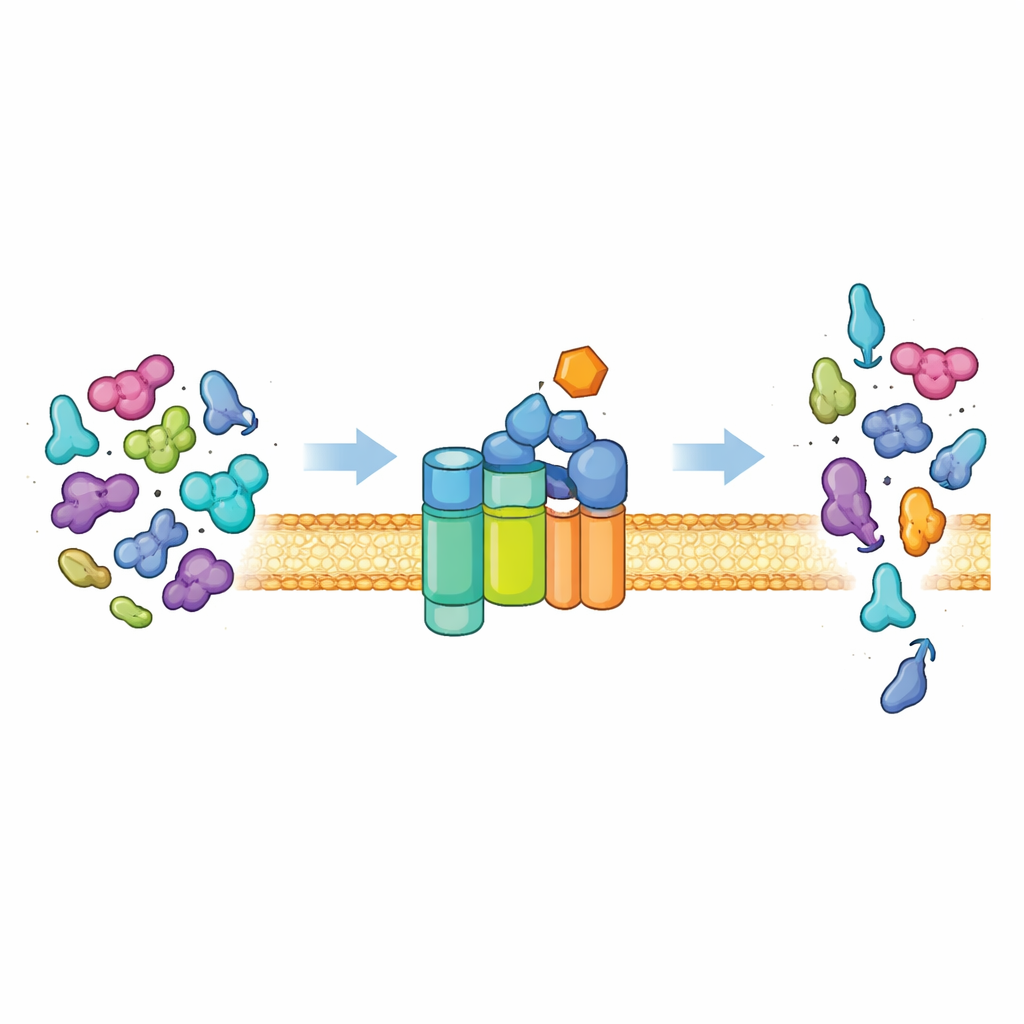
Cellens proteinutgång
De flesta bakterier skickar ut proteiner ur cellen via en universell väg känd som Sec‑systemet. I dess kärna finns en membranchannel (SecYEG) och ett motorprotein (SecA) som förbrukar cellens bränsle (ATP) för att pressa ofolda proteinkedjor genom kanalen. Under normala omständigheter är detta system noggrant. Det exporterar främst ”preproteiner” som bär speciella adressmärken, så kallade signalpeptider, samt ytterligare egenskaper i sin huvudsekvens. Dessa egenskaper behövs för att växla SecA från ett lugnt, lågaktivt tillstånd till en kraftfull motor. Endast proteiner som uppvisar rätt kombination av signaler kan låsa upp full aktivitet, vilket säkerställer att cellen exporterar rätt last och behåller vanliga cytoplasmatiska proteiner säkert inuti.
En liten molekyl som väcker motorn
Forskarna upptäckte HSI#6 i en screening efter föreningar som påverkar bakteriell proteinsekretion och tillväxt. Biokemiska tester visade att HSI#6 binder direkt till SecA med mikromolär styrka och ändrar hur effektivt det använder ATP. I lösning får det SecA att hålla i ATP mer tätt; när SecA sitter vid kanalen förbättrar HSI#6 både ATP‑bindningen och ökar ATP‑omsättningen. Detta mönster är kännetecknet för en allosterisk aktivator: en molekyl som binder vid en plats på ett protein men ändrar aktiviteten vid en annan, avlägsen plats. Till skillnad från naturliga proteinklienter behöver HSI#6 inte fungera som last för att stimulera motorn — den finjusterar helt enkelt SecA:s interna dynamik så att hela translokasen blir katalytiskt förberedd.
Från selektivt filter till promisisk nanomaskin
När HSI#6 har bundit kräver inte längre Sec‑systemet de vanliga exporttaggarna. I provrörsexperiment ökade föreningen ungefär sekretionen av ett standardpreprotein tvåfaldigt och gjorde komplexet mer motståndskraftigt mot natriumazid, en känd SecA‑hämmare. Än mer anmärkningsvärt var att HSI#6 tillät den normala, vildtypiska maskineriet att flytta proteiner som helt saknar signalpeptider, liksom proteiner som normalt befinner sig i cytoplasman. I levande bakterieceller sågs samma effekt med hjälp av rapportörer baserade på alkalisk fosfatas: när cytoplasmatiska proteiner fusionskopplades till ett sekreterat enzym orsakade närvaro av HSI#6 en kraftig ökning av sekretorisk aktivitet utan att mängden producerat protein ändrades. Med andra ord kopplar HSI#6 effektivt bort exporten från de vanliga klientidentifieringskontrollerna och gör Sec‑systemet till en brett verkande exportpump för alla tillräckligt ofolda proteiner.
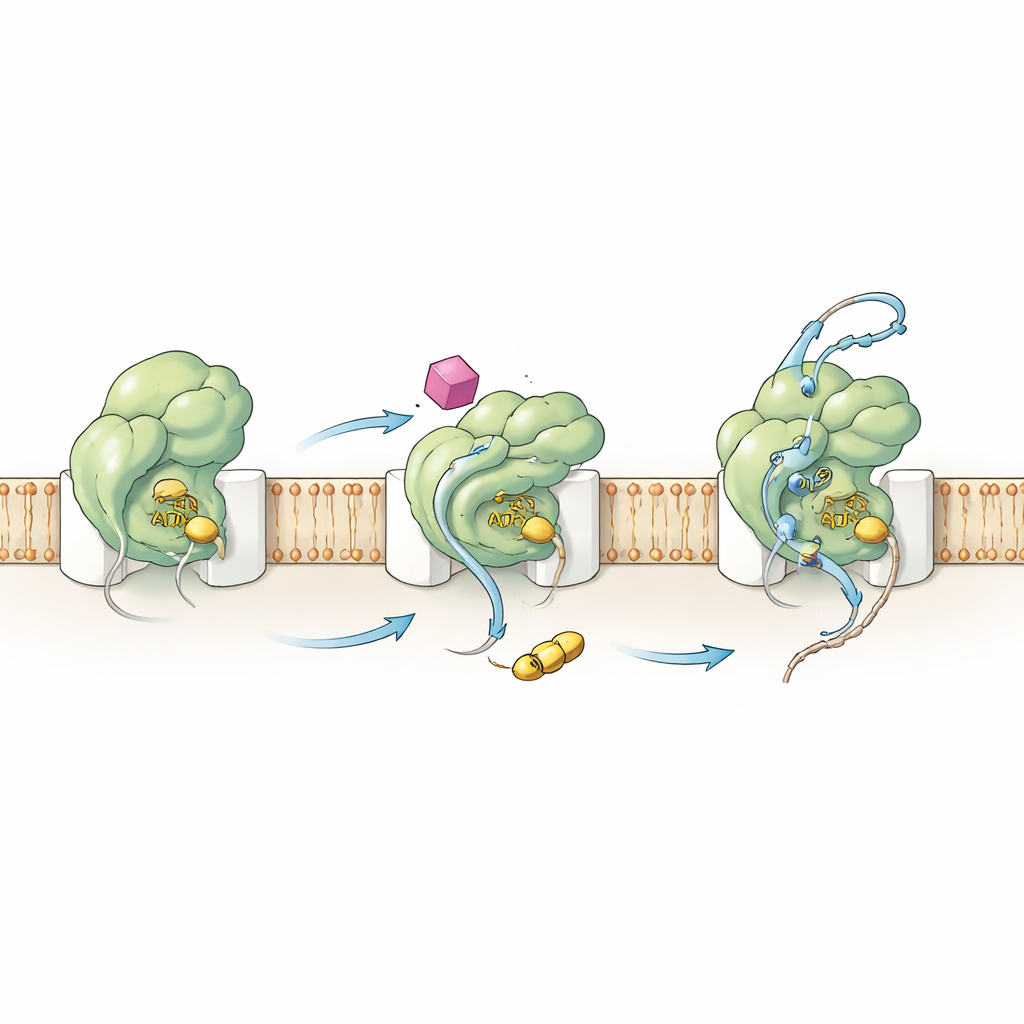
Omskola motorn inifrån
För att förstå hur HSI#6 utlöser detta beteende undersökte teamet både kemin och rörelserna hos SecA. Kinetiska mätningar visade att föreningen förskjuter den viktiga aktiveringssteget uppströms: SecA–kanal‑komplexet blir katalytiskt aktivt redan innan en proteinklient binder. HSI#6 hjälper också SecA att släppa ut använt bränsle (ADP), ett normalt sett långsamt, hastighetsbegränsande steg, och understöder därigenom snabbare ATP‑cykling. Med hjälp av väte‑deuteriumutbytes‑masspektrometri kartlade författarna hur HSI#6 omformar flexibiliteten i olika SecA‑regioner. Föreningen luckrar selektivt upp delar av proteinet som känner av klienter och kopplar till kanalen, samtidigt som den förstyvar en stomme som sannolikt rymmer dess bindningsställe. Det resulterande rörelsemönstret liknar ett redan engagerat, ”på”‑tillstånd för translokasen, vilket tyder på att HSI#6 stabiliserar en aktiverad form — möjligen till och med gynnar en monomerisk SecA bunden till kanalen — utan någon klient närvarande.
Varför detta är viktigt för medicin och bioteknik
Genom att visa att en liten molekyl kan allosteriskt aktivera SecA och avlägsna dess normala klientselektivitet avslöjar detta arbete ett nytt sätt att kontrollera en central bakteriell maskin. För infektionssjukdomar kan sådan tvångsmässig, okontrollerad sekretion försvaga patogener genom att tömma energi och störa deras finjusterade exportprogram, vilket gör HSI#6‑lika aktivatorer till attraktiva utgångspunkter för antibiotikadesign — eller som vägvisare för att skapa framtida hämmare som blockerar samma regulatoriska funktioner. För bioteknik kan samma princip återanvändas för att förbättra sekretionen av nyttiga rekombinanta proteiner, utan behov av konstruerade signalpeptider eller komplexa genetiska ingrepp. I huvudsak visar studien att den bakteriella protein"lastkajen" kan omprogrammeras kemiskt, vilket öppnar nya vägar både för att bekämpa mikrober och använda dem som mikroskopiska fabriker.
Citering: Sedky, H., Hamed, M.B., Krishnamurthy, S. et al. A small molecule allosterically activates SecA dependent secretion. Commun Biol 9, 368 (2026). https://doi.org/10.1038/s42003-026-09623-w
Nyckelord: bakteriell proteinsekretion, SecA‑translokas, allosterisk aktivering, små molekylregulatorer, upptäckt av antibakteriella läkemedel