Clear Sky Science · sv
LncRNA P4HA2-AS1 driver njurmellanfibros via trim32-medierad k63-ubikvitinering av ULK1 och autofiltreringsdysreglering
Varför njäräscarbildning spelar roll
Kronisk njursjukdom drabbar hundratals miljoner människor världen över och framskrider ofta tyst tills dialys eller transplantation är det enda sättet att överleva. I centrum för denna försämring finns en process som kallas ärrbildning, där normal njurvävnad gradvis ersätts av stel, icke-fungerande massa. Denna studie ställer en enkel men avgörande fråga: vilka molekylära omkopplare inne i njurceller driver dem mot denna skadliga ärrbildning, och kan dessa omkopplare vändas tillbaka?
En dold RNA-omkopplare i njurceller
Våra njurar filtrerar blod genom ett invecklat nätverk av små tubuli. När dessa tubuli skadas av blockerat urinflöde, högt blodsocker eller en plötslig minskning av blodtillförseln kan de reagera genom att lägga ned ärrvävnad mellan cellerna. Forskarna undersökte njurarna från möss med flera typer av skada och jämförde dem med friska njurar med hjälp av RNA-sekvensering, en teknik som läser av vilka gener som är aktiva. De upptäckte att en relativt okänd molekyl kallad P4HA2-AS1, ett långt icke-kodande RNA som inte ger upphov till protein, konsekvent var förhöjd i skadade, ärrbildande njurar och i mänskliga njurceller som utsatts för stress i laboratoriet. Detta RNA återfanns främst i cellernas vätskefyllda del, vilket antyder att det kan reglera andra proteiner där. 
Nedreglering av RNA skyddar njuren
För att testa om P4HA2-AS1 bara är en åskådare eller en aktiv drivkraft bakom skadan minskade teamet dess nivåer i möss och i odlade mänskliga njurceller. I en väletablerad musmodell där ena urinledaren knyts för att orsaka långvarigt hinder lindrade sänkning av detta RNA via riktad viral leverans många kännetecken för ärrbildning: tubuli förblev mer intakta, det fanns mindre kollagen och andra ärrproteiner mellan cellerna, och njurfunktionsmarkörer i blodet förbättrades. I odlingar av mänskliga njurceller dämpade minskad P4HA2-AS1 även svaret på en stark ärrbildande signal, TGF-β, vilket ledde till mindre produktion av fibronectin, kollagen och andra profibrotiska faktorer. Dessa experiment visade att detta RNA inte bara är en markör för skada utan aktivt driver ärrbildningsprocessen.
Autofagi: från hushållsarbete till skada
Forskarna frågade sedan hur detta RNA orsakar skada. Deras genuttrycks- och bilddata pekade mot autofagi, cellens inbyggda återvinningssystem som bryter ner utslitna proteiner och organeller. Under normala förhållanden är autofagi en hälsosam städprocess, men när den drivs för hårt under för lång tid kan den pressa skadade njurar mot maladaptiv reparation och ärrbildning. I stressade njurceller ökade P4HA2-AS1 flödet genom autofagin, vilket ledde till en ackumulering av återvinningsvesiklar. När RNA:t blockerades sjönk denna överaktiva återvinning tillbaka mot det normala, både i celler och i njurar från obstruerade möss. Möss som saknade ULK1, ett centralt startenzym för autofagi, var också skyddade från ärrbildning, och i dessa djur kunde inte överuttryck av P4HA2-AS1 förvärra skadan, vilket tydligt kopplar RNA:ets effekter till denna väg.
En molekylär kedja i tre delar
Närmare undersökningar använde biokemiska fisketekniker för att identifiera proteiner som fysiskt binder till P4HA2-AS1. Ett stack ut: TRIM32, ett enzym som märker andra proteiner med små molekylära ”flaggor” kallade ubikvitin. RNAt binder till TRIM32 och skyddar det från nedbrytning, vilket höjer dess nivåer i njurcellerna. Stabiliserat TRIM32 fäster i sin tur en specifik typ av ubikvitinkedja på ULK1. I stället för att skicka ULK1 för destruktion fungerar denna kedja som en förstärkning, och ökar ULK1:s förmåga att starta autofagi. När forskarna antingen tog bort TRIM32 i möss eller tystade det i njurceller minskade både ärrbildning och överdriven autofagi. Återinförande av TRIM32 i celler där P4HA2-AS1 blockerats återställde delvis ärrsvaret, vilket visar att detta enzym är en nyckellänk i kedjan. 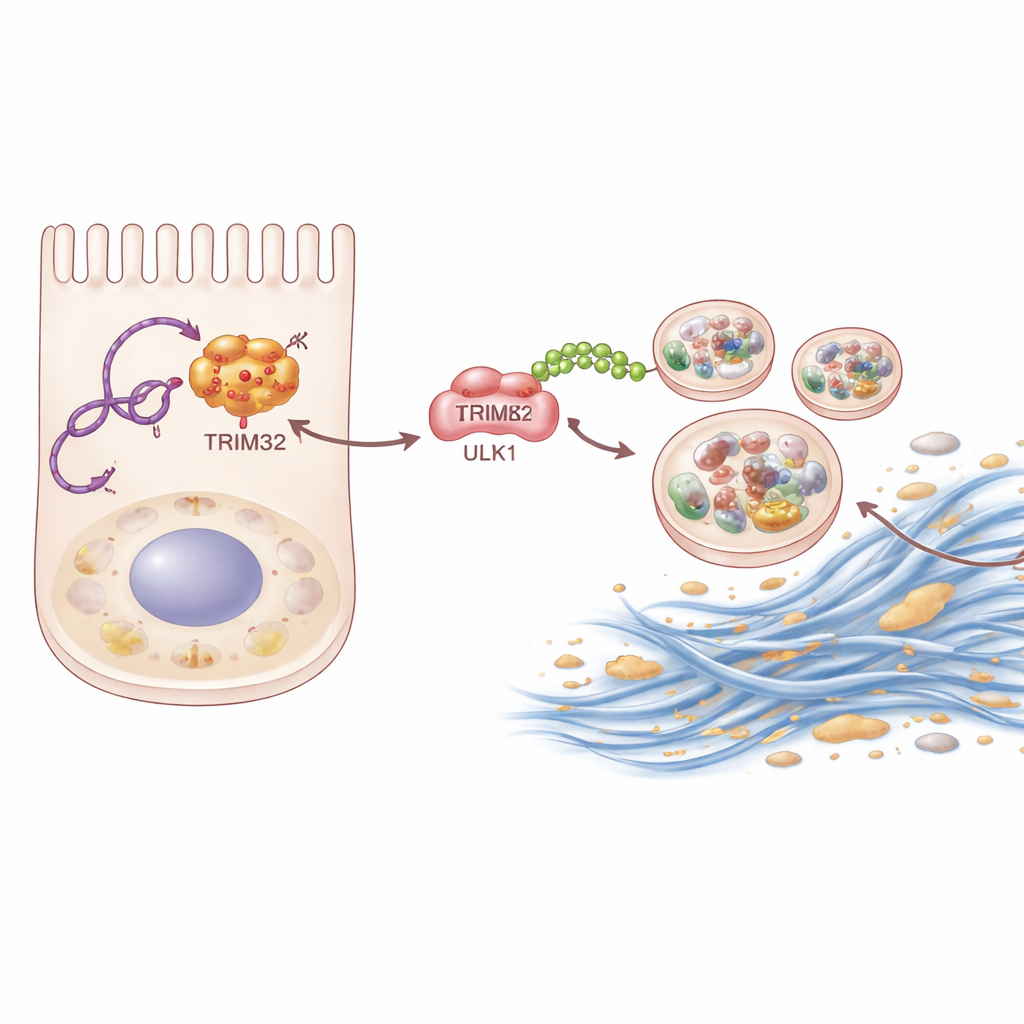
Nya vägar mot mjukare njurar
Tillsammans visar arbetet en tidigare okänd molekylär bana som kopplar långt icke-kodande RNA, proteinmärkning och cellulär återvinning till uppbyggnaden av njurärrvävnad. I skadade njurar stiger P4HA2-AS1, stabiliserar TRIM32, överaktiverar ULK1 och driver autofagin förbi dess nyttiga gräns, vilket i slutändan främjar uppbyggnad av fibrotiska proteiner och förlust av funktion. För icke-specialister är huvudbudskapet att njurärrbildning inte är en oundviklig svart låda: den drivs av identifierbara omkopplare som kan vara möjliga att målinrikta med läkemedel. Att rikta in sig på denna P4HA2-AS1–TRIM32–ULK1-axel — genom att sänka det skadliga RNA:t, dämpa TRIM32 eller finjustera ULK1-aktiviteten — skulle en dag kunna erbjuda nya behandlingar för att bromsa eller förhindra progressionen av kronisk njursjukdom.
Citering: Pan, Z., Xiao, F., Hu, W. et al. LncRNA P4HA2-AS1 drives renal interstitial fibrosis via trim32-mediated k63 ubiquitination of ULK1 and autophagic dysregulation. Commun Biol 9, 339 (2026). https://doi.org/10.1038/s42003-026-09618-7
Nyckelord: kronisk njursjukdom, renal fibros, autofagi, lång icke-kodande RNA, njurtubuli