Clear Sky Science · sv
Hämmare av revers transkriptas möjliggör generering av fertila spermatider från foster-testiklar hos mus in vitro
Att förvandla tidiga könsceller till fungerande spermier
Infertilitetsbehandlingar och grundforskning är beroende av förståelsen för hur omogna könsceller i testikeln omvandlas till spermier. Den här studien visar att det nu är möjligt att få mycket tidiga foster-testiklar från mus, hämtade strax efter att embryots kön har bestämts, att fullfölja denna omvandling helt i en skål. Genom att noggrant justera den kemiska miljön och syrehalten producerade forskarna inte bara mogna spermieliknande celler utan använde dem också för att skapa friska, fertila avkommor.
Varför tidig testikelutveckling är svår att återskapa
Att odla spermier utanför kroppen har tidigare uppnåtts med testikelvävnad från nyfödda eller äldre möss, men effektiviteten var låg och försök med mycket tidigare foster-vävnad misslyckades ofta. I det här unga stadiet håller testikeln fortfarande på att bygga upp sin inre arkitektur, och könsceller genomgår omfattande förändringar i hur deras DNA packas och märks. Att reproducera denna intrikata samordning i en skål är utmanande, och tidigare kulturer gick sällan förbi de tidiga stegen när man började med testiklar insamlade runt embryonal dag 12.5, strax efter att embryots kön är fastställt.
Låna antivirala läkemedel för att skydda utvecklande celler
Teamet fokuserade på ett dolt hinder: mobila DNA-element kallade retrotransposoner, som kan kopiera sig själva och infoga nya kopior på olika platser i genomet. I normala testiklar i kroppen är dessa element noggrant kontrollerade, särskilt i könsceller. I kultur fann författarna däremot att retrotransposonaktiviteten var mycket högre, medan cellernas egna försvarsgener var tystare. Denna obalans korrelerade med dålig spermieutveckling. Eftersom retrotransposoner använder ett revers transkriptas-enzym, liknande vissa virus, testade forskarna flera läkemedel ursprungligen utformade som hämmare av revers transkriptas. En specifik tre-läkemedelsblandning, kallad AEC, fördubblade ungefär andelen spermatogena celler och tredubblade mer än andelen haploida, spermieliknande celler i odlade neonataltestiklar jämfört med obehandlade kontroller.
Från små foster-testiklar till funktionella spermier
Med denna läkemedelscocktail gick forskarna vidare till foster-testiklar. I vävnad tagen strax före födseln ökade inhibitorerna förekomsten av avancerade spermatider. Mer anmärkningsvärt, när de odlade testiklar från embryon vid dag 12.5, ett stadium som aldrig tidigare visat fullföljd spermatogenes in vitro, kunde de nu generera runda och avlånga spermatider. De största vinsterna kom när de kombinerade inhibitorblandningen med en atmosfär med låg syrehalt som bättre efterliknar förhållandena i den utvecklande kroppen. Under dessa hypoxiska förhållanden visade omkring en tredjedel av vävnadsarean markörer för avancerad könscellsutveckling, och spermier med svansar kunde återfinnas i kulturerna.
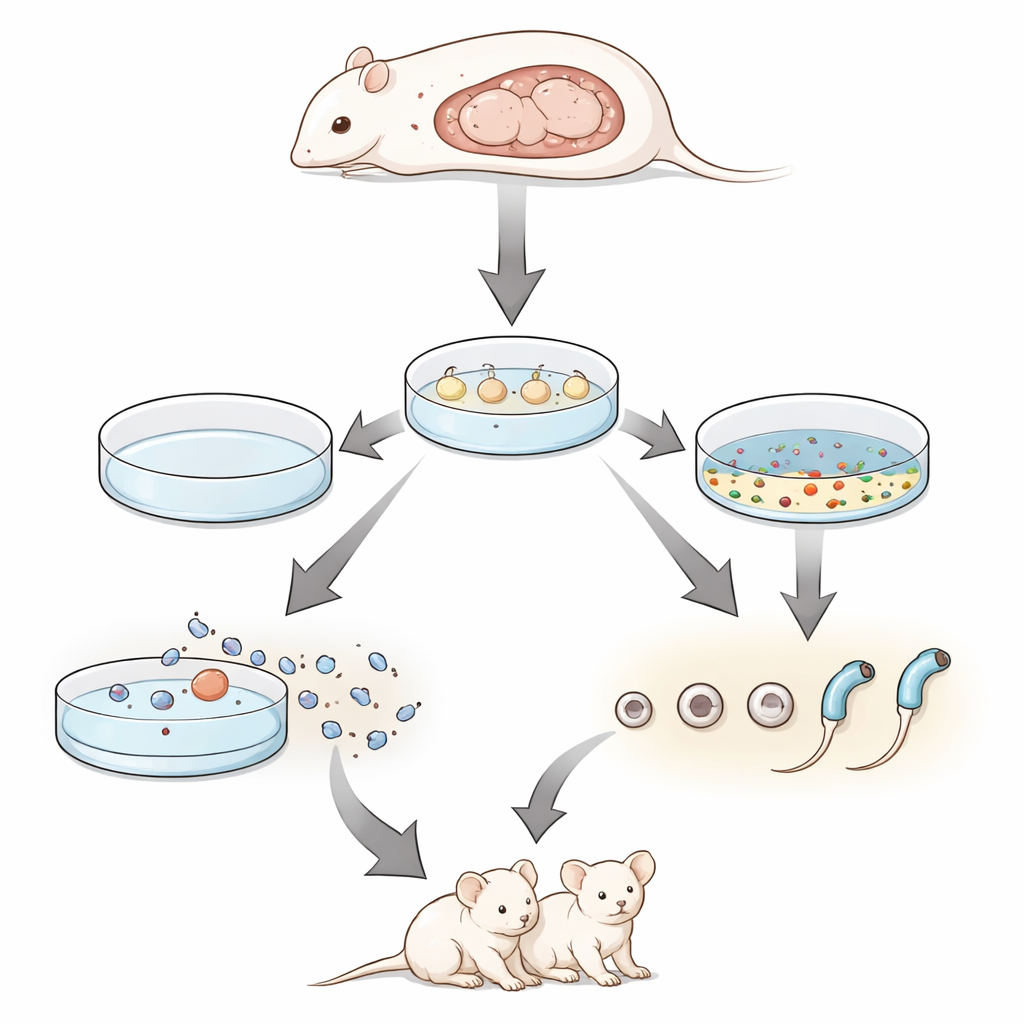
Testa om labbframställda spermatider verkligen fungerar
För att ta reda på om dessa in vitro–framställda celler verkligen var funktionella använde teamet en teknik kallad injektion av runda spermatider. De isolerade runda spermatider från de odlade foster-testiklarna och injicerade dem i musägg som varsamt aktiverats. De resulterande embryona överfördes till fostermöss. Från endast två odlade testikelfragment gav proceduren flera levande ungar, många av vilka bar en fluorescerande markörgen som bekräftade deras odlade ursprung. När dessa första generationens djur tilläts para sig producerade de normalstora kullar av friska andragenerationens avkommor, vilket visar att de laboratorieframställda spermatiderna kunde stödja inte bara utveckling till födsel utan också full fertilitet.
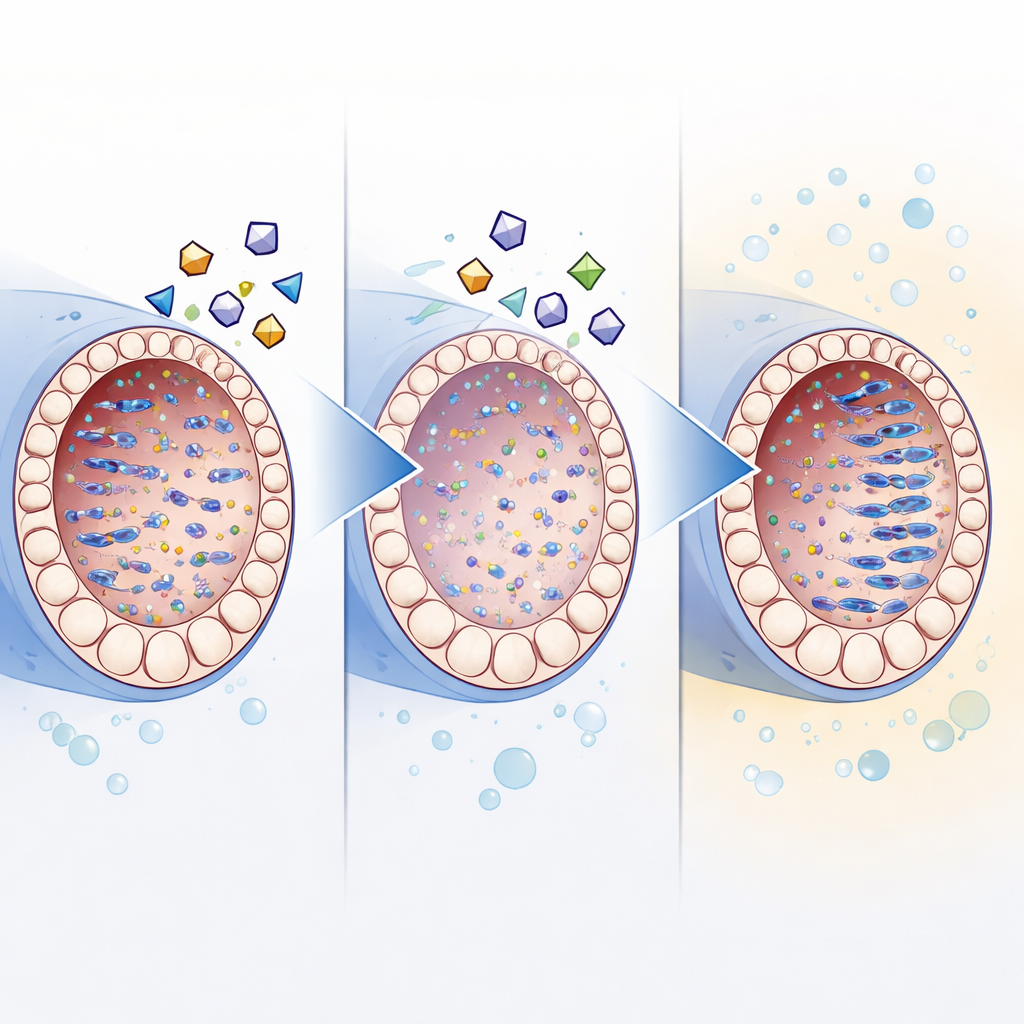
Hur blockering av mobilt DNA kan möjliggöra framtida terapier
Ytterligare experiment stödde idén att hämmare av revers transkriptas främst hjälper genom att hålla mobilt DNA i schack. Jämfört med åldersmatchade testiklar i kroppen visade odlade testiklar högre nivåer av retrotransposonproteiner och extra kopior av deras DNA, tillsammans med minskad uttryckning av cellernas naturliga tystningsmekanismer. Tillsats av inhibitorcocktailen minskade denna ackumulering, samtidigt som mognaden av könsceller förbättrades. Även om läkemedlen något bromsade den övergripande vävnadstillväxten förbättrade försök att kompensera detta med serum-baserade tillsatser inte spermieutfallet, vilket tyder på att tillväxt och korrekt differentiering måste balanseras noggrant.
Vad detta betyder för reproduktionsvetenskapen
Detta arbete visar att även mycket omogna foster-testiklar redan innehåller alla ingredienser som krävs för att bygga en fungerande spermiefabrik, förutsatt att miljön skyddar deras genom och efterliknar viktiga aspekter av livet i livmodern. Genom att kombinera antivirala-liknande läkemedel med låg syrehalt skapade forskarna ett kultursystem som återger full spermatogenes från ett av de tidigaste stadier som hittills testats och ger avkommor som växer upp och förökar sig normalt. Även om studien är i möss och långt ifrån klinisk användning öppnar den ett kraftfullt fönster in i de tidigaste stegen av manlig könscellsutveckling och ger ledtrådar som en dag kan hjälpa till att bevara eller återställa fertilitet hos patienter vars reproduktionsceller skadats tidigt i livet.
Citering: Nishida, M., Ono-Sunagare, Y., Kato, S. et al. Reverse transcriptase inhibitors enable the generation of fertile spermatids from fetal mouse testes in vitro. Commun Biol 9, 329 (2026). https://doi.org/10.1038/s42003-026-09613-y
Nyckelord: in vitro-spermatogenes, foster-testikelkultur, hämmare av revers transkriptas, retrotransposoner, manlig fertilitet