Clear Sky Science · sv
Fetma försämrar spermatogenesen via Leydig‑cellsferroptos inducerad av leverns exosomala miR-122-5p
Varför vikt och fertilitet hänger ihop
Fetma diskuteras oftast i samband med hjärtsjukdom och diabetes, men den kan också tyst underminera manlig fertilitet. Denna studie i möss avslöjar ett överraskande sätt som en fettrik diet kan sänka testosteron och skada spermieproduktionen: levern skickar små ”meddelandebubblor” ut i blodet som utlöser en särskild form av celldöd i testikelns hormonskapande celler. Att förstå denna dolda lever‑till‑testikel‑kommunikation kan hjälpa till att förklara varför överviktiga män ofta brottas med lågt testosteron och infertilitet, samt peka mot nya behandlingsmål.
Gömda meddelanden mellan organ
Våra organ kommunicerar ständigt med varandra via hormoner och andra kemiska budbärare. En form av denna kommunikation använder exosomer—nanometerstora bubblor som släpps ut av celler och bär på fetter, proteiner och genetiskt material. Forskarna började med möss som fick antingen en normal diet eller en fettrik diet som orsakade fetma, insulinresistens och dålig blodsockerreglering. De feta mössen hade mindre, mindre aktiva testiklar: deras spermieantal, testosteronnivåer samt storlek och antal spermieproducerande tubuli var alla reducerade. När teamet undersökte viktiga cellmarkörer i testiklarna fann de färre testosteronproducerande Leydig‑celler och färre tidiga och sena spermieceller, vilket bekräftar att hela spermieproduktionslinjen var nedsatt. 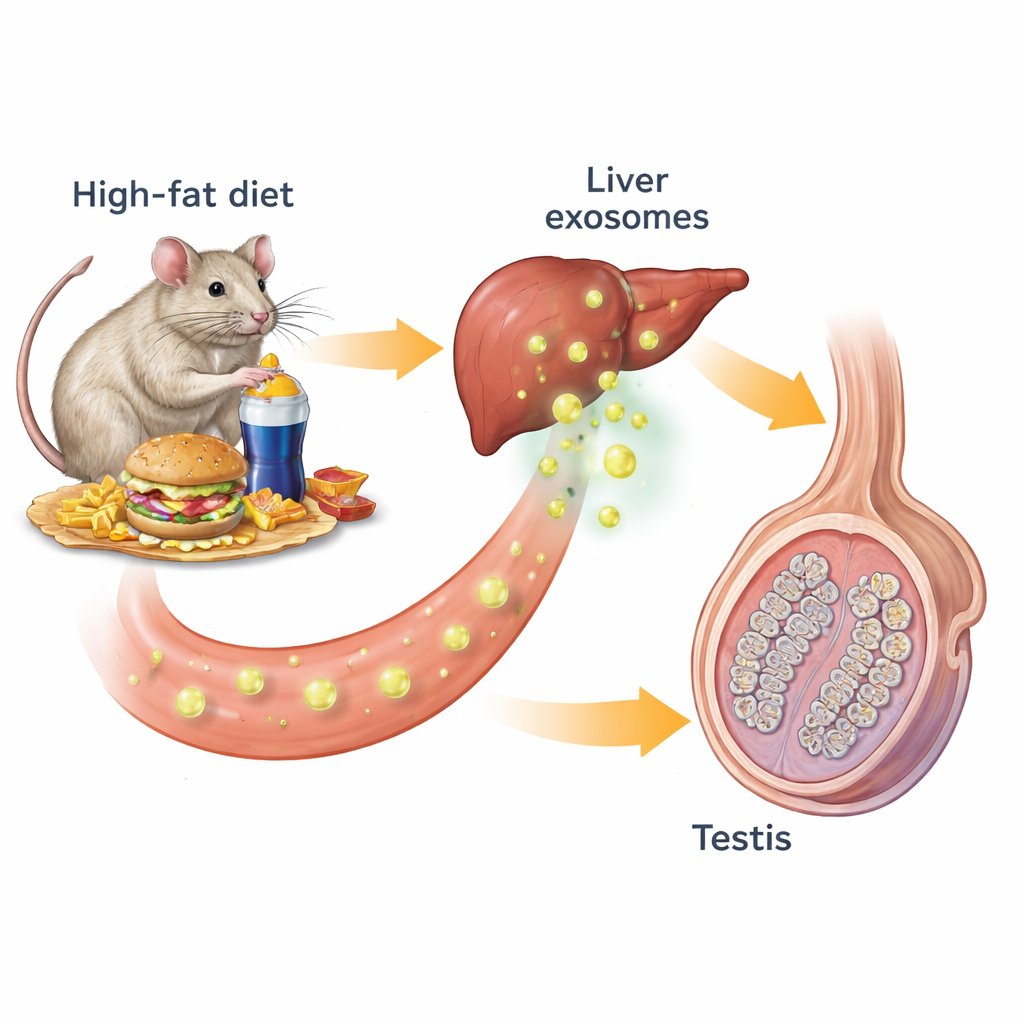
Exosomer sprider skadan
För att testa om cirkulerande exosomer bidrar till denna skada renade forskarna exosomer från blodet hos feta respektive magra möss. Injektion av exosomer från feta möss i friska, magra möss räckte för att reproducera många av problemen: mottagarna utvecklade tecken på metabola störningar, deras testosteronnivåer sjönk och deras spermieantal och testikelstruktur försämrades. Att blockera exosomfrisättning hos feta möss med ett läkemedel kallat GW4869 vände i hög grad dessa förändringar, och återställde spermieantal, testosteron och normal testikelarkitektur. Dessa resultat visar att exosomer i blodomloppet inte bara är åskådare; de bär aktivt skadliga signaler från fetma till reproduktionssystemet.
En toxisk form av celldöd
Teamet undersökte sedan vad exosomerna faktiskt gjorde mot Leydig‑cellerna. De fokuserade på ferroptos, en järn‑driven form av celldöd kännetecknad av järnansamling, oxidativ skada på fetter och skadade mitokondrier—cellens kraftverk. Hos feta möss och hos friska möss som fick exosomer från feta djur visade testiklarna högre nivåer av järn och malondialdehyd, en biprodukt av fettförstörelse, samt tydliga mitokondriella skador under elektronmikroskopet. Behandling av feta möss med en ferroptos‑blockerande förening, Ferrostatin‑1, bevarade Leydig‑celler, ökade testosteron och spermieantal samt förbättrade mitokondriernas hälsa. I cellkultur skyddade samma läkemedel isolerade Leydig‑celler från död och oxidativ stress inducerad av exosomer från feta djur. Tillsammans visar dessa experiment att ferroptos är en nyckellänk mellan fetma och sviktande testosteronproduktion.
Levern skickar budskapet och SCD2‑brytaren
För att spåra budskapet inne i exosomerna sekvenserade forskarna deras små RNA‑last och fann att en särskild mikroRNA, miR‑122‑5p, var starkt förhöjd i exosomer från feta möss. Denna mikroRNA var särskilt riklig i levern och i lever‑härledda exosomer, och dessa leverexosomer kunde spåras till testiklarna. När miR‑122‑5p‑nivåerna experimentellt sänktes i exosomer blev Leydig‑celler mindre benägna att genomgå ferroptos och testosteronproduktionen förbättrades, även om djuren förblev metaboliskt sjuka. Ytterligare tester visade att miR‑122‑5p direkt släcker ett genuttryck av ett gen som kallas Scd2, vilket hjälper till att omvandla vissa fetter till former som skyddar celler från oxidativ skada. Att minska Scd2 i Leydig‑celler gjorde dem mer sårbara för ferroptos och sänkte testosteron, medan att öka Scd2 i feta möss delvis återställde hormonnivåer, spermieproduktion och mitokondriell struktur. 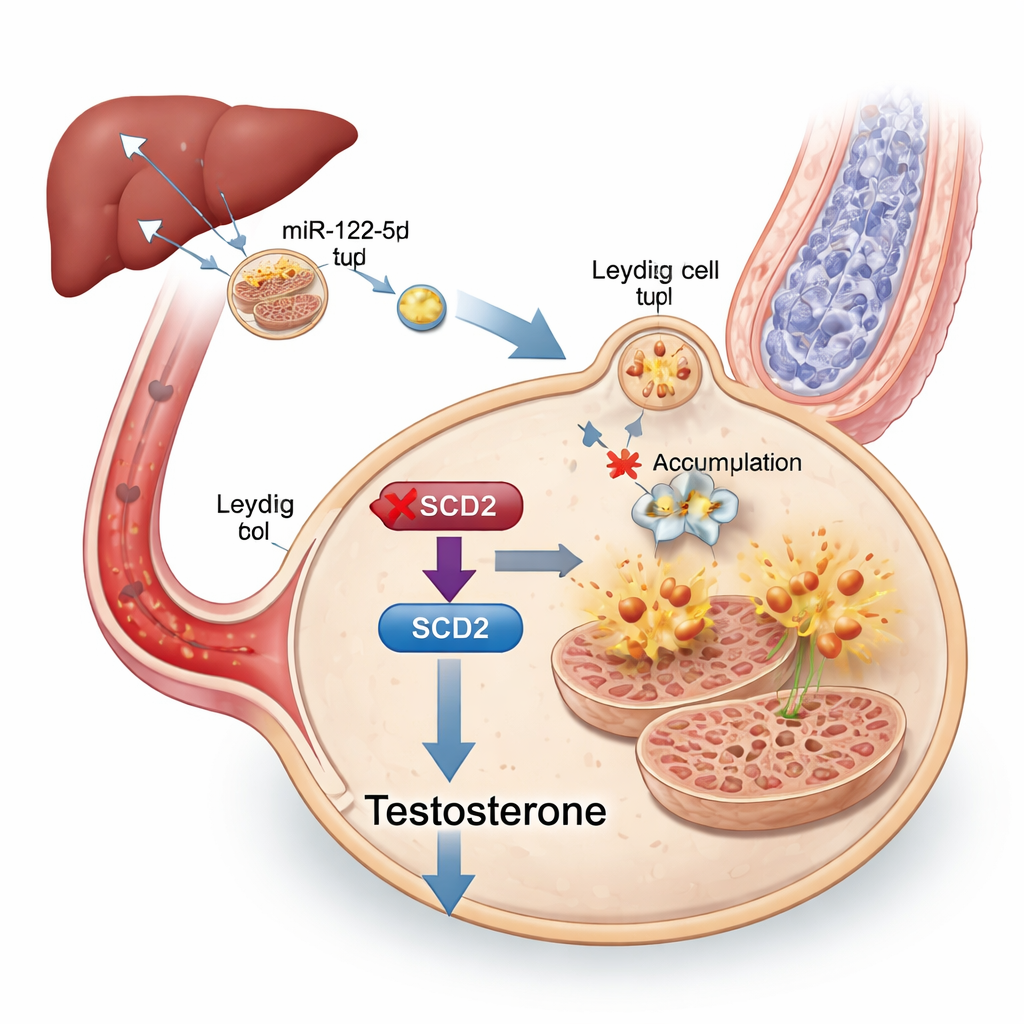
Vad detta betyder för människors hälsa
Enkelt uttryckt visar arbetet att en fettrik diet kan få levern att ladda exosomer med ett överskott av miR‑122‑5p. Dessa exosomer reser via blodet till testiklarna, där mikroRNA:t slår av Scd2‑”fethanterings”‑brytaren i Leydig‑celler. Utan Scd2 samlar dessa celler på sig järn‑driven oxidativ skada, genomgår ferroptos, producerar mindre testosteron och understöder i slutändan färre friska spermier. Även om denna forskning är utförd i möss och fortfarande behöver bekräftas hos människor identifierar den lever‑härledda exosomer, miR‑122‑5p, ferroptos och Scd2 som lovande biomarkörer och potentiella läkemedelsmål för behandling av fetmarelaterad manlig infertilitet—och understryker ytterligare en anledning till att långvariga fettrika dieter tyst kan undergräva reproduktiv hälsa.
Citering: Wang, N., Zhang, B., Chen, T. et al. Obesity impairs spermatogenesis via Leydig cell ferroptosis induced by liver-derived exosomal miR-122-5p. Commun Biol 9, 318 (2026). https://doi.org/10.1038/s42003-026-09612-z
Nyckelord: fetma och manlig fertilitet, testosteron, exosomer, Leydig‑celler, ferroptos