Clear Sky Science · sv
Glykolipidigenkänning och bindning av Siglec-6 hänger på interaktioner med cellmembranet
Hur våra celler skiljer vän från fiende
Immunförsvaret skannar ständigt våra egna celler och avgör när det ska vara lugnt och när det ska slå till. En viktig del av denna övervakning innebär att känna igen sockerstrukturer på cellspridytan. Denna studie visar att en mänsklig immunreceptor, kallad Siglec-6, inte bara använder de där sockren utan även det omgivande cellmembranet för att fatta särskilt precisa beslut om vad den binder. Denna ovanliga strategi kan hjälpa till att förklara hur kroppen finjusterar immunsignaler och kan öppna nya vägar för riktade terapier.
En sockerkännande grindvakt på immunceller
Siglecer är en familj receptorer som sitter på immunceller och känner igen sialinsyra‑innehållande sockerarter, vilket hjälper immunförsvaret att särskilja ”själv” från ”icke‑själv”. De flesta Siglecer förlitar sig på en enda, starkt bevarad byggsten—en argininaminosyra—för att fästa vid dessa sockerarter. Om den argininen tas bort, uteblir vanligtvis bindningen. Siglec-6 är dock en avvikare: tidigare arbete visade att den fortfarande kan binda vissa sockerbärande lipider även när denna nyckelarginin är muterad. Den nya studien syftade till att ta reda på hur Siglec-6 kan avvika från denna til synes gällande regel och vad det innebär för dess roll på mastceller, minnes B‑celler och mänskliga placentaceller.
De speciella lipiderna Siglec-6 söker
På cellsurfäten kan relevanta socker framträda både på proteiner och lipider. Detta arbete fokuserar på en grupp sockerbärande lipider kallade gangliosider, särskilt tre nära besläktade: GM1, GM2 och GM3. Alla tre sticker ut ett enda sialinsyra‑kappt ”huvud” ur membranet. Tidigare experiment visade att Siglec-6 binder starkt till GM1 när det är en del av ett membran, men knappt alls till GM2 eller GM3, trots att deras sockerhuvuden är mycket lika. Med detaljerade datorbaserade simuleringar av realistiska membran bekräftade författarna att sialinsyran i GM1 och GM3 är lika exponerad och tillgänglig. Med andra ord är enkel fysisk åtkomst inte vad som ger GM1 dess speciella status. Istället framträdde en ytterligare sockerenhet i spetsen av GM1—den terminala galaktosen—som en avgörande komponent som hjälper till att positionera Siglec-6 korrekt mot membranet.
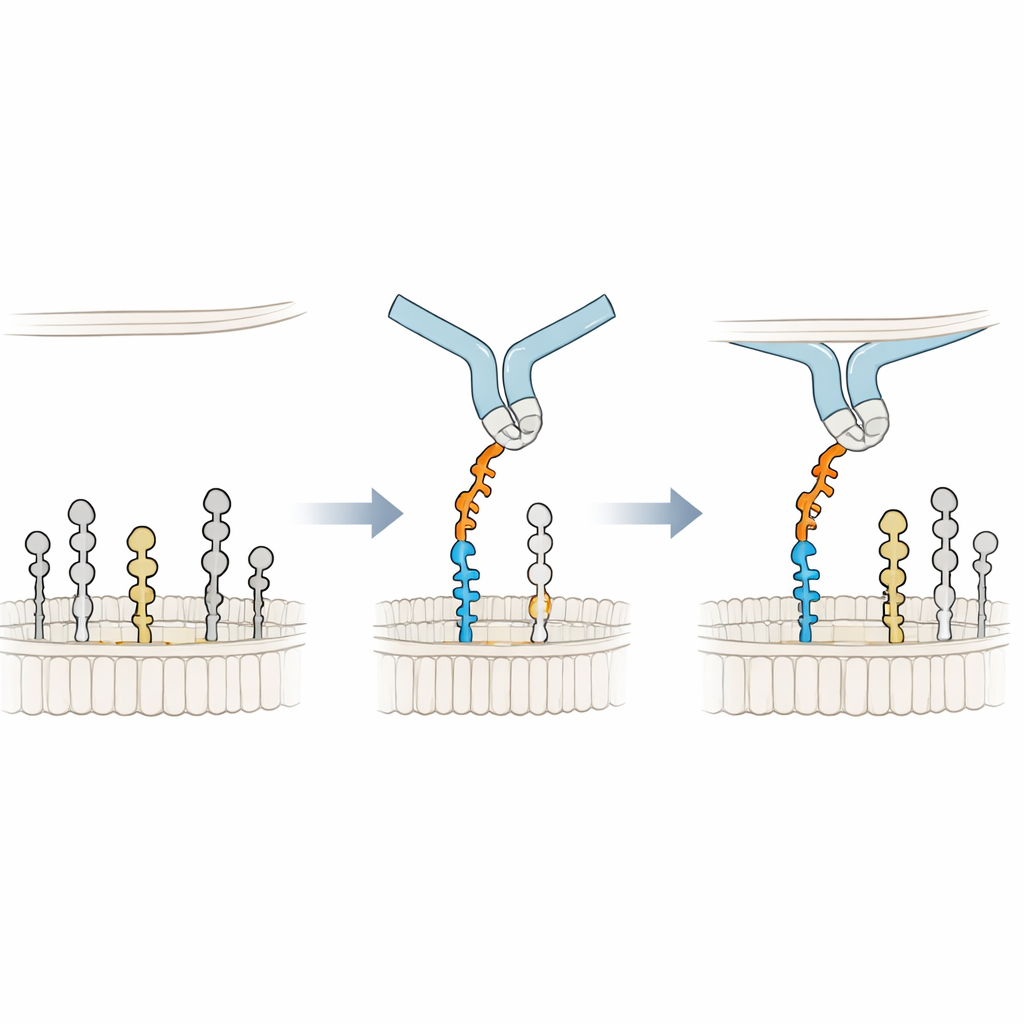
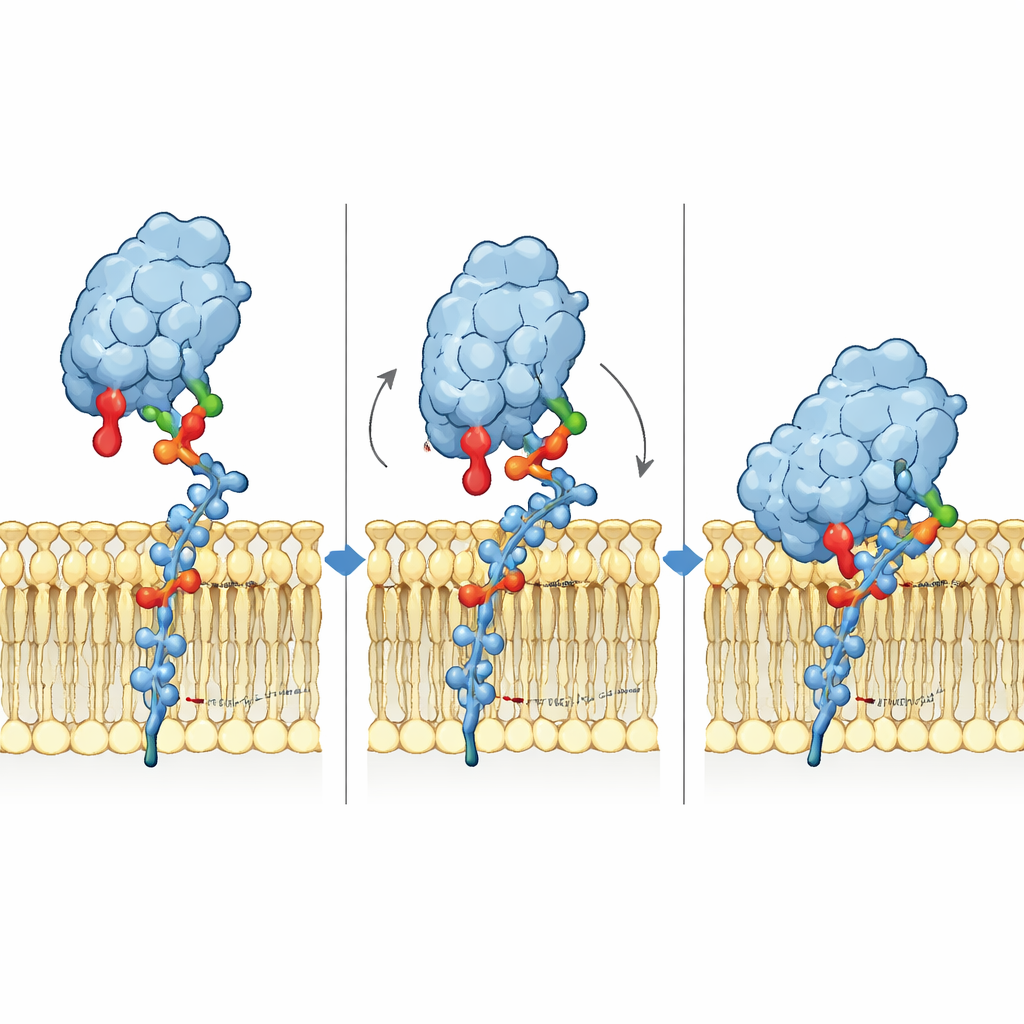
Lutar sig mot membranet för bättre grepp
För att förstå bindningsmekanismen på atomär nivå byggde forskarna tredimensionella modeller av Siglec-6 som engagerar GM1 i ett membran och körde långa molekylärdynamiksimuleringar. De fann att Siglec-6 fortfarande använder sin kanoniska arginin (Arg122) för att kontakta sialinsyran, men den kontakten fladdrar av och på över tid. Det som håller komplexet stabilt är något nytt: en närliggande tryptofan (Trp127) tränger in i membranets fettdel, medan en intilliggande lysin (Lys126) interagerar med de laddade huvudgrupperna hos omkringliggande lipider. Denna ”kil” i membranet kompletterar den vanliga socker–arginin‑interaktionen och lånar effektivt bindningsenergi från lipidmiljön. När den terminala galaktosen i GM1 tas bort för att efterlikna GM2, svänger en flexibel slinga i Siglec-6 in i det lediga utrymmet, drar receptorn bort från membranet och stör detta membranstödda grepp, vilket förklarar förlusten av stabil bindning.
Experiment som prövar mekanismen
Teamet testade sedan dessa datorbaserade insikter i levande celler och biokemiska assay. De konstruerade celler för att uttrycka normal eller muterad Siglec-6 och mätte hur väl dessa celler band till fluorescerande liposomer och små lipid‑diskar som bar GM1. Att mutera den kanoniska argininen minskade bindningen endast måttligt när GM1 satt i ett membran, vilket bekräftar att Siglec-6 inte ensam är beroende av denna rest i det sammanhanget. Däremot abolierade mutationen av Trp127 i stort sett bindningen till GM1‑innehållande liposomer, och att mutera både Trp127 och Lys126 raderade nästan all bindning. Samma mutanter band dock normalt till GM1‑lika sockerarter presenterade utanför ett membran, vilket visar att Siglec-6:s grundläggande struktur var intakt. Native masspektrometri visade vidare att Siglec-6 kan binda inte bara GM1 utan också vanliga fosfolipider, och att denna lipidinteraktion försvinner när Trp127 tas bort. Anmärkningsvärt nog fäster Siglec-6 till och med till ”nakna” liposomer som saknar GM1, återigen på ett Trp127‑beroende sätt, vilket tyder på att den först kan pröva membranet och sedan låsa sig när den stöter på GM1.
Fria sockerarter berättar en annan historia
När samma tre gangliosider testades som fritt flytande sockerfragment snarare än som del av ett membran, uppträdde Siglec-6 mer likt sina släktingar. I lösning band den GM1, GM2 och GM3 med likartat svag affinitet, och nu var den kanoniska argininen avgörande: mutation av Arg122 minskade bindningen kraftigt, medan mutation av Trp127 hade liten effekt. Denna kontrast visar att Siglec-6 effektivt växlar mekanism beroende på om den möter socker i ett membran eller i fri form. I membran förlitar den sig på ett samverkande partnerskap mellan sockerhuvudet, den terminala galaktosen i GM1 och direkt membrankontakt; i lösning återgår den till den klassiska arginincentrerade igenkänningsmotiv.
Varför detta är viktigt för immunreglering
Tillsammans visar studien att Siglec-6 är en fint avvägd sensor som använder membranets fysiska kontext för att skärpa sin specificitet. Genom att delvis förankra sig i omgivande lipider kan den selektivt känna igen GM1 bland mycket lika gangliosider, och därigenom omvandla en allmän ”sialinsyraläsare” till en högprecisionsdetektor av ett särskilt ytmönster. Denna membranstärkta strategi verkar vara unik bland hittills studerade Siglecer och kan hjälpa Siglec-6 att skanna cellsurfätor efter specifika glykolipid‑signaturer som reglerar immunsvar eller markerar särskilda vävnader, såsom mänsklig placenta. Att förstå detta dubbla igenkänningsläge kan underlätta utformningen av terapier och diagnostiska verktyg som utnyttjar Siglec-6:s ovanliga kombination av socker‑ och membransinne.
Citering: D’Andrea, S., Schmidt, E.N., Bui, D. et al. Glycolipid recognition and binding by Siglec-6 hinges on interactions with the cell membrane. Commun Biol 9, 333 (2026). https://doi.org/10.1038/s42003-026-09609-8
Nyckelord: Siglec-6, gangliosider, cellmembran, glykolipidigenkänning, immunreglering