Clear Sky Science · sv
Hämning av ATM förbättrar knock-in-effektiviteten genom att undertrycka AAV‑inducerad aktivering av apoptotiska vägar
Göra genredigering mer effektiv
CRISPR‑genredigering lovar behandlingar för genetiska sjukdomar, mer robusta grödor och kraftfulla forskningsverktyg. Men ett av dess mest värdefulla knep — att exakt infoga ny DNA på en bestämd plats i genomet, kallat “knock‑in” — fungerar fortfarande ineffektivt. Denna studie undersöker varför vissa celler accepterar ny DNA lättare än andra och visar ett sätt att få celler att utföra precisa ändringar oftare, särskilt vid användning av adenoassocierat virus (AAV), ett ledande fordon för genterapi.
Observera DNA‑reparation i realtid
För att förstå vad som hjälper eller hindrar exakt geninsertion byggde forskarna ett intrikat “instrumentpanel” inuti mus‑embryonala stamceller. Detta tredubbla rapportörsystem använder tre fluorescerande markörer för att i samma celler följa om CRISPR har klyvt DNA, om en precis knock‑in har inträffat, och om cellen istället har fogat in donator‑DNA med en grövre reparationsmetod. Genom att läsa av olika färgkombinationer med flödescytometri kunde de skilja rena, templatsbygga ändringar från felbenägna insättningar och oredigerade celler. Denna sida‑vid‑sida‑övervakning gjorde det möjligt att kartlägga hur olika DNA‑reparationsvägar bidrar till varje utfall med mycket högre upplösning än äldre PCR‑baserade tester.
Två DNA‑hjälpare, två mycket olika svar
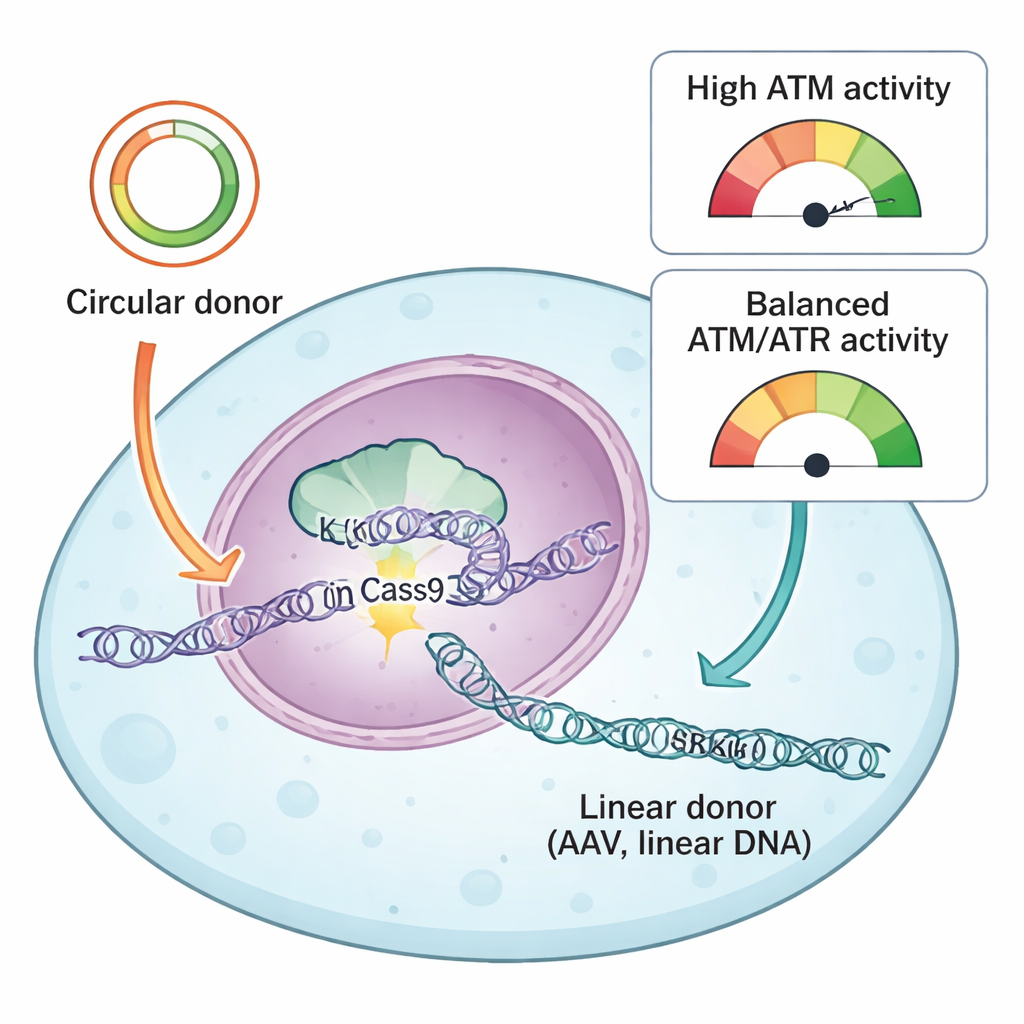
Teamet jämförde två vanliga typer av donator‑DNA som används för att styra CRISPR‑reparationer: cirkulära plasmider och linjära AAV‑härledda DNA. Båda bär matchande “homologiarmar” som talar om för cellen var den ska infoga den nya sekvensen, men de kommer in i cellen i olika fysiska former. Cirkulära plasmider är slutna slingor av dubbelsträngat DNA, medan AAV‑donatorer typiskt anländer som enkla linjära molekyler. Med sitt rapportörsystem och ett bibliotek av läkemedel som riktar sig mot DNA‑skaderesponsproteiner fann författarna att ett nyckelprotein, ATR, var konsekvent nödvändigt för framgångsrika knock‑ins med båda donortyperna. Hämning av ATR reducerade kraftigt den precisa insättningen, medan en mild förstärkning av ATR‑aktivitet via en KEAP1–NRF2‑väg gjorde knock‑ins mer effektiva, särskilt med AAV‑donatorer.
När DNA‑skydd slår tillbaka
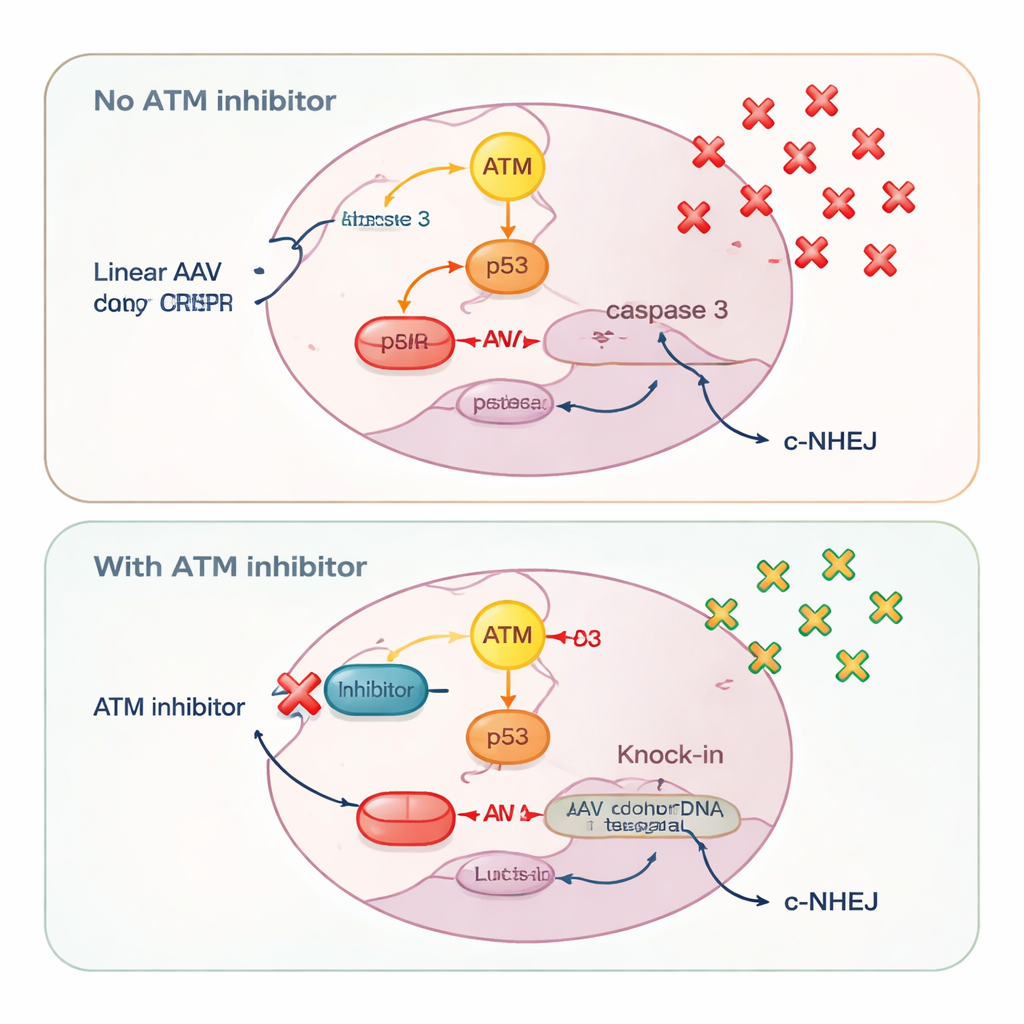
En annan DNA‑skadesensor, ATM, visade sig bete sig på ett slående donorberoende sätt. Med cirkulära plasmiddonatorer minskade blockad av ATM både precis knock‑in och änd‑till‑änd‑sättet för insättningar, vilket stämmer med dess klassiska roll i att hjälpa celler reparera dubbelsträngsbrott. Men med linjärt DNA — oavsett om det kom från AAV, självkompletterande AAV eller plasmider klippta till raka bitar — gjorde ATM‑hämning det motsatta: den ökade knock‑in‑effektiviteten. Forskarna spårade denna effekt till hur celler tolkar inbrytningar av linjärt DNA. Höga doser AAV aktiverade starkt ATM, som i sin tur slog på p53 och kaspas 3, centrala spelare i programmerad celldöd. Celler som tagit upp många kopior av donator‑DNA, och därför hade störst chans till en framgångsrik knock‑in, var också de mest benägna att dödas av detta larmsystem.
Spara de bäst rustade cellerna
Genom att tillsätta ATM‑hämmare tystade forskarna ATM–p53–kaspas 3‑dödsvägen. Detta skonsade celler som bar stora mängder donator‑DNA, vilket gjorde att fler av dem överlevde tillräckligt länge för att fullfölja en precis knock‑in. Mätningar av virala genomkopior bekräftade att ATM‑hämning ökade antalet AAV‑molekyler som behölls inne i cellerna. Samtidigt dämpade ATM‑blockad något en snabb, blunt reparationsväg kallad klassisk icke‑homolog änd‑till‑änd‑ligering, vilket visades genom reducerad aktivering av DNA‑PK, ett centralt enzym i den vägen. Att försvaga detta konkurrerande reparationsalternativ puttade fler CRISPR‑klipp mot homologi‑baserad knock‑in snarare än snabba lagningar som ignorerar donator‑templaten.
Vad detta betyder för framtida genterapier
För icke‑specialister är budskapet att samma cellskydd som skyddar oss från DNA‑skador oavsiktligt kan sabotera precis genredigering, särskilt när stora mängder viralt donator‑DNA används. Detta arbete visar att en försiktig fininställning av dessa skydd — att hålla ATR aktiv men tillfälligt dämpa ATM när linjära donatorer som AAV är närvarande — kan göra CRISPR‑knock‑ins mer tillförlitliga och effektiva. En sådan strategi skulle kunna förbättra genterapier, celleteknik och sjukdomsmodeller genom att hjälpa fler celler acceptera den avsedda förändringen samtidigt som onödig cellförlust undviks.
Citering: Natsagdorj, ME., Hara, H., Uosaki, H. et al. ATM Inhibition Enhances Knock-in Efficiency by Suppressing AAV-Induced Activation of Apoptotic Pathways. Commun Biol 9, 177 (2026). https://doi.org/10.1038/s42003-026-09604-z
Nyckelord: CRISPR knock-in, AAV genredigering, DNA‑skaderespons, ATM‑hämning, genomteknik