Clear Sky Science · sv
Karaktärisering av nanobodys utvecklingsbarhet för bättre terapeutisk design med Therapeutic Nanobody Profiler
Varför de små antikroppskusinerna är viktiga för framtidens läkemedel
Många av dagens blockbustermediciner är antikroppar — proteiner som fäster vid sjukdomsmål med stor precision. En nyare klass av ännu mindre bindare, kallade nanobodies, kan glida in i svåråtkomliga fickor på virus, tumörer och andra molekyler. Men förmågan att binda ett mål räcker inte: en läkemedelskandidat måste också vara enkel att framställa, stabil i en flaska och säker i kroppen. Denna artikel presenterar Therapeutic Nanobody Profiler, ett beräkningsverktyg utformat för att hjälpa forskare att tidigt och enbart från sekvens avgöra vilka nanobodies som mest sannolikt kan bli praktiska läkemedel.
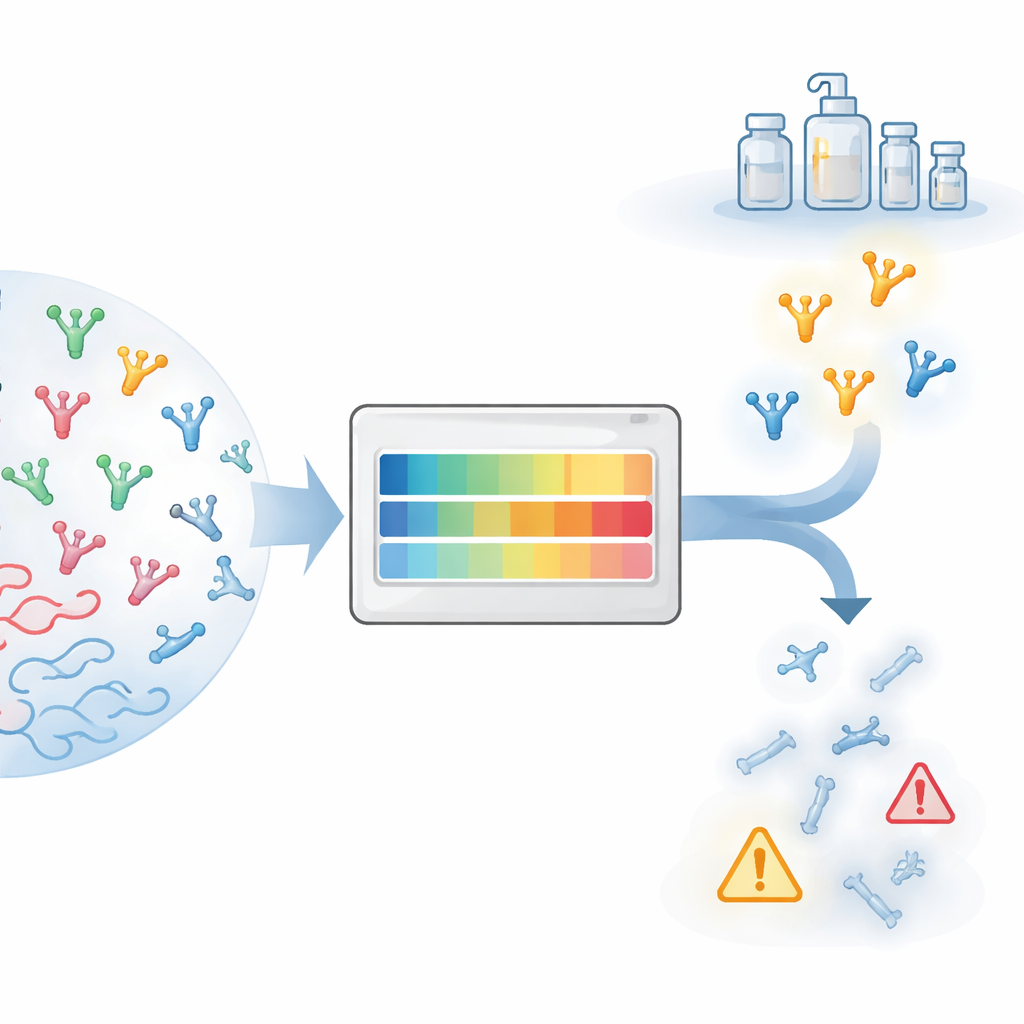
Från lovande idé till praktiskt läkemedel
Att omvandla ett protein till en verklig terapi innebär en rad praktiska hinder som samlas under begreppet ”developability” (utvecklingsbarhet). Proteiner måste kunna produceras i stora mängder, förbli lösliga, undvika att klumpa ihop sig och vara stabila under transport och förvaring. Under det senaste decenniet har forskare lärt sig förutsäga många av dessa egenskaper för fullstora monoklonala antikroppar, stödda av rikliga kliniska data och specialiserade labbtester. Nanobodies är dock strukturellt annorlunda: de består av en enda domän i stället för ett par kedjor, har ofta längre binderloopar och exponerar ytområden som är begravda i konventionella antikroppar. Som en följd kan metoder anpassade till vanliga antikroppar ge missvisande svar när de används på nanobodies.
En profilerare byggd för nanobody‑egenskaper
För att möta denna mismatch utformade författarna Therapeutic Nanobody Profiler (TNP), inspirerad av ett tidigare verktyg för standardantikroppar men ombyggt kring nanobodybiologi. De samlade nanobodysekvenser från många källor: kliniska prövningar, naturliga immunrepertoarer, patent, vetenskapliga artiklar och kända kristallstrukturer. Med hjälp av djupinlärningsbaserade strukturprediktorer anpassade för enkeldomänsantikroppar genererade de tredimensionella modeller för dessa sekvenser. Från varje modell mätte de hur långa binderlooparna är, hur långt en nyckelloop sticker ut från proteinets kropp och hur kluster av hydrofoba och laddade rester är ordnade på ytan — egenskaper som starkt påverkar löslighet, aggregering och icke‑specifikt fastnande.
Två strukturella varianter, båda gångbara
En av de mest iögonfallande resultaten rör huvudbindarloopen, känd som CDR3. När teamet kvantifierade hur ”kompakt” denna loop är — genom att jämföra dess längd med hur långt den sträcker sig från proteinet — fann de en tydlig uppdelning i två strukturella stilar. I den ena undergruppen är loopen längre och viker tillbaka över proteinets sida och bildar många stabiliserande kontakter med en uppsättning karakteristiska rester. I den andra sticker loopen mer utåt, liknande ett konventionellt antikroppsfragment. Nanobodies i klinisk fas förekommer i båda undergrupperna, och när forskarna jämförde dussintals praktiska labbmässiga mätningar — såsom aggregering, självassociation och termisk stabilitet — såg de ingen systematisk nackdel för någon av stilarna. Det innebär att läkemedelsdesigners inte behöver favorisera en övergripande loopform framför den andra, så länge andra egenskaper ser acceptabla ut.
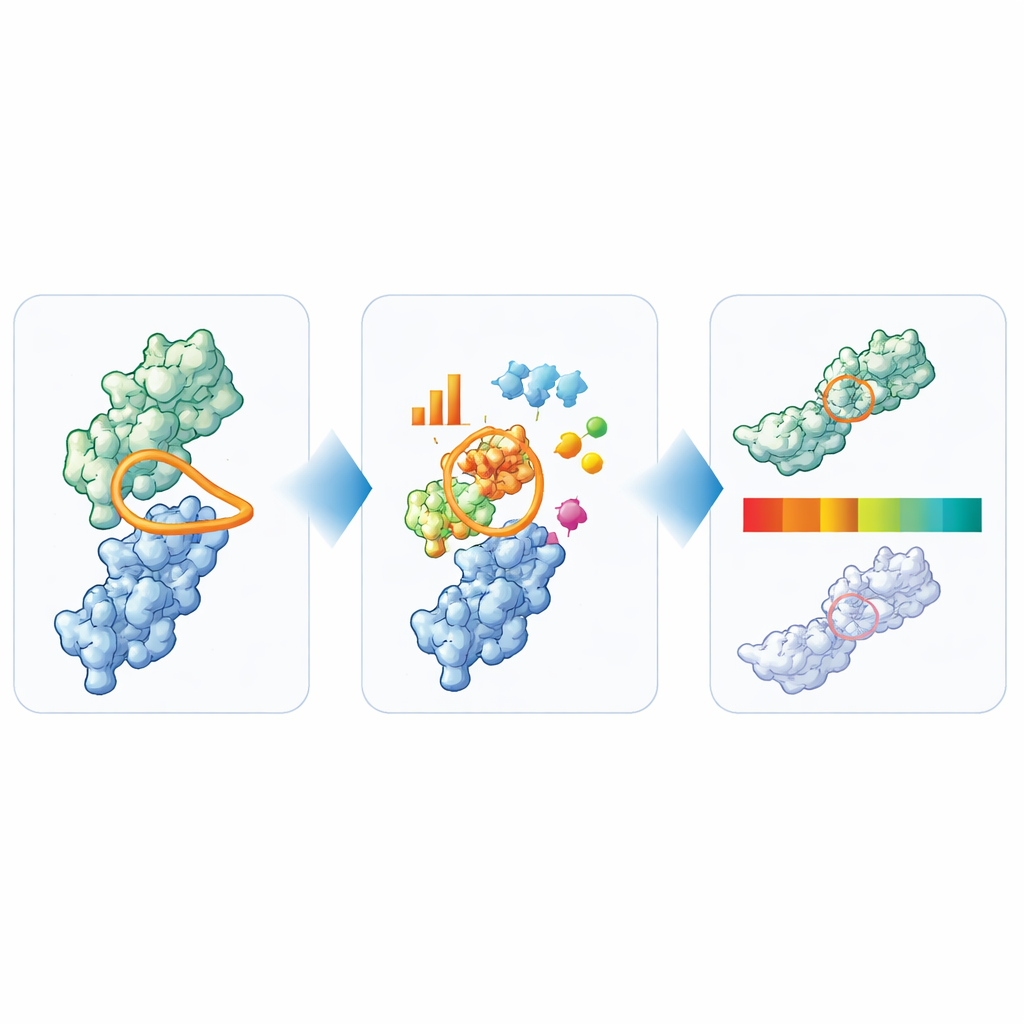
Att göra struktur till enkla trafikljus
Utifrån sin breda analys destillerade författarna sex nyckelfunktioner som tillsammans fångar huvudfrågorna kring nanobodys utvecklingsbarhet: total loop‑längd, den specifika längden och kompaktheten hos CDR3 samt storleken på hydrofoba, positivt laddade och negativt laddade ytplåster runt bindningsstället. De använde sedan de 36 nanobodies som nått klinisk testning för att sätta praktiska gränser för varje mått. Värden i den centrala, vältrafikerade regionen märks ”grönt”, gränsfall ”gult” och tydliga avvikare ”rött”. För att pröva hur informativa dessa signaler är tillämpade de TNP på ytterligare 72 proprietära nanobodies och jämförde flaggorna med ett omfattande panel av labbtester. Nanobodies som TNP markerade som tydliga avvikare visade sig ofta också ha flera experimentella varningssignaler, medan de som såg rena ut beräkningsmässigt oftare uppförde sig väl i labbet.
Vad detta betyder för morgondagens behandlingar
För icke‑specialister är huvudbudskapet att formen och ytmönstret hos en nanobody nu kan omvandlas till en enkel utvecklingsbarhetsprofil innan kostsamma labbarbeten inleds. Therapeutic Nanobody Profiler ersätter inte experiment, och avvikelser mellan förutsägelser och tester förekommer fortfarande, särskilt eftersom labbtester gjordes på nanobodies som var fästa vid större antikroppsfragment. Men genom att snabbt flagga kandidater med ovanligt långa eller tätt vikta loopar eller med problematiska ytplåster hjälper TNP att rikta uppmärksamheten mot nanobodies som är mer benägna att bli pålitliga läkemedel. Allteftersom fler nanobodies går in i kliniska prövningar och referensuppsättningen växer bör detta verktyg bli ännu mer träffsäkert, vilket påskyndar designen av små, robusta antikroppsliknande läkemedel för ett brett spektrum av sjukdomar.
Citering: Gordon, G.L., Gervasio, J., Souders, C. et al. Characterising nanobody developability to improve therapeutic design using the Therapeutic Nanobody Profiler. Commun Biol 9, 344 (2026). https://doi.org/10.1038/s42003-026-09594-y
Nyckelord: nanobodies, utvecklingsbarhet för biologiska läkemedel, beräkningsprofilering, antikroppsingenjörskonst, proteinstabilitet