Clear Sky Science · sv
DTX1-medierad nedbrytning av TUBB3 i Kupffer-celler dämpar hepatocellulär karcinomprogression genom reglering av M1/M2-polarisering
Varför levercancerens immunceller i omgivningen spelar roll
De flesta föreställer sig cancer som en sjukdom där avvikande celler växer okontrollerat. Men tumörer lever i ett myller av immunceller, blodkärl och stödjevävnad som antingen kan bekämpa cancern eller tyst hjälpa den att växa. Den här studien fokuserar på levercancer—specifikt hepatocellulärt karcinom—och visar hur ett protein inne i specialiserade leverimmunceller kan tippa balansen mellan ett antitumörsvar och en tumörvänlig miljö. Att förstå denna dolda kontrollspak kan öppna nya vägar för att förbättra befintliga immunterapier.
En levercancer styrd av sin omgivning
Levern är rik på immunceller, inklusive en bosatt population kallad Kupffer-celler som normalt hjälper till att hålla organet friskt. Vid levercancer omvandlas många av dessa celler till tumörassocierade makrofager som antingen kan angripa cancern (ett M1-liknande tillstånd) eller skydda den (ett M2-liknande tillstånd). Patienter vars tumörer är fyllda med M2-typiska makrofager har ofta sämre prognos och svarar ibland dåligt på läkemedel som frigör immunsvaret, såsom PD-1-hämmare. Författarna började med att söka i offentliga genbanker och patientprover efter molekyler kopplade både till levercancer och till dessa makrofager, och landade på ett strukturellt protein kallat TUBB3 som oväntat var rikligt i tumörvävnad.
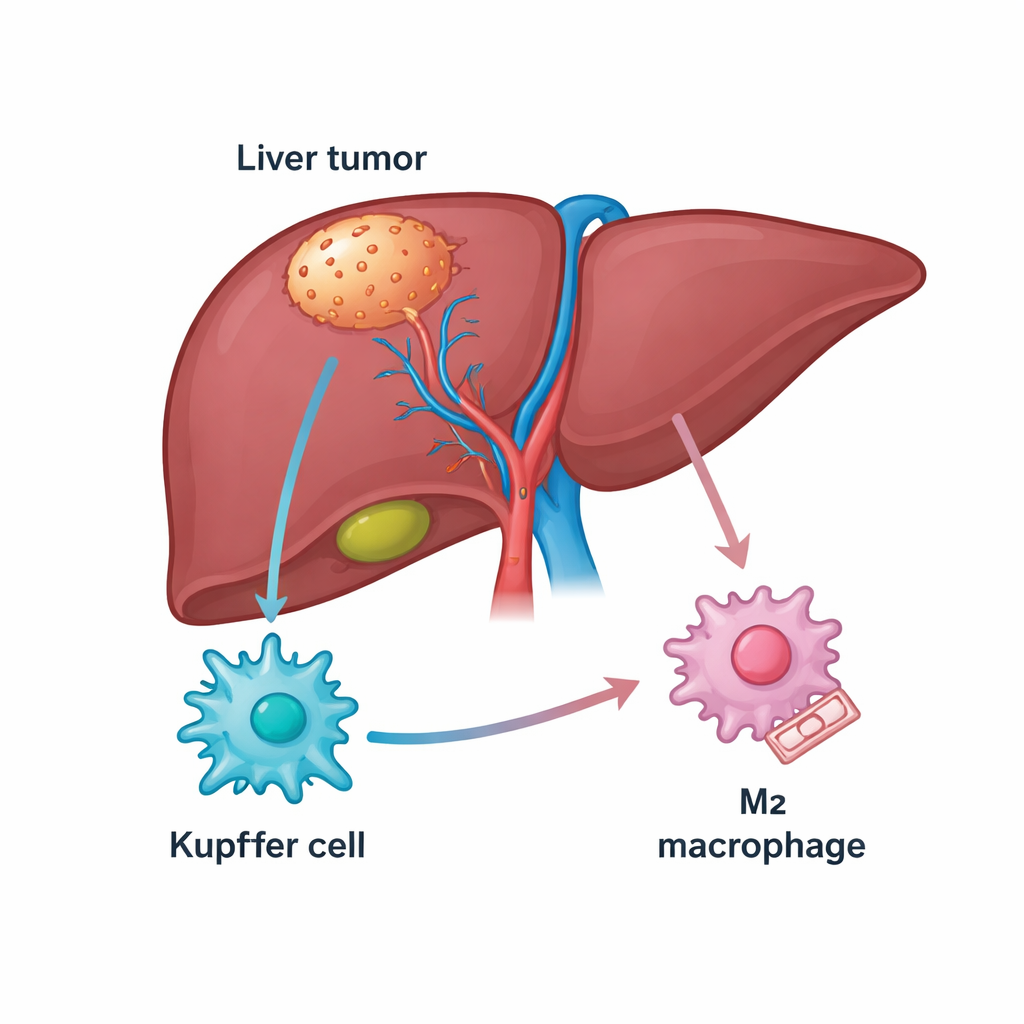
Ett överraskande protein som får immunceller att stödja tumörer
TUBB3 är mest känt som en byggsten i cellernas mikroskopiska “räls”, men har också kopplats till aggressivt beteende och läkemedelsresistens i flera cancerformer. Här fann forskarna att TUBB3-nivåerna var mycket högre i levertumörer än i närliggande frisk vävnad, och att patienter med mer TUBB3 ofta hade kortare överlevnad. Med färgningstekniker visade de att TUBB3 särskilt var förhöjt i Kupffer-celler inne i tumörer, och dess närvaro korrelerade starkt med markörer för den tumörstärkande M2-staten. Med andra ord var Kupffer-celler rika på TUBB3 mer benägna att bete sig så att de dämpar immunsvar och stödjer cancerns tillväxt.
Omlärning av makrofager för att hejda levertumörer
För att testa orsak och verkan sänkte teamet TUBB3-nivåerna i Kupffer-celler i laboratorieexperiment. När TUBB3 släcktes ned producerade dessa celler färre M2-typiska signaler, fler M1-typiska signaler och utsöndrade färre molekyler som normalt undertrycker immunaktivitet. Levercancerceller som exponerades för dessa omprogrammerade makrofager växte långsammare, delade sig mindre och var mindre benägna att migrera och invadera. I möss ledde blandningar av levercancerceller med TUBB3-bristande Kupffer-celler till mindre tumörer, mer cancercelldöd och en ökad infiltration av mördande CD8 T‑celler utrustade med destruktiva proteiner. Om makrofager togs bort från djuren helt och hållet försvann i stort sett fördelen med att blockera TUBB3, vilket understryker att effekten går genom dessa immunceller snarare än enbart genom cancercellerna.
Avslöjande av en intern broms på en nyckelsignalväg
Studien undersökte också hur TUBB3 utövar detta inflytande. Författarna fokuserade på en välkänd tillväxt- och överlevnadsväg styrd av proteinerna PTEN och AKT, som också påverkar om makrofager antar en M1- eller M2-identitet. De fann att sänkta TUBB3-nivåer ökade PTEN, vilket i sin tur minskade de aktiverande ”fosfat-taggarna” på AKT, och därmed sköt makrofager mot den tumörbekämpande staten. När de artificiellt återaktiverade AKT återgick makrofagerna till M2-mönstret och cancercellerna återfick sitt aggressiva beteende, även utan TUBB3. Detta placerar TUBB3 uppströms om PTEN och AKT som en slags intern ratt för makrofagbeteende.
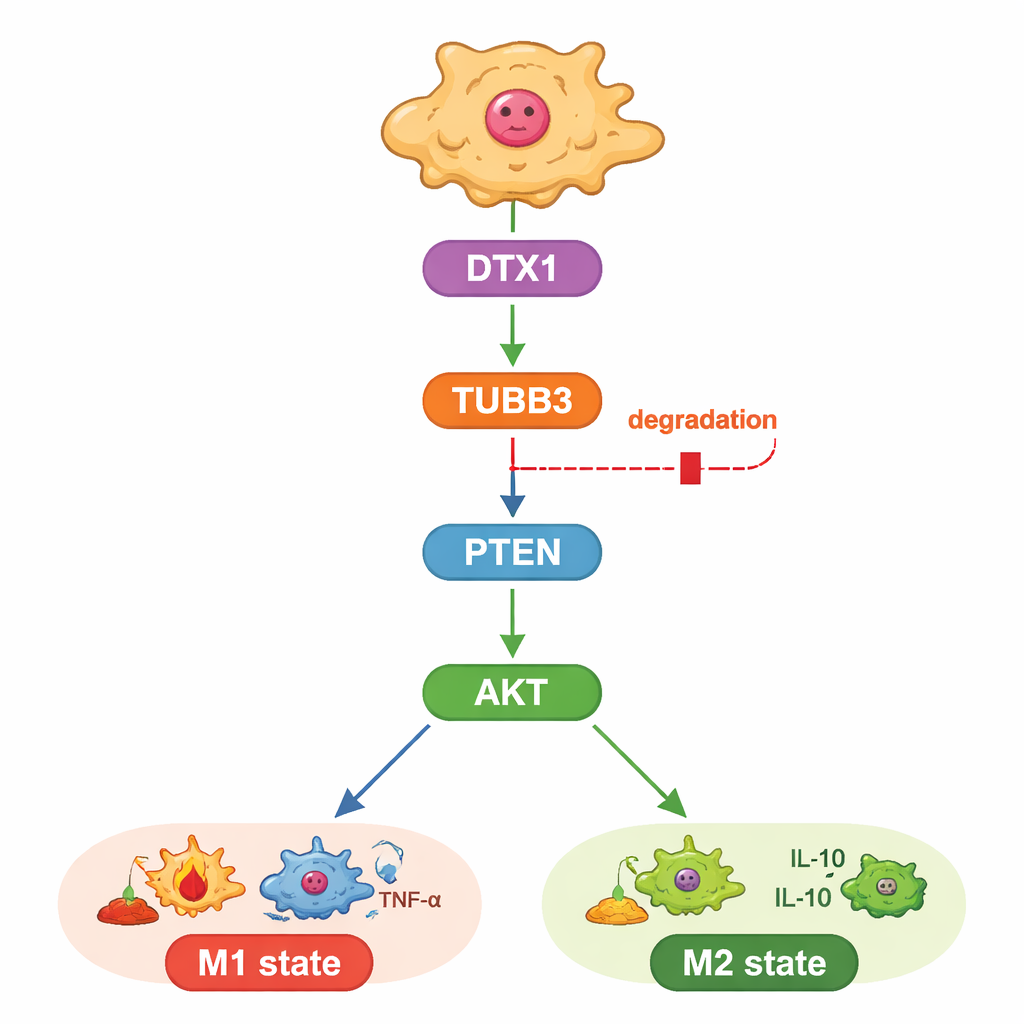
En inbyggd skräppost-tag som kan slås på igen
Slutligen undersökte forskarna varför TUBB3 är så rikligt i levertumörer. Genom att kombinera bioinformatiska förutsägelser med uttrycksdata identifierade de ett enzym kallat DTX1, som tillhör en familj som märker proteiner för nedbrytning, som en sannolik regulator. DTX1-nivåerna var lägre i levertumörer än i frisk vävnad och kopplades till bättre patientutfall och till en större närvaro av M1-typiska makrofager. In vitro accelererade ökat DTX1 TUBB3-nedbrytning, dämpade AKT-aktivitet och drev makrofager mot den tumörbekämpande staten, vilket hämmade cancercellernas tillväxt. Att återinföra extra TUBB3 åsidosatte fördelarna med DTX1, både i odlingsskålar och i mösstumörer. Tillsammans drar dessa resultat en tydlig linje från DTX1 via TUBB3 och PTEN/AKT till tumörens immunologiska tonläge.
Vad detta innebär för framtida behandling av levercancer
För icke-specialister är huvudbudskapet att denna forskning identifierar ett tidigare dolt styrsystem i leverns residenta immunceller som avgör om de hjälper eller hindrar cancer. När det skräppost-märkande enzymet DTX1 är lågt ackumuleras TUBB3, en tillväxtväg aktiveras och Kupffer-celler glider in i ett tumörstödjande läge som försvagar effekten av immunterapi. Att återställa denna bana—genom att sänka TUBB3, öka DTX1 eller fintunedera PTEN/AKT-signalen—kan återväcka lokalt immunsvar och göra behandlingar som PD-1-hämmare mer effektiva. Även om sådana strategier fortfarande är på experimentstadiet, understryker de potentialen i att behandla inte bara tumörcellerna utan också de omgivande immuncellerna som starkt påverkar hur levercancer beter sig.
Citering: Sun, J., Sun, T., Zhang, Y. et al. DTX1-mediated degradation of TUBB3 in Kupffer cells mitigates hepatocellular carcinoma progression by regulating M1/M2 polarization. Commun Biol 9, 311 (2026). https://doi.org/10.1038/s42003-026-09593-z
Nyckelord: hepatocellulär karcinom, tumörassocierade makrofager, Kupffer-celler, immunterapi, AKT-signalering