Clear Sky Science · sv
Strukturella insikter i WRN‑helikaset visar konformationsstater och möjligheter för läkemedelsupptäckt mot MSI‑H‑cancer
Varför detta är viktigt för cancerbehandling
Vissa cancerformer bär på en inneboende svaghet: de har svårt att reparera misstag i sitt DNA. Ett protein kallat WRN‑helikas fungerar som ett molekylärt reparationsverktyg som håller dessa sköra tumörer vid liv. Denna studie visar i atomär detalj hur WRN rör sig längs DNA och hur experimentella läkemedel kan låsa dess rörelse—vilket ger en färdplan för nya behandlingar som selektivt dödar dessa sårbara cancerceller samtidigt som frisk vävnad skonas.
DNA‑handlaren under mikroskopet
WRN‑helikas är en del av cellens underhållsbesättning och hjälper till att öppna upp DNA så att skador kan upptäckas och åtgärdas. Personer födda utan fungerande WRN utvecklar Werner‑syndrom, en sällsynt sjukdom kännetecknad av förtida åldrande, vilket visar hur avgörande detta protein är för genomintegriteten. Tumörer med ”mikrosatellitinstabilitet–hög” (MSI‑H)—en vanlig defekt i kolorektal och vissa andra cancerformer—visar sig vara särskilt beroende av WRN. När WRN stängs av i dessa celler faller deras redan bräckliga DNA snabbt samman och cancercellerna dör. Det gör WRN till ett lockande läkemedelsmål, men fram tills nu har forskarna saknat en tydlig bild av hur proteinet ändrar form när det griper DNA, förbrukar kemisk energi och rör sig längs det genetiska materialet.
Att se WRN böja sig och andas
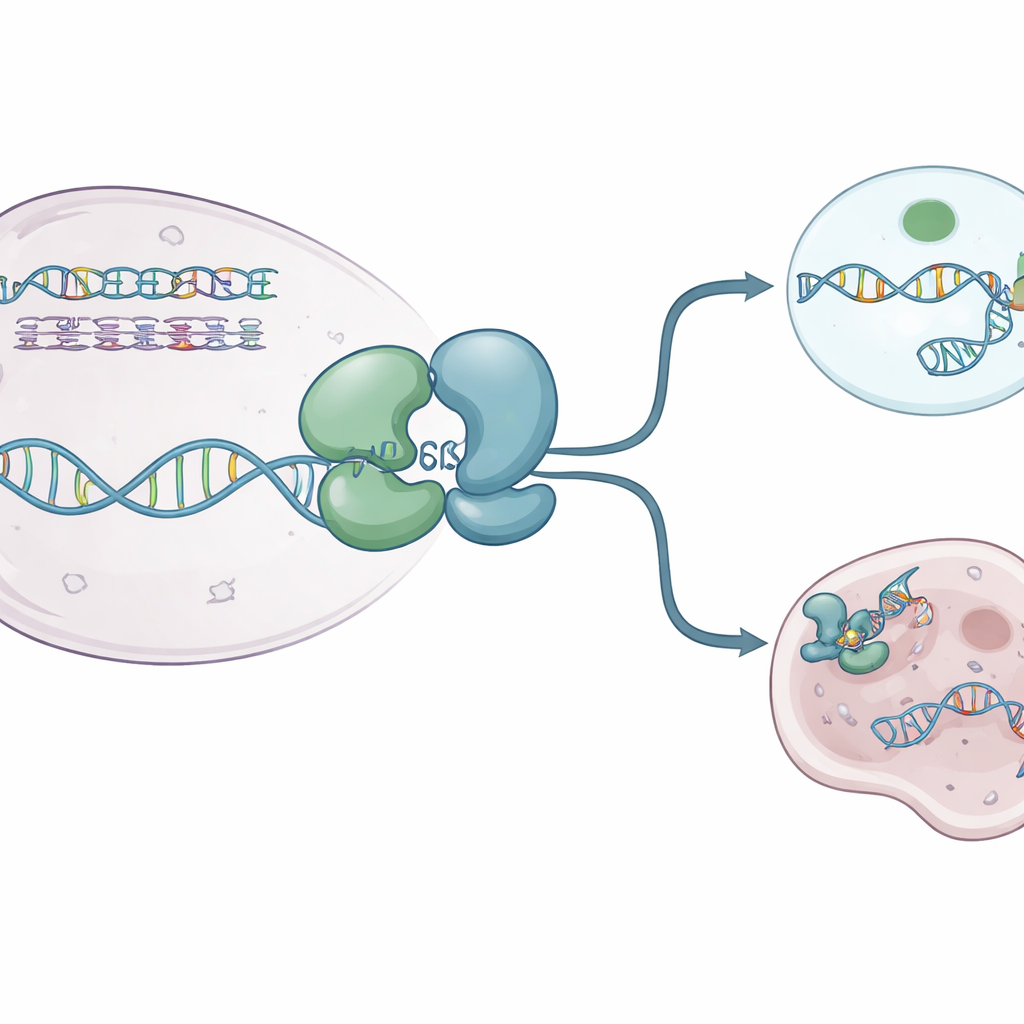
Författarna använde röntgenkristallografi för att fånga flera högupplösta ”ögonblicksbilder” av den humana WRN‑helikaskärnan. De löste strukturer av WRN ensamt och av WRN bundet till enkelsträngat DNA samt en icke‑klyvbar ATP‑liknande bränslemolekyl. Dessa vyer avslöjade att proteinet byggs upp av två huvudsakliga lober som förbinds av en flexibel gångjärnsliknande del som beter sig som en andningsled. I sitt vilande, bränslefria tillstånd antar WRN en kompakt ”stängd” form där loberna ligger nära varandra. När ATP‑liknande bränsle och DNA är närvarande svänger loberna isär till en mer ”öppen” konfiguration som kan omsluta DNA i en positivt laddad fåra. En liten aromatisk slinga inom WRN omformas till en kort helix och kilas in mellan DNA‑baskomponenter, fungerande som en spärrmekanism som hjälper proteinet att ta steg framåt utan att glida bakåt.
Hur nuvarande läkemedel slår av WRN
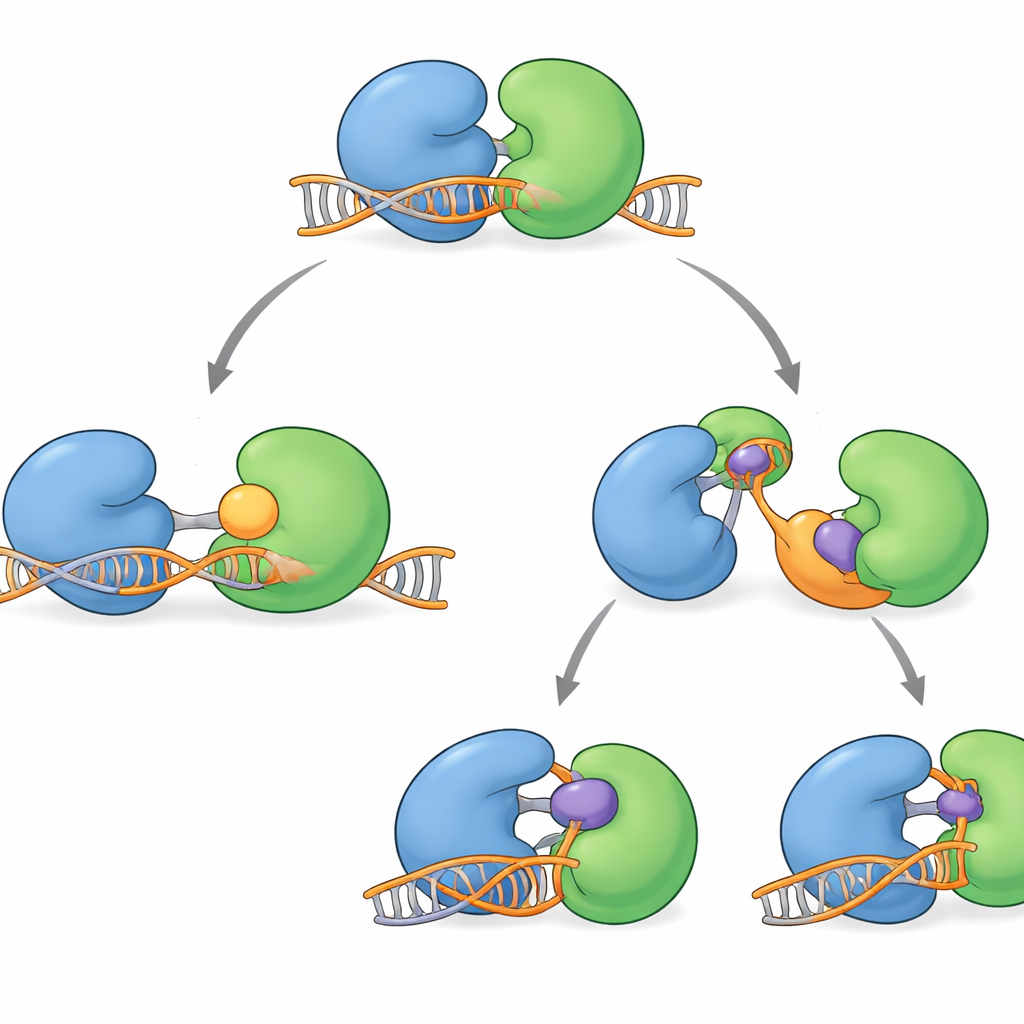
Flera WRN‑blockerande föreningar har nyligen gått in i kliniska prövningar. De täpper inte igen proteinet aktiva fåra direkt. I stället verkar de på avstånd, griper tag i gångjärnsregionen och låser WRN i former som inte kan engagera DNA på rätt sätt. Vissa molekyler, såsom HRO761 och en relaterad klinisk kandidat från GSK, vrider en lob ungefär 180 grader i förhållande till den andra och skapar en dramatisk ”vriden” form som ligger utanför DNA. Andra, inklusive VVD‑133214 och en nära släkt förening som studerats här, spänner fast WRN i en tätt ”stängd” konfiguration som inte exponerar viktiga DNA‑greppytor. Biofysiska experiment bekräftade att när dessa läkemedel är bundna kan WRN inte längre bilda ett stabilt komplex med enkelsträngat DNA, vilket effektivt bryter kopplingen mellan ATP‑användning och DNA‑upprullning.
Hur cancerceller lär sig att undkomma
För att se hur tumörer kan undvika dessa läkemedel odlade teamet MSI‑H kolorektala cancerceller i närvaro av WRN‑hämmare under veckor till månader. Resistent populationer uppstod snabbt. Genetisk analys visade att cellerna i varje fall hade förvärvat en enskild, precis ändring i WRN‑genen nära läkemedelsbindande gångjärnet. En mutation försvagade effekten av ”vridnings‑tillståndet” hos hämmaren HRO761, medan en annan mutation minskade känsligheten för VVD‑133214, som favoriserar det slutna tillståndet. Dessutom ökade många resistenta celler produktionen av WRN, vilket gav dem fler kopior av målet och delvis utspädde läkemedelseffekten. Dessa fynd speglar resistensmönster som setts med andra riktade cancerläkemedel, där små strukturella förändringar i målproteinet eller överexpression kan dämpa behandlingen.
Framåtblick mot smartare WRN‑blockerare
Tillsammans kartlägger de nya strukturerna en hel arbetscykel för WRN när det låser sig på DNA, tar steg och sedan återställer sig. De visar också att dagens kliniska föreningar främst stabiliserar proteinets ”av‑DNA” former. För en allmän läsare är huvudpoängen att vi nu förstår var WRN är sårbart och hur tumörer kan anpassa sig. Detta antyder en nästa våg av hämmare som binder WRN när det sitter fast på DNA, potentiellt fångande det i ett toxiskt tillstånd—likt framgångsrika läkemedel som fångar andra DNA‑reparationsenzymer. Sådana ”på‑DNA” WRN‑blockerare, använda ensamma eller tillsammans med befintliga medel, kan erbjuda mer hållbara sätt att utnyttja den dolda svagheten hos MSI‑H‑cancer.
Citering: Fletcher, C.T., Mornement, A.A., Barrett, C. et al. Structural insights into WRN helicase reveal conformational states and opportunities for MSI-H cancer drug discovery. Commun Biol 9, 334 (2026). https://doi.org/10.1038/s42003-026-09584-0
Nyckelord: WRN‑helikas, mikrosatellitinstabilitet, DNA‑reparation, allosteriska hämmare, läkemedelsresistens