Clear Sky Science · sv
Kvalitetsbedömning av RNA 3D-struktursmodeller med djupinlärning och mellanliggande 2D-kartor
Varför det är viktigt att värdera RNA-former
Inuti varje cell viker sig RNA-molekyler och antar intrikata tredimensionella former som hjälper till att styra vilka gener som slås på, leda kemiska reaktioner och till och med försvara mot virus. I dag kan kraftfulla datorprogram förutsäga många av dessa former, men forskare står fortfarande inför ett grundläggande problem: när datorn producerar dussintals eller hundratals kandidatstrukturer för samma RNA, vilken av dem ligger verkligen nära verkligheten? Denna artikel presenterar RNArank, ett AI-verktyg utformat för att tackla den frågan genom att betygsätta RNA 3D-modeller, ungefär som en strukturell kvalitetsinspektör, så att forskare kan koncentrera sig på de mest trovärdiga förutsägelserna.
En ny inspektör för RNA-modeller
RNArank är byggt för att bedöma kvaliteten hos en föreslagen RNA-form utan att behöva veta hur formen skapats. Oavsett om modellen kommer från ett djupinlärningssystem, en fysikbaserad simulering eller en mänsklig expert, tittar RNArank endast på de slutliga 3D-koordinaterna. Det frågar sedan, i praktiken: ”Ser den här strukturen ut som ett realistiskt RNA?” Denna typ av oberoende kvalitetsbedömning är viktig eftersom RNA-prediktion, till skillnad från proteinvärlden där verktyg som AlphaFold ofta ger mycket tillförlitliga svar direkt, fortfarande gagnas av att kombinera flera metoder och mänsklig insikt — och av ett smart sätt att ranka de resulterande modellerna.
Att lära AI vad bra RNA ser ut som
För att träna RNArank sammanställde författarna cirka 200 000 RNA-strukturer, som täcker ett brett spektrum från uppenbart felaktiga till nästan perfekta. Dessa byggdes från kända experimentella strukturer med hjälp av en mängd olika angreppssätt, inklusive moderna djupinlärningsprediktorer, molekylär dynamiksimuleringar som efterliknar atomrörelser och avsiktliga förvrängningar av korrekta strukturer för att skapa ”decoys”. För varje modell beräknade teamet hur nära den överensstämde med det verkliga, experimentellt bestämda RNA:t, med en förfinad noggrannhetspoäng anpassad till RNA kallad lDDT_RNA. Denna poäng fokuserar på hur väl avstånden mellan nukleotidpar reproduceras, vilket fångar både övergripande veckning och lokala detaljer utan att vara överdrivet känslig för molekylens längd.
Hur RNArank läser och poängsätter ett RNA
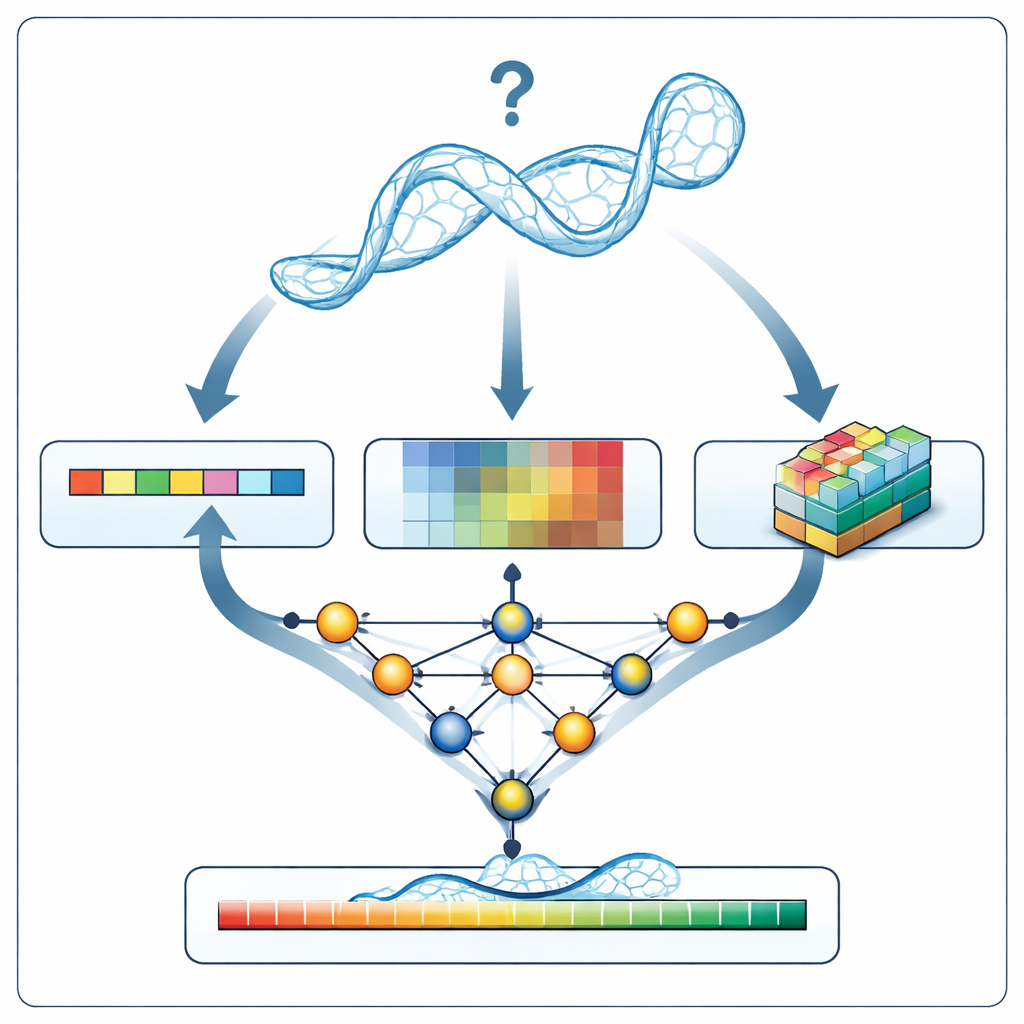
När RNArank undersöker en ny RNA-modell översätter det först strukturen till tre typer av information: en 1D-beskrivning av sekvensen och ryggradens geometri längs kedjan, 2D-beskrivningar av hur varje par nukleotider förhåller sig till varandra (deras avstånd, uppskattade interaktionsenergier och möjliga atomkrockar) samt 3D ”voxel”-snabbfotografier, små rutnät som fångar den lokala atommolnet runt varje nukleotid. Ett flerdelat neuralt nätverk väver ihop dessa ledtrådar till en enhetlig bild och förutspår sedan två mellanliggande 2D-kartor: vilka nukleotider som sannolikt är i kontakt och hur mycket varje modellerat avstånd sannolikt avviker från den okända sanna strukturen. Från dessa kartor rekonstruerar RNArank både en per-nukleotid tillförlitlighetspoäng och en övergripande poäng för hela RNA-modellen.
Metoden utsatt för test
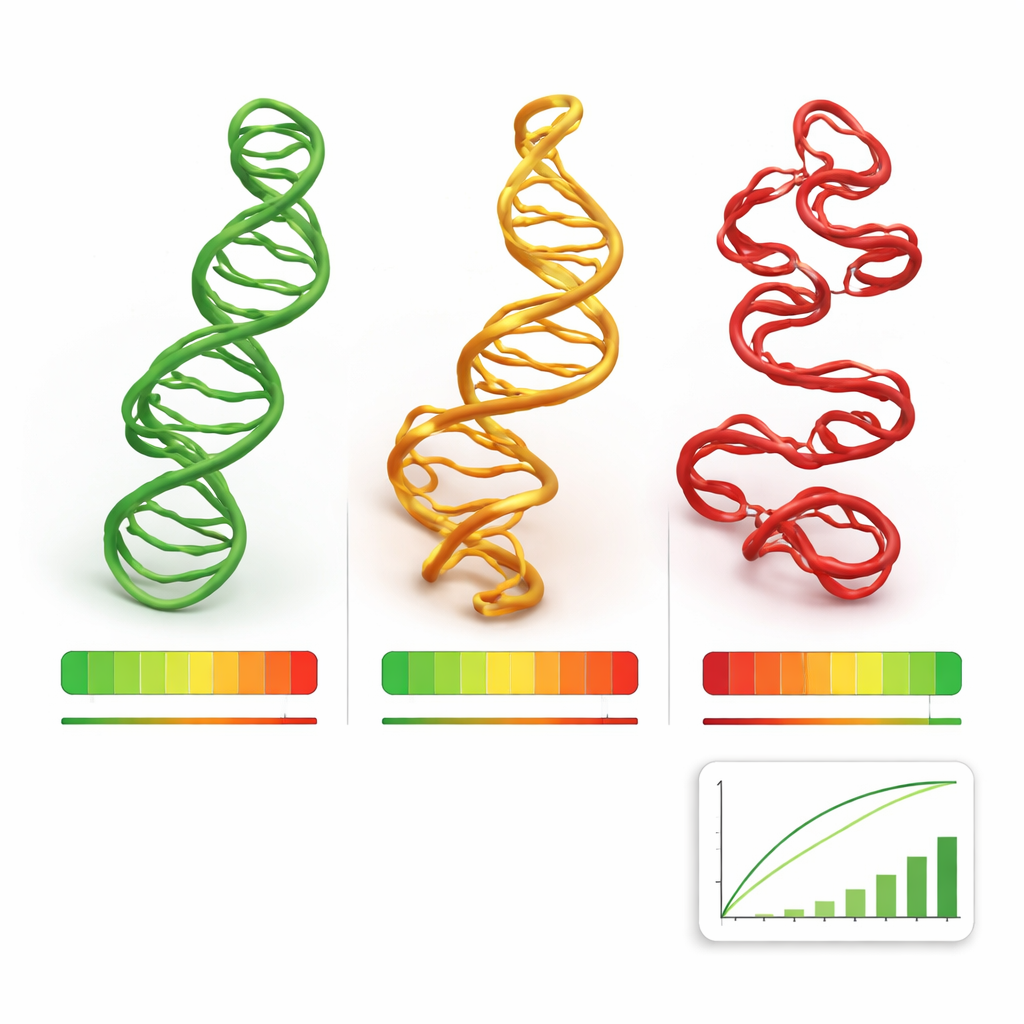
Teamet utvärderade RNArank på tre krävande datasätt: en uppsättning om 24 nyligen lösta RNA från Protein Data Bank och RNA-målen från två internationella blinda förutsägningstävlingar, CASP15 och CASP16, där många grupper skickar in modeller utan att känna svaren i förväg. Över tusentals kandidatstrukturer följde RNAranks poäng den verkliga modellkvaliteten närmare än flera etablerade energibaserade scoringsmetoder och andra djupinlärningsmetoder. Den var särskilt bra på att plocka ut de bästa eller näst bästa modellerna ur en pool och på att identifiera vilka delar av en struktur som sannolikt var opålitliga. Författarna visade också att RNArank bibehöll sin prestanda även på RNA som tydligt skilde sig i sekvens från dem som förekom i träningen, ett tecken på verklig generalisering snarare än memorering.
Gränser i dag och utsikter framåt
RNArank är inte perfekt: det har fortfarande problem med särskilt flexibla RNA som antar många former och med RNA som ändrar sitt utseende när de hålls på plats av proteiner i stora molekylära maskiner. Däremot är det tillräckligt snabbt för att hantera många modeller för RNA av några hundra nukleotider på bara sekunder, och det hjälper redan automatiserade servrar att välja förutsägelser av högre kvalitet i samhällsomfattande tester. Genom att tillhandahålla en metod-agnostisk, strukturendimensionell domare för RNA-modeller ger RNArank biologer ett skarpare filter för att omvandla rå datoroutput till tillförlitliga strukturella hypoteser, vilket för fältet ett steg närmare rutinmässiga, pålitliga förutsägelser av RNA-former och i förlängningen djupare insikter i hur dessa mångsidiga molekyler fungerar.
Citering: Liu, X., Wang, W., Du, Z. et al. Quality assessment of RNA 3D structure models using deep learning and intermediate 2D maps. Commun Biol 9, 293 (2026). https://doi.org/10.1038/s42003-026-09582-2
Nyckelord: RNA 3D-struktur, djupinlärning, modellkvalitetsbedömning, strukturell bioinformatik, RNArank