Clear Sky Science · sv
Lokal katjon-klämning förvränger och mjukar upp RNA-duplex
Varför denna lilla vridning i RNA spelar roll
Inuti varje cell böjs, sträcks och vrids DNA och RNA ständigt när de lagrar och använder genetisk information. Dessa rörelser är inte bara mekaniska detaljer — de styr hur gener läses, hur virus kopierar sig och hur nya RNA-baserade läkemedel och nanodevices kommer att fungera. Denna studie visar att enkla salter bestående av positivt och negativt laddade joner kan förändra hur styvt eller flexibelt RNA är påtagligt, och att RNA svarar mycket annorlunda än DNA. Att förstå denna subtila ”mjuknings- och härdnings”-dans kan hjälpa forskare att bättre utforma RNA-läkemedel, vacciner och molekylära verktyg.
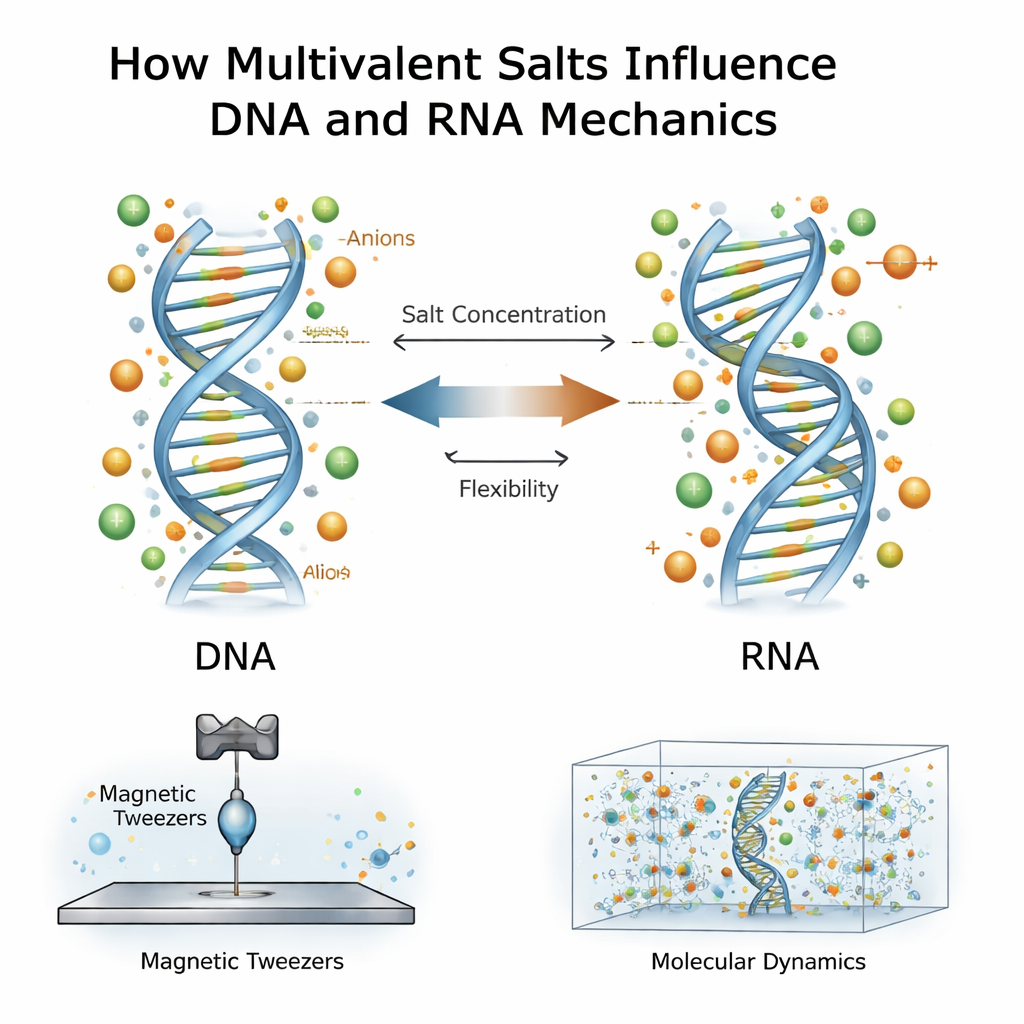
Salta omgivningar och genetiska molekyler
DNA och RNA bär en stark negativ elektrisk laddning, så de omges av moln av motsatt laddade joner i vatten. Det mesta tidigare arbetet har fokuserat på positivt laddade joner, särskilt multivalenta sådana som bär två eller tre positiva laddningar, till exempel magnesium eller spermidin. Dessa joner är kända för att hålla DNA-strängar samman, kondensera dem eller ändra hur lätt de böjs. RNA, även om det är kemiskt likt DNA, beter sig annorlunda: det är vanligtvis svårare att böja men lättare att sträcka. Det nya arbetet ställer en djupare fråga: vad händer när både de positiva jonerna och deras medföljande negativa partner — kallade anjoner — interagerar med DNA och RNA vid mycket höga salthalter, mycket högre än i typiska celler?
Drar i enskilda molekyler för att mäta styvhet
Forskarna använde en teknik som kallas magnetiska pincetter för att sträcka enskilda DNA- eller RNA-dubbelspiraler en i taget. Varje molekyl var förankrad i ena änden på en glasskiva och i andra änden vid en liten magnetisk pärla. Genom att röra magneter ovanför provet kunde de dra med kontrollerade krafter och registrera hur långt varje molekyl förlängdes och hur den vridits under spänning. Från dessa kraft–förlängningskurvor drog de ut fyra viktiga mekaniska egenskaper: hur svår molekylen är att böja, hur svår den är att sträcka, dess effektiva längd per baspar och hur vridning påverkar dess längd. De upprepade dessa mätningar över ett brett spektrum av multivalenta saltkoncentrationer för flera olika salter, inklusive spermidin och kalciumklorid.
DNA härdas igen, men RNA mjuknar plötsligt
För DNA stämde beteendet i stort sett med förväntningarna. När koncentrationen av multivalenta positiva joner ökade blev DNA först lättare att böja — dess styvhet minskade — eftersom jonerna neutraliserade dess negativa laddning. Vid ännu högre nivåer överkompenserade de positiva jonerna och vände effektivt DNA:s nettoladdning. Denna ”laddningsinversion” gjorde DNA svårare att böja igen, så dess styvhet ökade. Överraskande nog visade RNA mönstret motsatt och mer dramatiskt. Vid låga till måttliga saltnivåer ökade dess böjstyvhet: RNA-duplexet blev rakare och mer stelt. Men vid mycket höga koncentrationer sjönk RNA:s böjstyvhet med mer än hälften, och andra egenskaper såsom dess töjbarhet och vrid–sträck-beteende vändes på oväntade sätt.
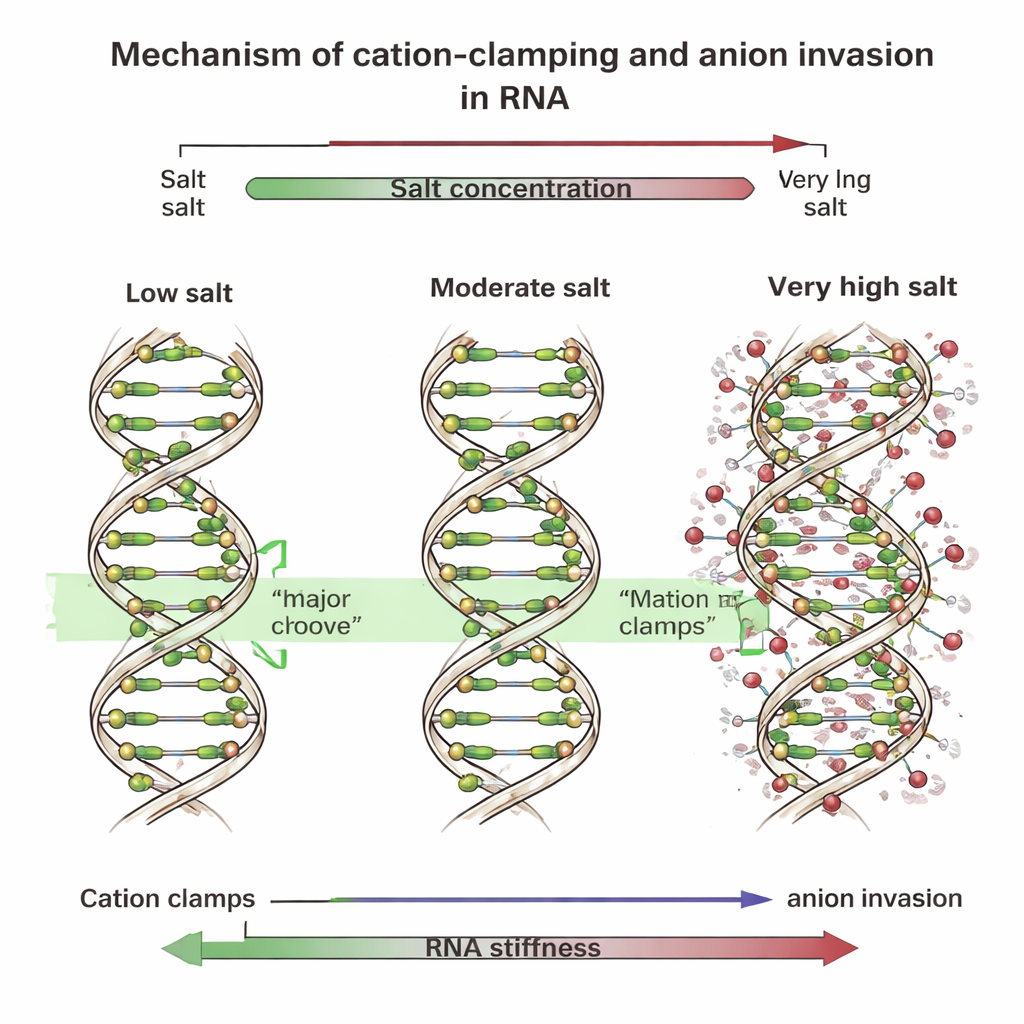
Klämmor, spår och invaderande joner
För att avslöja orsaken körde teamet detaljerade datorsimuleringar som följde varje atom i korta DNA- och RNA-fragment i saltat vatten. Dessa simuleringar visade att vid låga och måttliga koncentrationer sätter sig multivalenta positiva joner i en vid yta på RNA som kallas den stora fåra. Där bildar de ”katjonklämmor” som sträcker sig över fåran, drar dess sidor närmare varandra, rätar ut helixen och gör den stelare. DNA, vars fåror har annan form, binder dessa joner främst längs sin yttre ryggrad istället. Vid mycket höga saltnivåer tränger dock många negativa joner — som klorid — nära RNA-ryggraden och in i den stora fåran. Deras närvaro stör de ordnade klämmorna och bryter upp dem i oregelbundna, fläckvisa ”lokala klämmor” som förvränger helixen. När forskarna efterliknade denna effekt genom att lägga till artificiella fjädrar eller låsa extra negativa joner nära RNA i simuleringar, böjde sig RNA-ryggraden mer och dess totala styvhet rasade, precis som i experimenten.
Vad detta betyder för framtida RNA-teknologier
Enkelt uttryckt visar studien att RNA kan göras antingen rakare och styvare eller mer vinklad och flexibel endast genom att ändra typen och koncentrationen av omgivande salter. Vid måttliga nivåer av multivalenta joner klämmer positiva laddningar snyggt RNA:s yta och spänner upp den; vid extrema nivåer bryter invaderande negativa joner sönder den enhetliga upprustningen och skapar sneda, mjukare regioner. DNA visar inte denna skarpa mjukning eftersom det binder joner på ett annat sätt och istället genomgår en nettoladdningsinversion. Dessa insikter betonar att inte bara positiva joner utan även deras negativa partners är avgörande för att kontrollera RNA-form. Den kunskapen hjälper forskare att medvetet ställa in RNA-mekanik i laboratoriet — till exempel för att stabilisera RNA-läkemedel, styra hur RNA veckar sig i biosensorer eller designa mer pålitliga RNA-baserade nanostrukturer.
Citering: Zhang, C., Dong, HL., Zhang, JH. et al. Local cation-clamping distorts and softens RNA duplex. Commun Biol 9, 308 (2026). https://doi.org/10.1038/s42003-026-09580-4
Nyckelord: RNA-mekanik, multivalenta joner, katjonklämning, DNA kontra RNA, salteffekter