Clear Sky Science · sv
CISH, en viktig intracellulär spärr, i jämförelse och kombination med befintliga och framväxande cancerimmunologiska checkpoints
Släppa bromsen på cancermotverkande celler
Cancerimmunterapier har förändrat utsikterna för många patienter, men en stor andel människor får fortfarande liten eller ingen nytta. Denna studie undersöker ett nytt sätt att förstärka kroppens egna T‑celler—immunsystemets ”hitmän”—genom att inaktivera en intern ”broms” kallad CISH. Till skillnad från nuvarande läkemedel som verkar på reglage i cellens yta riktar sig denna strategi mot ett kontrollsystem begravt inne i cellen, med målet att göra ingenjörsproducerade T‑celler mycket bättre på att finna och förstöra tumörer, även när cancer försöker gömma sig.
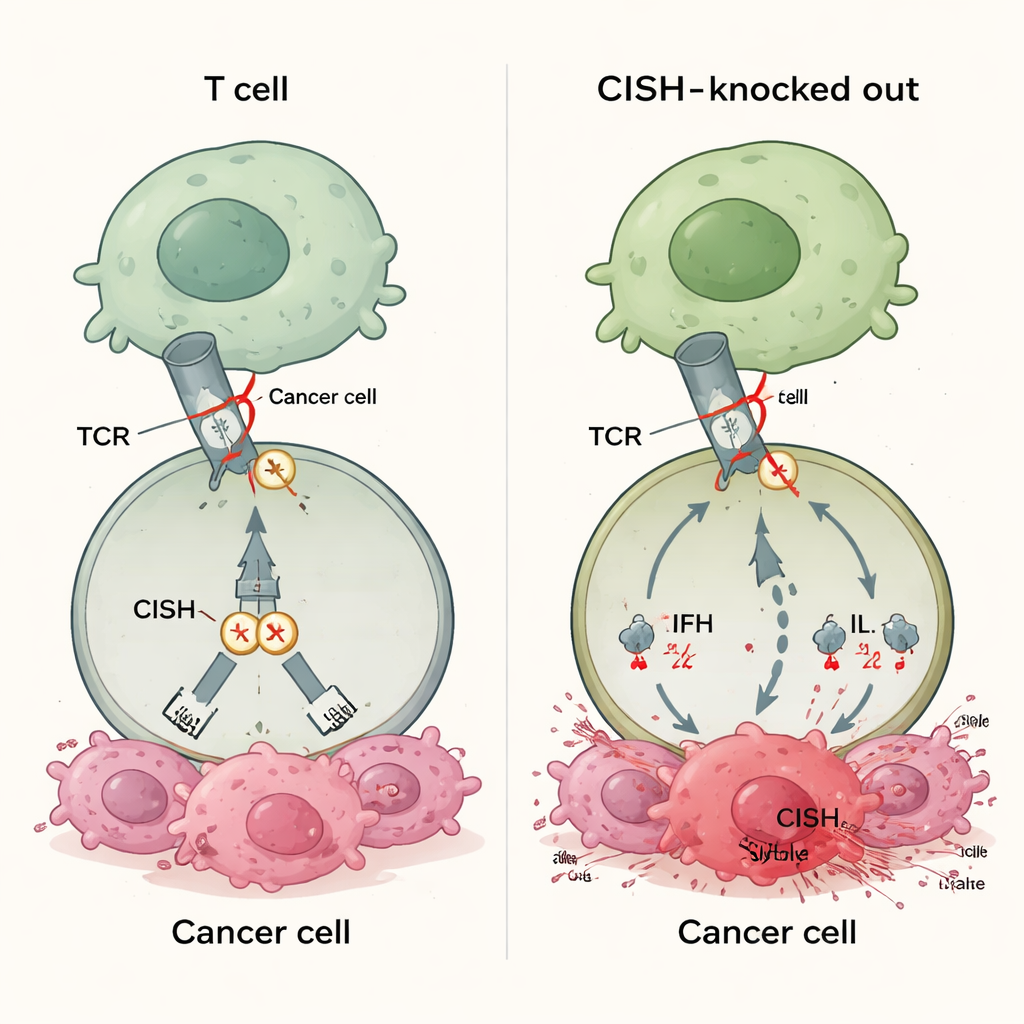
En ny typ av immunbroms
De flesta godkända immunterapiläkemedel blockerar proteiner som PD‑1 på T‑cellens yta. Dessa läkemedel fungerar bara när tumörer visar matchande partnermolekyler som PD‑L1, och många cancerformer uttrycker antingen aldrig tillräckligt av dessa partners eller förlorar dem över tid. Det hjälper till att förklara varför 30–60 % av patienterna inte svarar på dagens checkpoint‑behandlingar. CISH tillhör en annan klass av bromsar som sitter inne i T‑cellen. Den slås på när T‑cellreceptorn känner av ett mål och dämpar då signalen genom att främja nedbrytningen av ett nyckelprotein i signalvägen. Eftersom denna verkan inte är beroende av ligander uttryckta av tumören, kan avstängning av CISH i princip förstärka T‑cellsreaktioner över många cancertyper, oberoende av PD‑L1‑status eller andra biomarkörer.
Huvud mot huvud med befintliga checkpoints
Forskarna använde CRISPR‑genredigering för att ta bort CISH och jämförde de resulterande T‑cellerna med celler som saknade PD‑1 eller flera andra intracellulära bromsar. När de stimulerade T‑cellerna svagt—en situation avsedd att efterlikna tumörer som bara visar låga mängder antigen—producerade CISH‑borttagna celler mycket mer av viktiga immunsignaler, inklusive interferon‑gamma, TNF‑alpha och IL‑2. Dessa celler var också mer ”polyfunktionella”, vilket betyder att enskilda T‑celler kunde utföra flera uppgifter samtidigt, ett kännetecken för kraftfull antitumöraktivitet. I kontrast hjälpte det inte att enbart ta bort PD‑1 under dessa lågsignalsförhållanden. I flera tester ökade förlust av CISH aktivering, dödande kapacitet och bildandet av bestående minneslika T‑celler mer än borttagning av andra föreslagna interna checkpoints som RASA2, CBLB, SOCS1, REGNASE1, HPK1 eller PTPN1/2.
Samarbete med andra interna reglage
Eftersom T‑cellsignalering styrs av många överlappande vägar frågade teamet om kombinationen av CISH‑borttagning och borttagning av andra bromsar kunde ge additiva fördelar. Med multiplex CRISPR‑redigering fann de att borttagning av CISH tillsammans med SOCS1, HPK1 eller RASA2 ytterligare ökade produktionen av hjälpsamma cytokiner vid svag stimulans. I en tumörmodell byggd kring en vanlig KRAS‑mutation var T‑celler konstruerade med en KRAS‑specifik receptor bättre på att döda cancerceller när CISH togs bort, och denna effekt blev starkare när CISH‑borttag kombinerades med antingen SOCS1‑ eller RASA2‑borttag. Dessa fynd tyder på att CISH styr en icke‑redundant nod i T‑cellsbiologin och kan samarbeta med utvalda partners för att skärpa tumörspecifikt dödande.
Göra CAR‑T‑celler tåligare mot listiga tumörer
Författarna gick sedan vidare till en kliniskt viktig situation: CAR‑T‑celler riktade mot B‑cellsmarkören CD19. De skapade leukemiceller som uttryckte olika nivåer av CD19 för att efterlikna tumörer som tappar eller minskar sina mål för att undkomma behandling. CAR‑T‑celler utan CISH var avsevärt bättre på att förstöra cancerceller, även när CD19 var knapp, och utsöndrade fler aktiverande och rekryterande signaler. Samtidigt släppte de ut lägre mängder molekyler som är kända för att försvaga T‑celler eller främja tumörtillväxt, såsom Galectin‑1, Galectin‑3, lösligt 4‑1BB, IL‑1α och glykoproteinet EMMPRIN/CD147. Tillsammans pekar dessa förändringar mot en mer aggressiv, svårare att undertrycka CAR‑T‑cell, särskilt väl lämpad för fientliga, låg‑antigen‑tumörmiljöer.
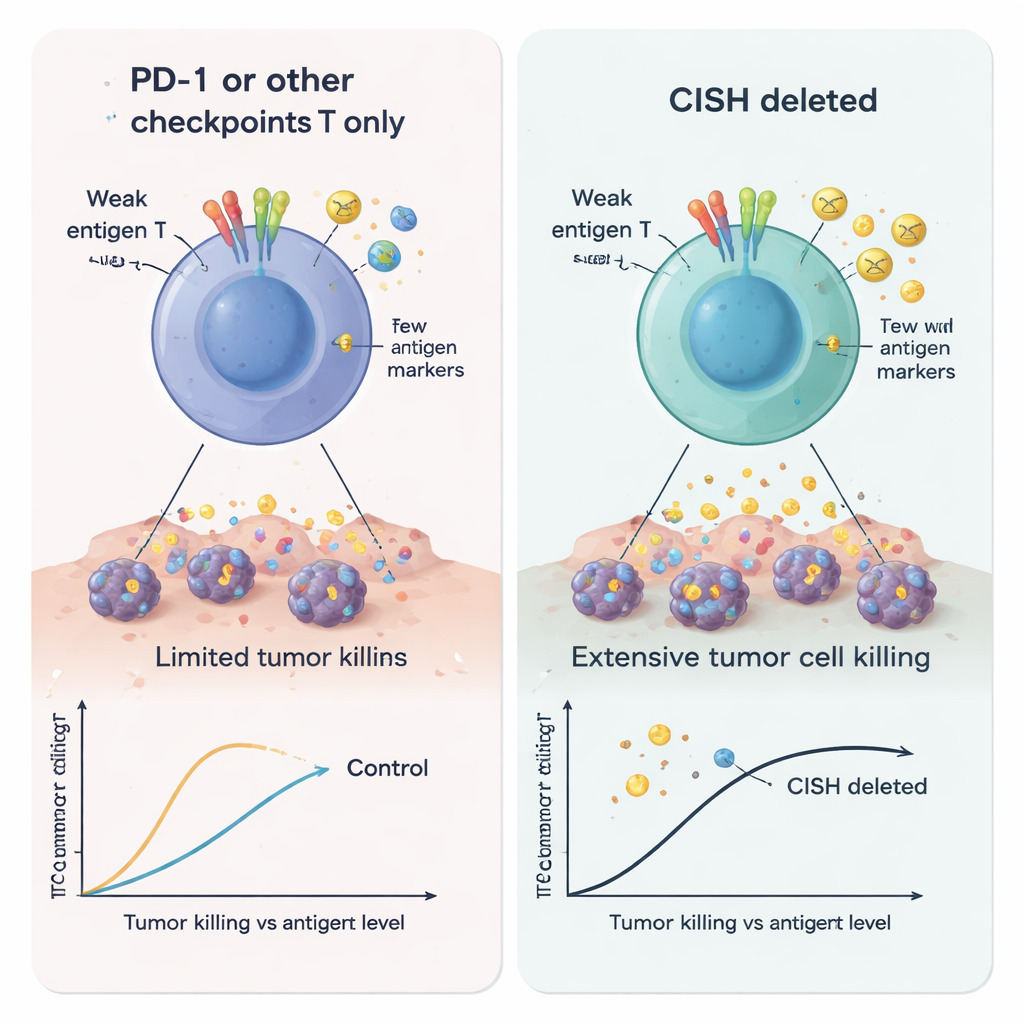
Från laboratoriebänk till patienter
Bortom provrör och odlingsskålar har idén att rikta in sig på CISH redan nått patienter. En första människa‑studie där tumörinfiltrerande lymfocyter redigerats för att ta bort CISH hos en person med avancerad kolorektalcancer gav ett komplett svar som varat i mer än två år, trots cancerens motståndskraft mot flera tidigare behandlingar. Genom att demonstrera att CISH är en kraftfull, läkbar intern checkpoint som ökar T‑cells känslighet för även svaga tumörsignaler hjälper denna studie till att förklara det anmärkningsvärda kliniska resultatet och stöder ansträngningar att utveckla framtida terapier—vare sig genredigerade celler eller piller—som säkert luckrar upp denna interna broms och breddar räckvidden för cancerimmunterapi.
Citering: Cano, F., Bravo-Blas, A., Colombe, M. et al. CISH, a key intracellular checkpoint, in comparison and combination to existing and emerging cancer immune checkpoints. Commun Biol 9, 319 (2026). https://doi.org/10.1038/s42003-026-09579-x
Nyckelord: cancerimmunterapi, T‑celler, CAR‑T‑terapi, immunologiska checkpoints, CRISPR‑genredigering