Clear Sky Science · sv
En sjukdomsframkallande mutation i α-SNAP försämrar membranlipidbindning genom att dölja en kritisk hydrofob snibb
Hur en mikroskopisk förändring i ett protein kan störa hjärnans utveckling
Våra hjärnceller skickar ständigt gods i små blåsor kallade vesiklar, och ett hjälpprotein som heter alpha-SNAP är centralt för att leveranserna ska kunna ske. En sällsynt mutation i alpha-SNAP, känd från en muslinje kallad “hyh”, leder till allvarliga problem i hjärnans bildning och vätskebalans. Denna studie ställer en till synes enkel fråga med stora konsekvenser: hindrar den där enda aminosyraförändringen alpha-SNAP från att fästa vid cellmembran, och kan det vara en nyckelorsak till att hjärnan utvecklas fel?
En cellulär kajarbetare med många uppgifter
Alpha-SNAP fungerar normalt som en slags kajarbetare för vesiklar, och hjälper dem att fusera med cellens membraner så att gods kan frisättas eller återvinnas. Den samarbetar med en uppsättning proteiner kallade SNAREs och en energidriven maskin, NSF, för att dra membraner samman och sedan återställa systemet inför nästa omgång. Utöver denna klassiska roll hjälper alpha-SNAP också till att reglera processer som cellens självstädning (autofagi), programmerad celldöd, kalciuminflux och energisensorik. Alla dessa funktioner beror, på ett eller annat sätt, på alpha-SNAPs förmåga att ta i och delvis tränga in i det oljiga membranets yta.
En dold snibb och en besvärlig mutation
Tidigare arbete visade att alpha-SNAP använder en kort fet “snibb” nära ena änden av proteinet för att haka i membraner. Hos det friska proteinet sticker denna snibb ut och kan dyka ner i membranets yttre lager. I hyh-musen byts en enskild byggsten vid position 105 ut, vilket ger M105I-mutationen. Författarna använde datorbaserade simuleringar för att se hur denna förändring påverkar proteinets form. De fann att det muterade proteinet blir något kompaktare och vrider sig så att den hydrofoba snibben viks inåt, bort från vatten och membraner. Som ett resultat närmar sig det muterade proteinet membraner i en plattare vinkel och tenderar att trycka mot dem med en mindre klibbig yta, vilket minskar både kontakttid och insättningsdjup. Beräkningar av bindningsenergi stödde detta: vildtypproteinet lade sig i ett lågenergiltillstånd med stark bindning, medan mutanten föredrog svagare, grundare kontakter.
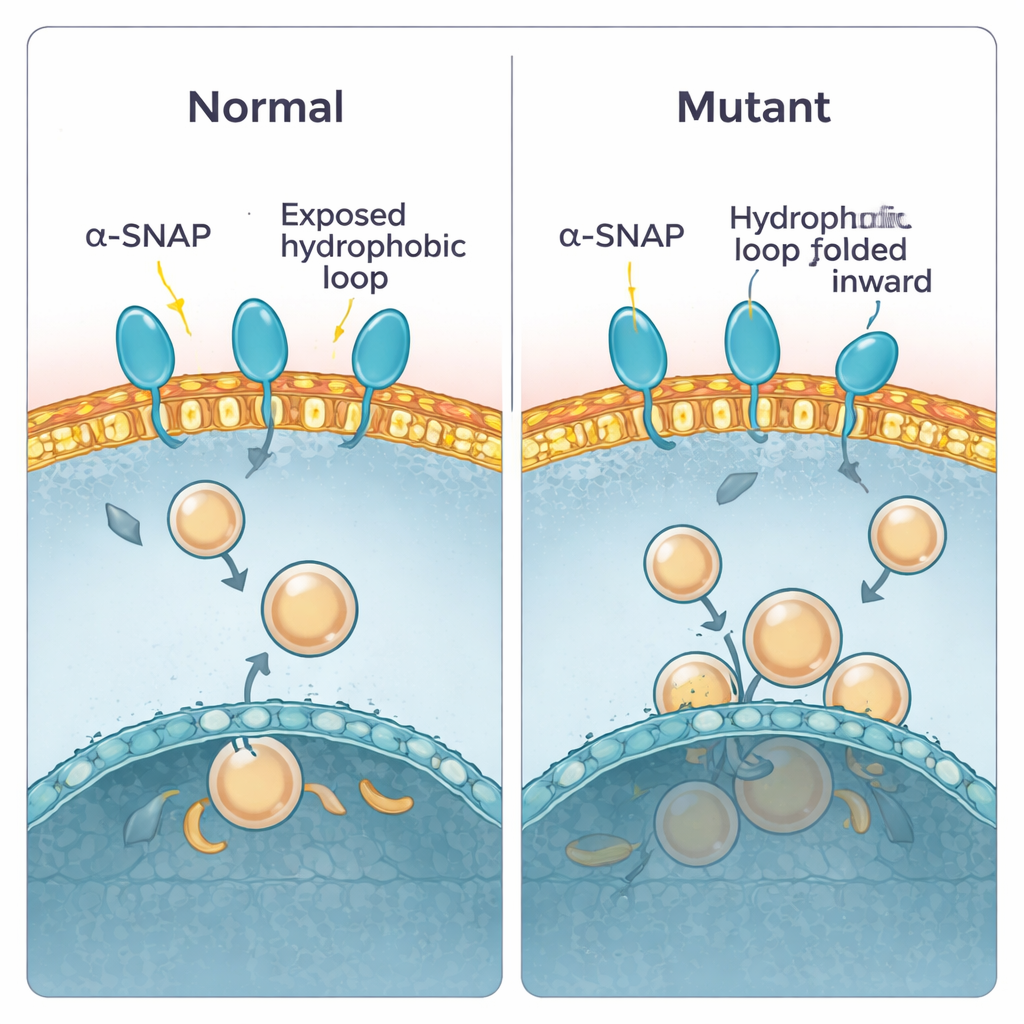
Att testa förutsägelsen i labbet
För att kontrollera dessa förutsägelser renade teamet både normalt och muterat alpha-SNAP och testade hur de uppträdde i olika experimentella uppsättningar. Först använde de ett tvättmedel som separerar i en vatten- och en oljefas, vilket efterliknar valet mellan vatten och membran. Normalt alpha-SNAP fördelade sig jämnt, i linje med en balanserad, delvis oljig yta. Den muterade varianten var mindre benägen att gå in i oljefasen, vilket tyder på att dess feta delar faktiskt är mer begravda. Därefter lät de proteinerna interagera med platta plasma-membran ”ark” preparerade från celler och avbildade hur många bindningsställen som uppstod. Återigen prickade normalt alpha-SNAP membranet medan mutanten band mycket mindre. Slutligen flöt de konstgjorda membranblåsor (liposomer) gjorda av hjärnlipider genom sockertäta gradienter. Vildtypens alpha-SNAP följde med vesiklar rika på plasmamembranlipider uppåt, medan mutanten halkade efter och band dåligt om inte vesiklarna var gjorda av en annan, mer intern membransammansättning.
Konsekvenser i den utvecklande hjärnan
Forskarna vände sig sedan till hjärnor från utvecklande musembryon, med fokus på en fas när nya nervceller bildas. Genom att separera cellulärt innehåll i lösliga och membranbundna fraktioner visade de att totalnivåerna av alpha-SNAP redan var reducerade i hyh-hjärnor, men viktigare var att andelen fäst vid membran var oproportionerligt låg jämfört med normala möss. När de vidare separerade olika membrantyper fann de att den största förlusten skedde vid plasmamembranet, cellens yta, medan interna membraner var mycket mindre påverkade. Mikroskopi berättade samma historia: i normalt vävnad konturerade alpha-SNAP celler i ett bikakemönster som matchade en känd ytmarkör. I hyh-hjärnor tonade denna skarpa gränsfärg bort till ett mer diffust, internt sken, vilket indikerar att det muterade proteinet inte stannar förankrat vid cellkanten där vesikelfusion och signalering är mest aktiva.
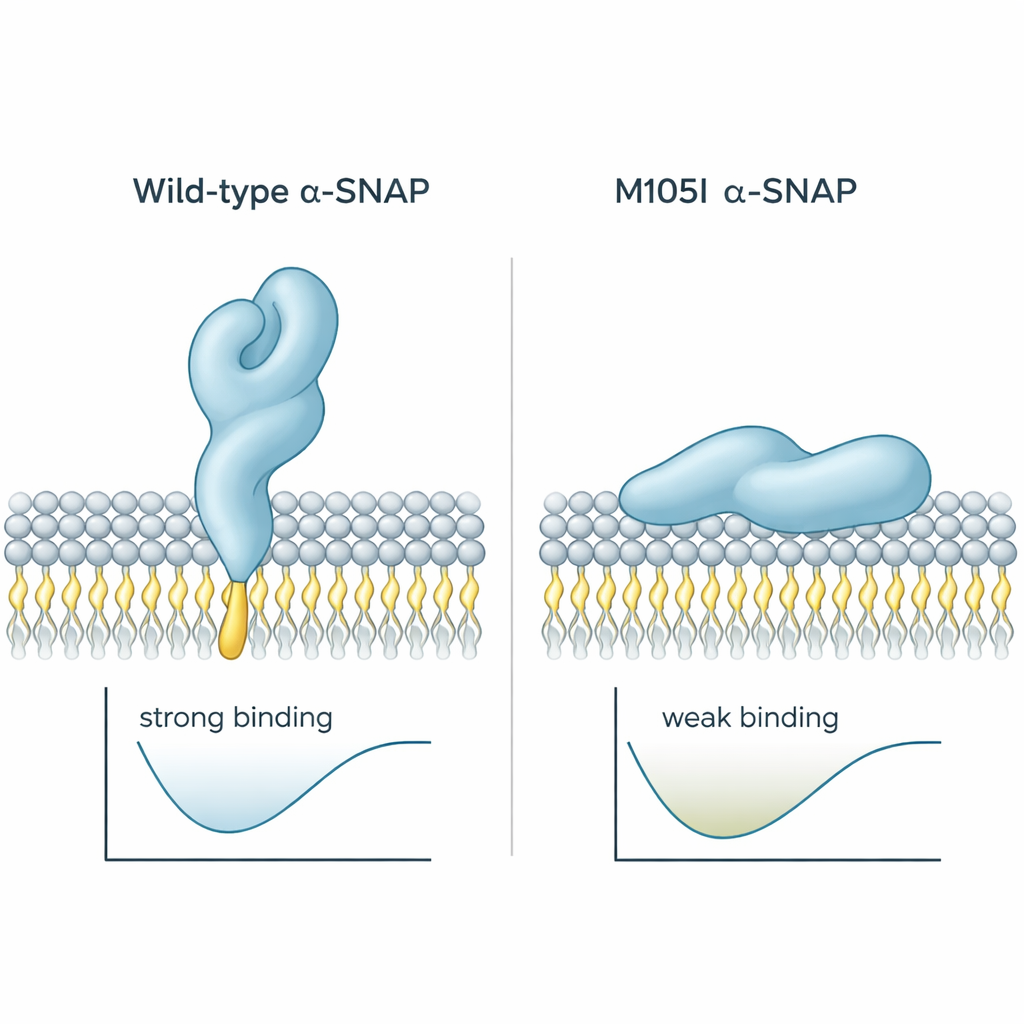
Varför detta är viktigt för sjukdom
Sammantaget visar arbetet att M105I-mutationen gör mer än att bara sänka mängden alpha-SNAP; den förändrar proteinets veckning så att dess viktiga membrangreppande snibb blir dold. Detta gör det svårare för alpha-SNAP att greppa plasmamembranet och anta rätt orientering för att organisera fusionsmaskineriet. I en utvecklande hjärna, där precision i leverans av signaler och byggmaterial till cellens yta är avgörande, bidrar denna subtila strukturella defekt sannolikt till hydrocefalus, felkopplad cortex och andra defekter som ses hos hyh-möss. För icke-specialister är budskapet tydligt: även en liten förändring i formen på ett enskilt protein kan omforma hur celler kommunicerar och därigenom hur en hjärna byggs.
Citering: Méndez-Ruette, M., Bedoya, M., Hinrichsen, B. et al. A pathogenic mutation in α-SNAP impairs membrane lipid binding by concealing a critical hydrophobic loop. Commun Biol 9, 294 (2026). https://doi.org/10.1038/s42003-026-09578-y
Nyckelord: alpha-SNAP, membranbindning, proteinmutation, hjärnans utveckling, vesikelfusion