Clear Sky Science · sv
Utveckling av capsaicin‑härledda prohibitin‑ligander för att modulera interaktionen mellan Aurora kinase A/PHB2 och mitofagi i cancerceller
Varför en kemisk förening från chilipeppar spelar roll för cancer
Chilipeppar får sin hetta från capsaicin, en liten molekyl som binder till proteiner i våra celler. Denna studie utforskar en oväntad vändning av den välkända kryddan: forskarna omdesignade capsaicin för att skapa nya läkemedelsliknande molekyler som riktar in sig på cancercellernas ”kraftverk” — mitokondrierna — och dämpar en process som dessa celler använder för att hålla sina energifabriker i gott skick. Eftersom cancerceller i hög grad förlitar sig på effektiva mitokondrier för att driva sin okontrollerade tillväxt, kan förmågan att selektivt störa detta understödssystem öppna en ny väg för antitumörbehandlingar.
Cellernas kraftverk och deras interna städpatrull
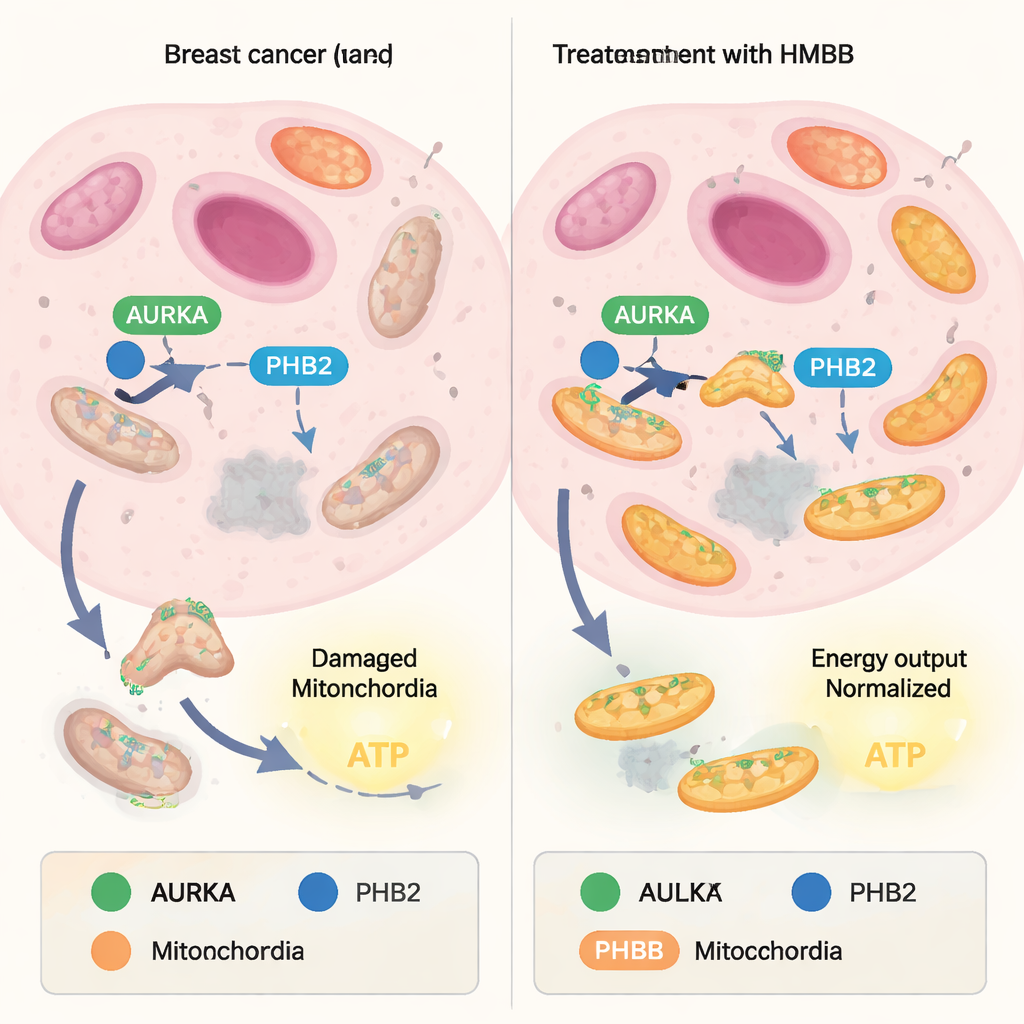
Mitokondrier balanserar ständigt mellan att bygga nya enheter och att återvinna skadade. Återvinningssidan, kallad mitofagi, fungerar som ett kvalitetskontrollsystem: utslitna mitokondrier märks ut och bryts ner, medan friskare behålls. Många cancerceller kapar denna balans och använder mitofagin för att rensa bort svaga mitokondrier och berika sig på ”superpresterare” som producerar stora mängder ATP, cellens energivaluta. Ett protein kallat Aurora kinase A (AURKA), som ofta överproduceras i tumörer, hittades nyligen inne i mitokondrier där det samarbetar med ett annat protein, Prohibitin‑2 (PHB2), och autofagiadaptern LC3. Tillsammans bildar de ett komplex som driver mitofagi och stödjer hög energiproduktion i cancerceller.
Från kryddig capsaicin till skräddarsydda molekylverktyg
Tidigare arbete visade att en naturförening kallad xanthohumol kan binda till PHB2 och störa AURKA–PHB2–LC3‑komplexet, blockera mitofagi och dämpa mitokondriell ATP‑produktion. Xanthohumols kemiska struktur är dock inte idealisk för läkemedelsutveckling. I denna studie vände sig författarna till capsaicin, en annan naturlig PHB‑ligand, och undersökte om den kunde omformas till mer praktiska verktyg. De bekräftade först att capsaicin svagt försvagar interaktionen mellan AURKA och PHB2 i levande bröstcancerceller, med en bildteknik (FRET/FLIM) som mäter hur nära två märkta proteiner sitter intill varandra. De syntetiserade sedan 16 capsaicin‑inspirerade molekyler genom att modifiera ”svansen” och den aromatiska ”huvudstrukturen” av den ursprungliga molekylen och testade systematiskt hur varje variant påverkade AURKA–PHB2‑partnerskapet inne i mitokondrierna.
Upptäckten av ett molekylärt ’lim’ som låser proteinerna samman
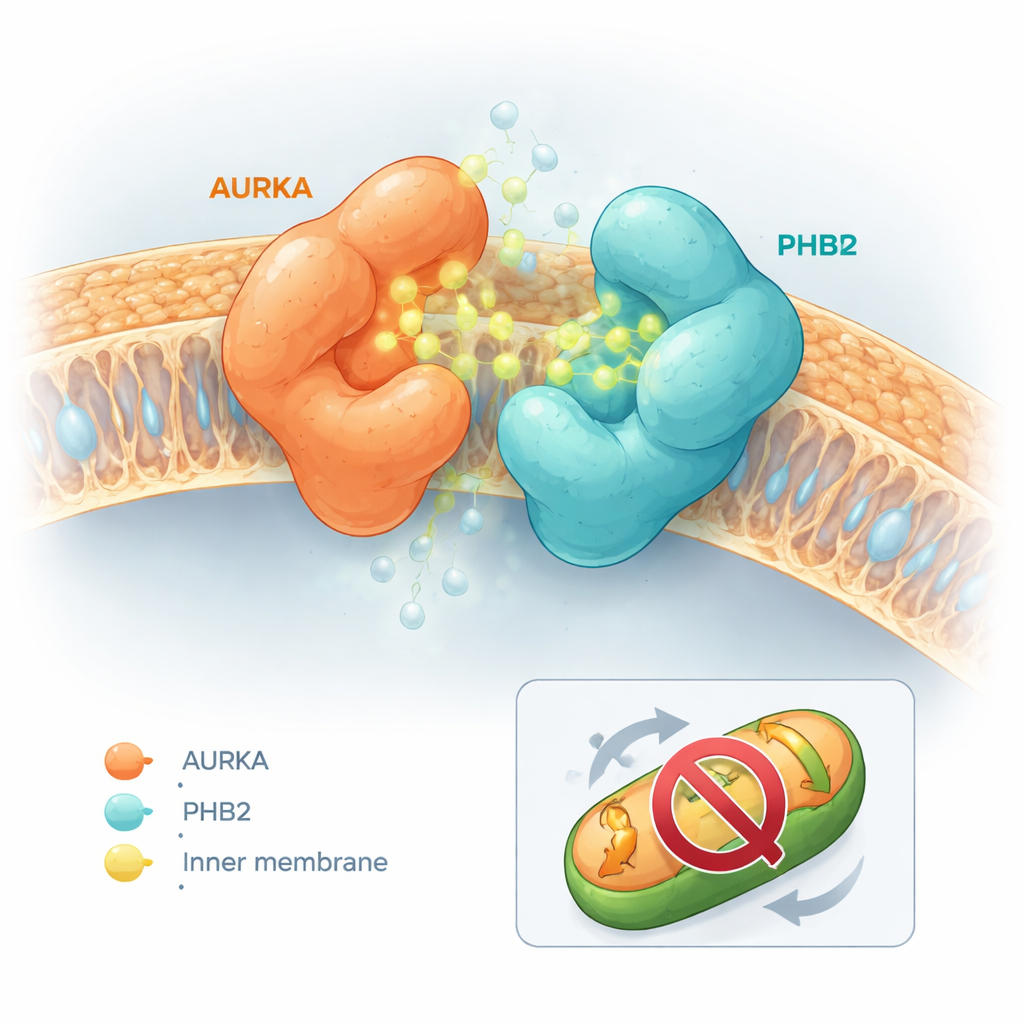
De modifierade molekylerna hade slående olika effekter. Vissa, som capsaicin självt eller ett derivat kallat förening 5, fick AURKA och PHB2 att separera lättare. Andra gjorde nästan ingenting. En delmängd — särskilt en molekyl benämnd förening 13, senare kallad HMBB — hade motsatt effekt och förtätade bindningen mellan AURKA och PHB2 avsevärt. Datorbaserade dockningssimulationer bidrog till att förklara detta beteende. Capsaicin och förening 5 tenderade att kila in i AURKA:s aktiva säte på sätt som skapade fysiska kollisioner med PHB2 och puttade de två proteinerna isär. I kontrast lade sig föreningarna 12 och 13 i AURKA:s aktiva säte och kontaktade samtidigt en känd inhibitorisk ficka på PHB2 utan att orsaka krockar. Istället tillät deras form dem att fungera som ett ”molekylärt lim” som förmedlade kontakt mellan AURKA och PHB2 och stabiliserade komplexet.
Blockera mitokondriell städning utan att stänga ner cellens kontrollcenter
En avgörande fråga var om detta molekylära lim helt enkelt inaktiverade AURKA i hela cellen — vilket skulle innebära risk för omfattande biverkningar — eller om det verkade mer selektivt. Med hjälp av en separat fluorescerande biosensor som rapporterar om AURKA‑aktivering vid centrosomerna — strukturerna som organiserar cellens delningsmaskineri — observerade forskarlaget att HMBB inte dämpade AURKA‑aktivitet på dessa platser. Men i mitokondriella analyser vände HMBB förlusten av mitokondriell massa som normalt orsakas av AURKA‑överuttryck i bröstcancerceller. I celler som naturligt producerar höga nivåer av AURKA ökade HMBB mitokondrieinnehållet, vilket indikerar att AURKA‑driven mitofagi blockerades. I celler med låga AURKA‑nivåer hade HMBB liten effekt, vilket understryker dess beroende av AURKA–PHB2‑vägen.
Vad detta kan innebära för framtida cancerbehandlingar
Sammantaget visar resultaten att noggrant designade capsaicin‑derivat kan finjustera hur AURKA och PHB2 interagerar i mitokondrier. Genom att fungera som molekylärt lim låser HMBB och besläktade föreningar AURKA och PHB2 i en konfiguration som förhindrar det normala mitofagiprogrammet från att fortgå, utan att slå ut AURKA:s viktiga roller på andra platser i cellen. För en allmän läsare är huvudidén att författarna har skapat prototypmolekyler som selektivt stör hur cancerceller håller sina kraftverk i toppskick, vilket potentiellt försvagar deras energiförsörjning samtidigt som normala cellfunktioner skonas. Även om dessa föreningar fortfarande befinner sig i ett tidigt laboratoriumskede, illustrerar de en lovande strategi: att använda små, läkemedelsliknande molekyler för att rikta in sig på specifika proteinpartnerskap inne i mitokondrierna och därigenom underminera de metabola fördelar som många tumörer är beroende av.
Citering: Djehal, A., Caron, C., Giordano, D. et al. Development of capsaicin-derived prohibitin ligands to modulate the Aurora kinase A/PHB2 interaction and mitophagy in cancer cells. Commun Biol 9, 320 (2026). https://doi.org/10.1038/s42003-026-09573-3
Nyckelord: mitokondrier, mitofagi, Aurora kinase A, capsaicin‑derivat, cancermetabolism