Clear Sky Science · sv
Funktionell omprogrammering av iNKT‑celler av sulfatid‑reaktiva typ II NKT‑celler omprogrammerar alveolära makrofager för att lindra lung‑ischemireperfusionsskada
Varför det är viktigt att skydda donatorlungor
När kirurger transplanterar en lunga eller återställer blodflödet efter en blockering kan den plötsliga återkomsten av syre paradoxalt nog skada vävnaden. Detta problem, kallat lung‑ischemireperfusionsskada, är en viktig orsak till tidigt avslag efter lungtransplantation och andra kritiska ingrepp. Den här studien undersöker hur en ovanlig uppsättning immunceller kan ”omprogrammeras” för att dämpa inflammation, vilket ger en möjlig ny metod för att skydda sårbara lungor när de behövs som mest.
Immunceller som kan hela eller skada
Våra lungor patrulleras av alveolära makrofager, immunceller som sitter i luftblåsorna och reagerar snabbt på fara. Dessa celler kan växla mellan två huvudlägen. I ett ”kamp”läge (ofta kallat M1) släpper de ut inflammatoriska ämnen som hjälper till att döda bakterier men som också kan skada vävnad. I ett ”reparations”läge (ofta kallat M2) frigör de lugnande molekyler som begränsar inflammation och främjar läkning. Vid lung‑ischemireperfusionsskada skjuts balansen mot det skadliga kamp‑läget. Forskarna antog att om de kunde försiktigt styra makrofager mot reparationsläget vid rätt tidpunkt, skulle de kunna mildra skadans omfattning.
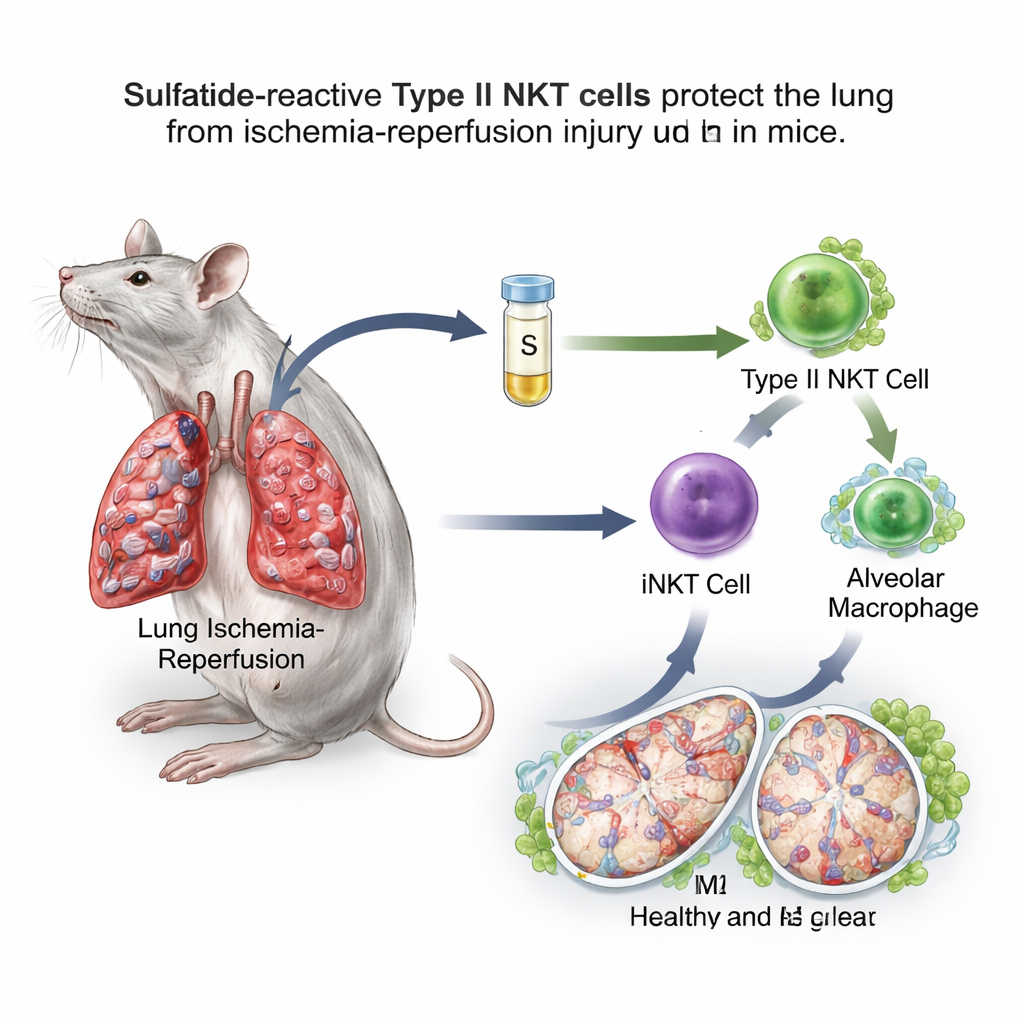
En socker–fettmolekyl vänder en immunbrytare
Teamet fokuserade på natural killer T (NKT)‑celler, ovanliga immunceller som ligger mellan snabbverkande medfödda försvar och långsammare, målinriktade svar. NKT‑celler finns i två huvudtyper. Typ I, även kallade invariant NKT (iNKT)‑celler, är kända för att förvärra lung‑ischemireperfusionsskada hos möss. Typ II NKT‑celler kan däremot dämpa immunsvar i andra organ. En fet molekyl som kallas sulfatid känns igen specifikt av typ II NKT‑celler. I en musmodell där blodflödet till en lunga klämdes av i en timme och sedan återställdes gav forskarna sulfatid flera timmar före skadan. De fann att sulfatidbehandlade möss hade mindre lungsvullnad, färre läckande blodkärl, lägre oxidativ stress, bättre syresättning och reducerade inflammatoriska ämnen i lungsköljvätska jämfört med obehandlade djur.
Omprogrammering av makrofager genom ett signalrelä
Närmare undersökning visade att sulfatid skiftade alveolära makrofager mot det reparationsinriktade M2‑tillståndet. Dessa makrofager visade fler ytmolekyler och gener kopplade till läkning och var bättre på att dämpa inflammation när de överfördes till andra möss. När forskarna selektivt avlägsnade alveolära makrofager förvärrades lungskadan och sulfatid förlorade i stor utsträckning sin skyddande effekt, vilket visar att dessa celler är en avgörande knutpunkt i vägen. Viktigt är att sulfatids fördel försvann i möss som saknade antingen typ II NKT‑celler eller typ I iNKT‑celler, och den kunde återställas genom att återföra iNKT‑celler som tidigare exponerats för sulfatid. Tillsammans avslöjade dessa experiment ett relä: sulfatid aktiverar typ II NKT‑celler, som i sin tur omformar iNKT‑cellernas beteende, och dessa omprogrammerar de alveolära makrofagerna.
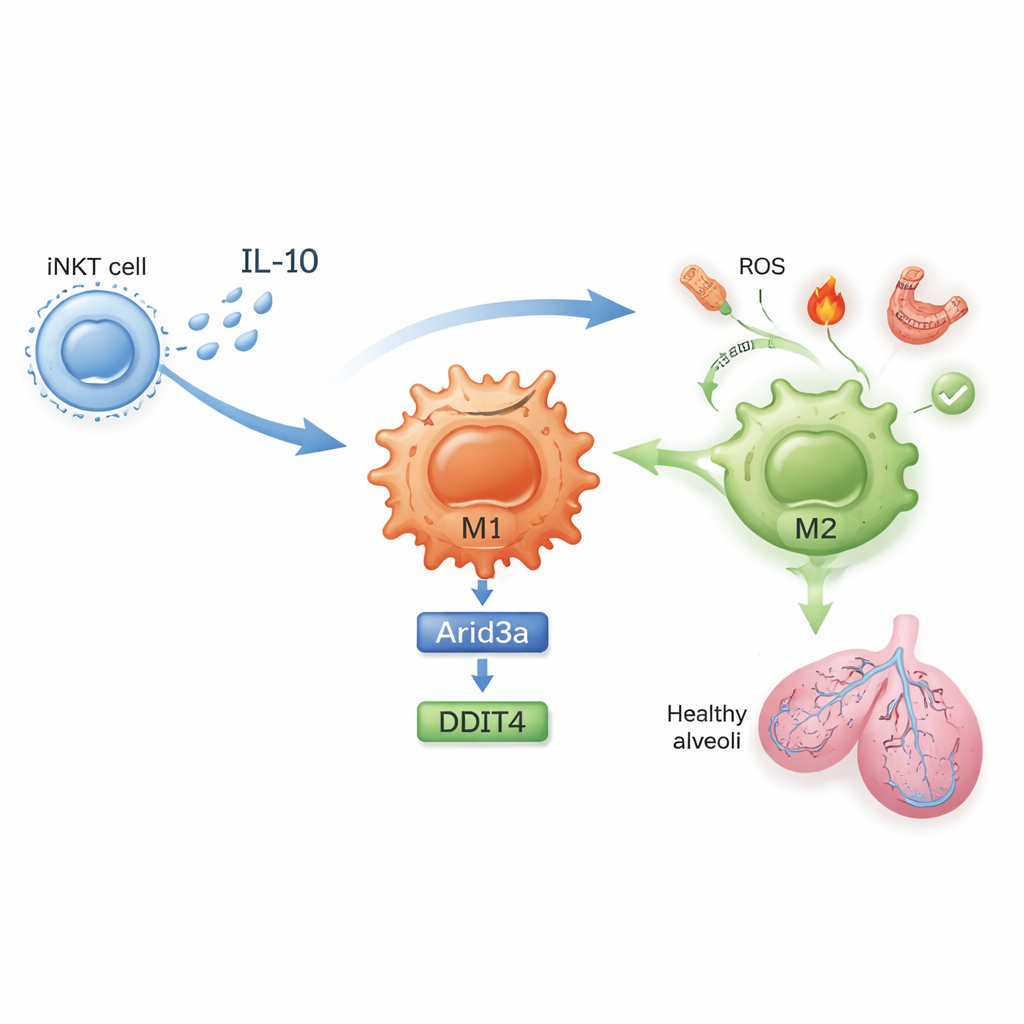
En molekylär kedja som lugnar inflammation
Vad förändras egentligen inne i dessa celler? I obehandlade möss prolifererade lung‑iNKT‑celler under ischemireperfusion och producerade höga nivåer interferon‑gamma, en kraftfull inflammatorisk signal. Efter sulfatidexponering producerade iNKT‑celler istället mer interleukin‑10 (IL‑10), en stark antiinflammatorisk molekyl, och mindre interferon‑gamma. Studien visar att IL‑10 från iNKT‑celler verkar direkt på makrofager för att driva deras M2‑polarisering. Genom genuttrycksprofilering och noggrant utformade cellkulturförsök identifierade författarna en molekylär kedja inne i makrofager: IL‑10 ökar en transkriptionsfaktor kallad Arid3a, som i sin tur höjer uttrycket av en stressresponsgen benämnd DDIT4. Denna Arid3a–DDIT4‑axel hjälper till att stänga av en tillväxtkontrollväg som annars håller makrofager i ett inflammatoriskt tillstånd, och styr dem mot det skyddande M2‑programmet.
Från muslungor till framtida behandlingar
För att testa hur central denna molekylära kedja är använde forskarna små interfererande RNA för att tysta Arid3a eller DDIT4 i makrofager innan de överförde dem till möss. När någon av generna slogs ned drev sulfatid inte längre makrofager helt in i reparationsläget och lungskyddet försvagades. Ytterligare analys tyder på att ett signalprotein kallat YES1 hjälper sulfatid‑aktiverade typ II NKT‑celler att koppla om iNKT‑celler mot IL‑10‑produktion. Även om dessa fynd kommer från musmodeller och från manipulerade celler i labbet, målar de upp en tydlig berättelse: genom att kortvarigt aktivera en specifik NKT‑cellssubtyp med sulfatid kan man möjligen omvandla annars skadliga immunsvar till sådana som skyddar transplanterade eller skadade lungor. I framtiden skulle läkemedel som imiterar denna bana kunna hjälpa fler patienter att överleva och återhämta sig efter livräddande lungingrepp.
Citering: Li, Q., Yin, J., Lin, Q. et al. Functional remodeling of iNKT cells by sulfatide-reactive type II NKT cells reprograms alveolar macrophages to alleviate lung ischemia-reperfusion injury. Commun Biol 9, 289 (2026). https://doi.org/10.1038/s42003-026-09572-4
Nyckelord: lungischemi reperfusionsskada, alveolära makrofager, natural killer T‑celler, interleukin‑10, immunmodulation