Clear Sky Science · sv
Omvärdering av Gα-protein–responselmentsspecificitet i GPCR‑signalering
Varför små cellomkopplare spelar roll för medicinen
Många av dagens läkemedel fungerar genom att växla molekylära ”omkopplare” på cellernas yta, så kallade G‑protein‑kopplade receptorer eller GPCR:er. Dessa omkopplare förmedlar budskap in i cellen via hjälpproteiner som kallas G‑proteiner och slutar så småningom med att gener slås på eller av. I årtionden har forskare förlitat sig på enkla ljusproducerande tester för att se vilka G‑proteiner en viss substans eller receptor använder. Denna studie ställer en grundläggande men avgörande fråga: talar dessa tester verkligen om för oss det vi tror — och kan vi lita på dem när vi utformar nästa generations precisionsläkemedel?
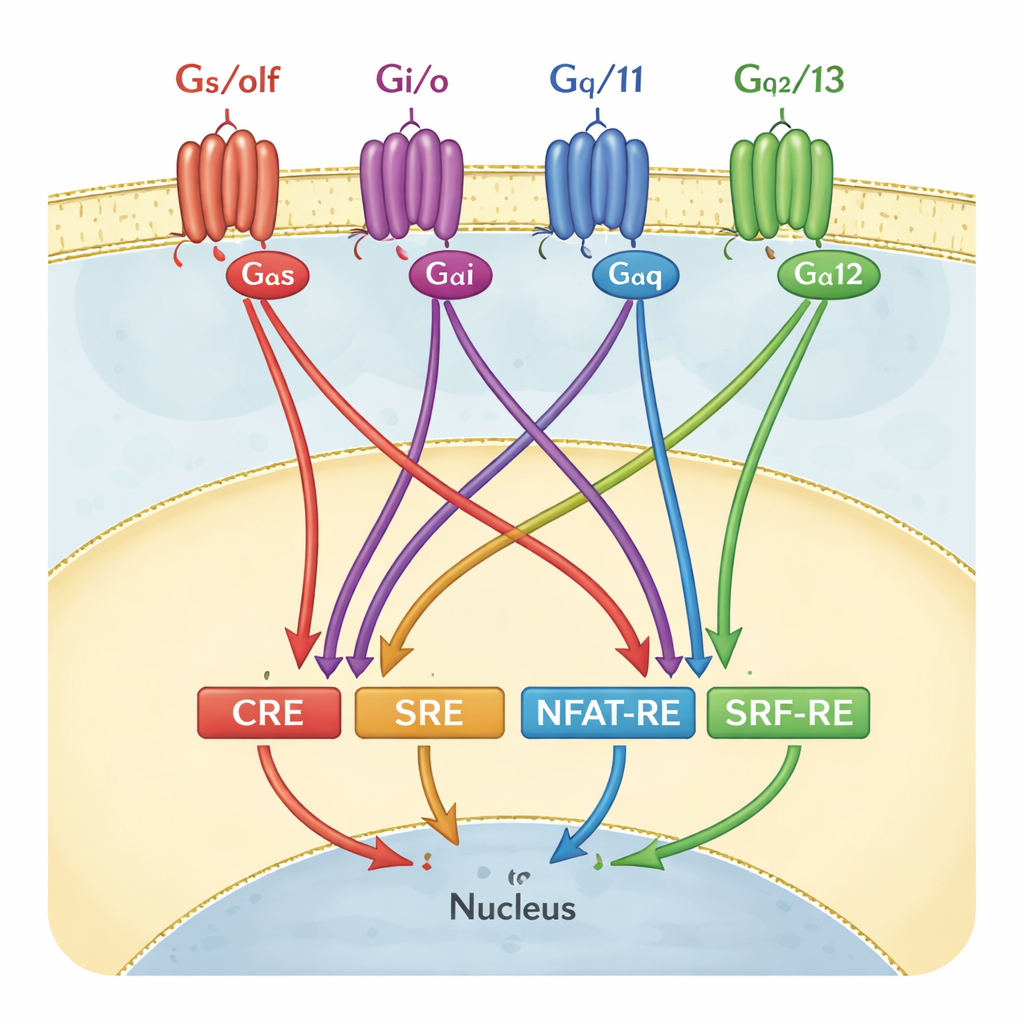
Hur forskare vanligtvis tolkar GPCR‑signaler
För att följa GPCR‑aktivitet använder många labb reporter‑genanalyser. I dessa tester konstrueras celler så att när en viss genswitch, eller ”respons-element”, aktiveras börjar cellerna att lysa. Fyra sådana element är särskilt vanliga: CRE, SRE, NFAT‑RE och SRF‑RE. Var och en har länge betraktats som en markör för en viss gren av G‑proteinsignalering — till exempel CRE för Gαs/olf‑familjen, eller SRF‑RE för Gα12/13. I läroböcker och screeningspipeline ritas dessa parningar ofta nästan som en‑till‑en‑kopplingar: aktivera ett specifikt G‑protein, och endast en reporter tänds.
Prövar den gamla kopplingsschemat
Författarna utmanade systematiskt denna bild med hjälp av humana HEK293‑celler där specifika G‑proteinfamiljer — eller till och med alla G‑proteiner — tagits bort med genredigering. De återinförde sedan individuella G‑proteintyper en åt gången. I dessa celler uttryckte de nio olika GPCR:er, valda för att representera receptorer som antingen signalerar mycket selektivt eller genom många G‑proteinpartner. Genom att mäta hur starkt var och en av de fyra reporterna glödde över många läkemedelskoncentrationer kunde de se vilka G‑proteiner som verkligen krävdes för varje respons‑element och vilka som kunde bidra indirekt.
Överlappande vägar istället för rena kanaler
Resultaten kullkastar den prydliga en‑receptor‑en‑reporter‑modellen. Medan CRE fortfarande främst berodde på Gαs/olf‑proteiner — den klassiska cAMP‑ökande vägen — kunde andra G‑proteinfamiljer märkbart påverka CRE‑aktiviteten, men bara när Gαs/olf var närvarande. För de övriga tre reporterna, SRE, NFAT‑RE och SRF‑RE, framträdde Gαq/11‑familjen som huvuddrivare, även om SRE och SRF‑RE traditionellt förknippats med andra G‑proteingrenar. SRE och SRF‑RE uppvisade särskilt liknande beteenden, vilket tyder på att de utnyttjar delad nedströmsmaskineri snarare än separata, isolerade vägar. I många fall gavs ytterligare G‑proteiner såsom Gα12/13 och Gαi/o ett extra drag eller bakgrundsaktivitet, vilket framhäver ett nätverk av korsprat snarare än separata kanaler.
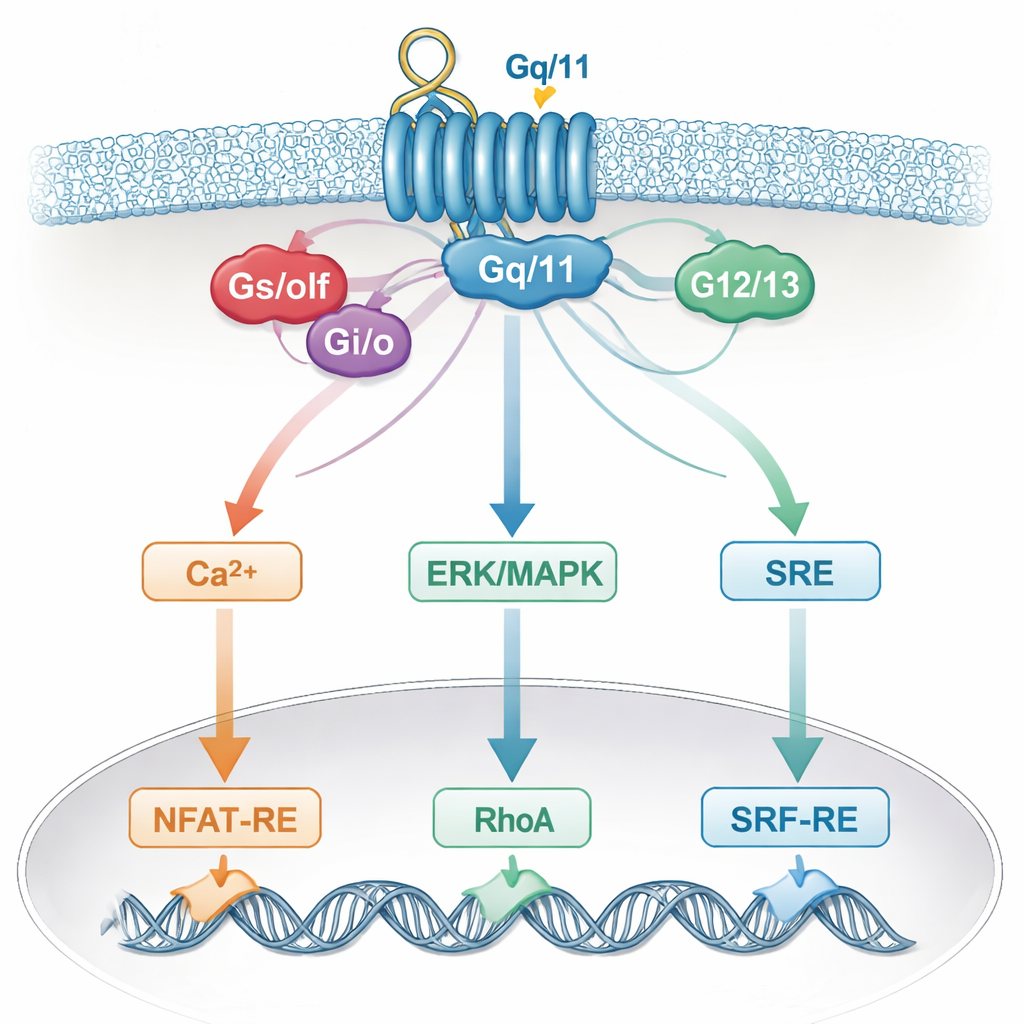
Varför cellens nätverk suddar ut våra avläsningar
Denna suddiga specificitet speglar sannolikt hur riktiga celler integrerar signaler. En enda receptor kan aktivera flera G‑proteiner, som sedan konvergerar på gemensamma budbärare som kalcium, ERK/MAPK, RhoA eller cAMP, och på delade hjälpare såsom Gβγ‑subenheter. Dessa gemensamma vägar går i sin tur in i samma genswitchar i kärnan. Följaktligen ”lyssnar” en reporter som troddes svara på en G‑proteinfamilj faktiskt på flera. Celltypsspecifika faktorer och den exakta uppsättningen receptorer som är närvarande tillför ännu mer komplexitet, vilket innebär att slutsatser dragna från ett cellsystem kanske inte gäller i ett annat.
Vad detta innebär för läkemedelsupptäckt
För icke‑specialister är huvudpoängen att många allmänt använda glow‑baserade GPCR‑tester är mindre specifika än vad deras etiketter antyder. De kan fortfarande berätta att en receptor är aktiv och grovt vilka breda vägar som är engagerade, men de är inte ett säkert bevis för att en viss G‑proteinfamilj — och endast den familjen — är involverad. Författarna menar att forskare och läkemedelsutvecklare bör betrakta dessa reporter‑tester som grova indikatorer och komplettera dem med mer direkta metoder som observerar proteininteraktioner i realtid. Det ger en sannare bild av hur potentiella läkemedel styr cellsignalering och hjälper till att undvika missvisande genvägar i jakten på säkrare, mer målinriktade terapier.
Citering: Saito, A., Kise, R., Yamaguchi, S. et al. Re-evaluating Gα protein–response element specificity in GPCR signaling. Commun Biol 9, 288 (2026). https://doi.org/10.1038/s42003-026-09569-z
Nyckelord: GPCR‑signalering, G‑proteiner, reporter‑analyser, cellsignaleringsnätverk, läkemedelsupptäckt