Clear Sky Science · sv
Cellbaserade och isoformspecifika G-proteinkopplade receptor-kinasassays för omfattande inhibitorutvärdering
Varför det spelar roll att skruva ner cellernas ”volymreglage”
Många av våra läkemedel fungerar genom att höja eller sänka aktiviteten hos cellmembranreceptorer som känner av hormoner, neurotransmittorer och droger. Dessa receptorer måste noggrant stängas av igen så att cellerna inte förblir överstimulerade, en process som delvis styrs av enzymer som kallas GRK:er. När GRK:er är för aktiva, som ses vid hjärtsvikt och vissa cancerformer, blir signaleringen störd. Denna studie utvecklar praktiska, cellbaserade tester för att mäta hur väl experimentella molekyler kan blockera specifika GRK:er, vilket hjälper forskare att designa smartare läkemedel som finjusterar dessa viktiga cellulära volymreglage.
Portvakter på cellens yta
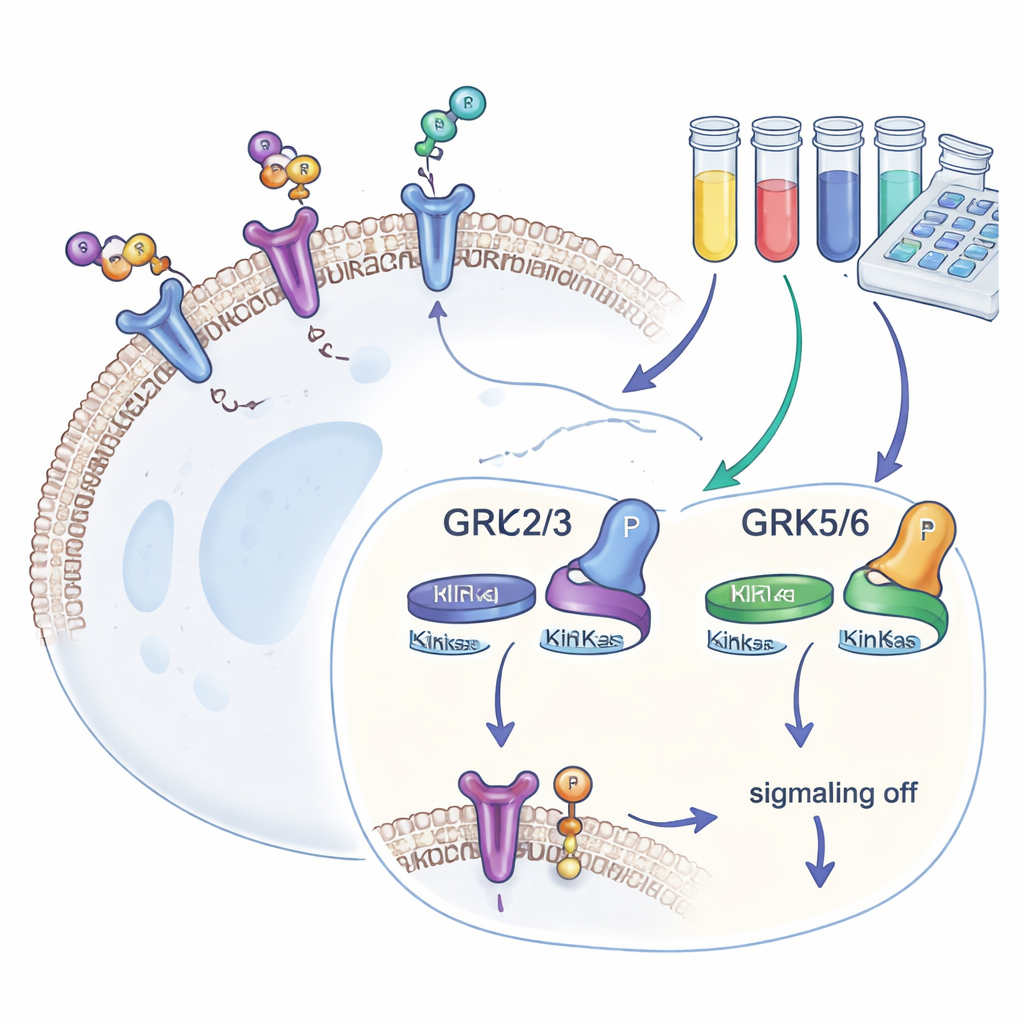
Våra celler bär på hundratals typer av G-proteinkopplade receptorer (GPCR), som upptäcker signaler utanför och översätter dem till interna svar. Efter att en GPCR aktiverats fäster GRK:er små fosfat-”flaggor” på dess svans. Dessa flaggor attraherar ett annat protein, beta-arrestin, som stoppar vidare signalering och ofta drar in receptorn i cellen. Fyra GRK-varianter—GRK2, GRK3, GRK5 och GRK6—finns i många vävnader. Eftersom de påverkar hur kraftigt GPCR:er svarar, och eftersom deras nivåer ändras vid sjukdomar som hjärtsvikt, cancer och beroende, är läkemedelsutvecklare angelägna om att hitta GRK-blockerare som både är potenta och selektiva.
Bygga en ren försöksplattform inuti celler
De flesta tidigare GRK-studier förlitade sig på datorbaserade modeller eller test-rörskemiska metoder, vilka visar hur tätt en hämmare kan binda men inte hur den presterar i en levande cells trånga inre. För att överbrygga detta gap konstruerade författarna humana HEK293-celler som saknar alla fyra vanliga GRK:er och återintroducerade sedan endast en GRK-isoform åt gången. Varje cellinje bar också en välstuderad receptor, beta-2-adrenerg receptor, märkt så att dess fosforylering vid en specifik svansplats (kallad T360/S364) kunde avläsas med en känslig antikroppsbaserad assay. Eftersom denna plats modifieras endast av GRK:er fungerar mängden fosfat som en direkt, kvantitativ måttstock på hur aktiv varje GRK-isoform är inne i levande celler.
Sortera de bra, svaga och icke-specifika
Med detta verktygstestkit utvärderade teamet en panel av kommersiellt tillgängliga GRK-hämmare. De grupperade först föreningar som huvudsakligen riktar sig mot GRK2 och GRK3, och en annan uppsättning riktad mot GRK5 och GRK6. Genom att jämföra hur mycket varje molekyl minskade receptorfosforylering i celler som uttryckte endast en GRK-subtyp kunde de kartlägga selektivitet i verkliga förhållanden. En förening, kallad 8h, framträdde som den mest potenta hämmaren av GRK2/3, medan förening 18 utmärkte sig genom att selektivt hämma GRK5/6. Vissa allmänt använda molekyler visade liten effekt vid de testade doserna, sannolikt eftersom de inte trängde in i cellerna effektivt, och en mycket kraftfull kovalent hämmare störde cellhälsan och var olämplig för avbildningsexperiment.
Från kemiska fingeravtryck till receptorbeteende
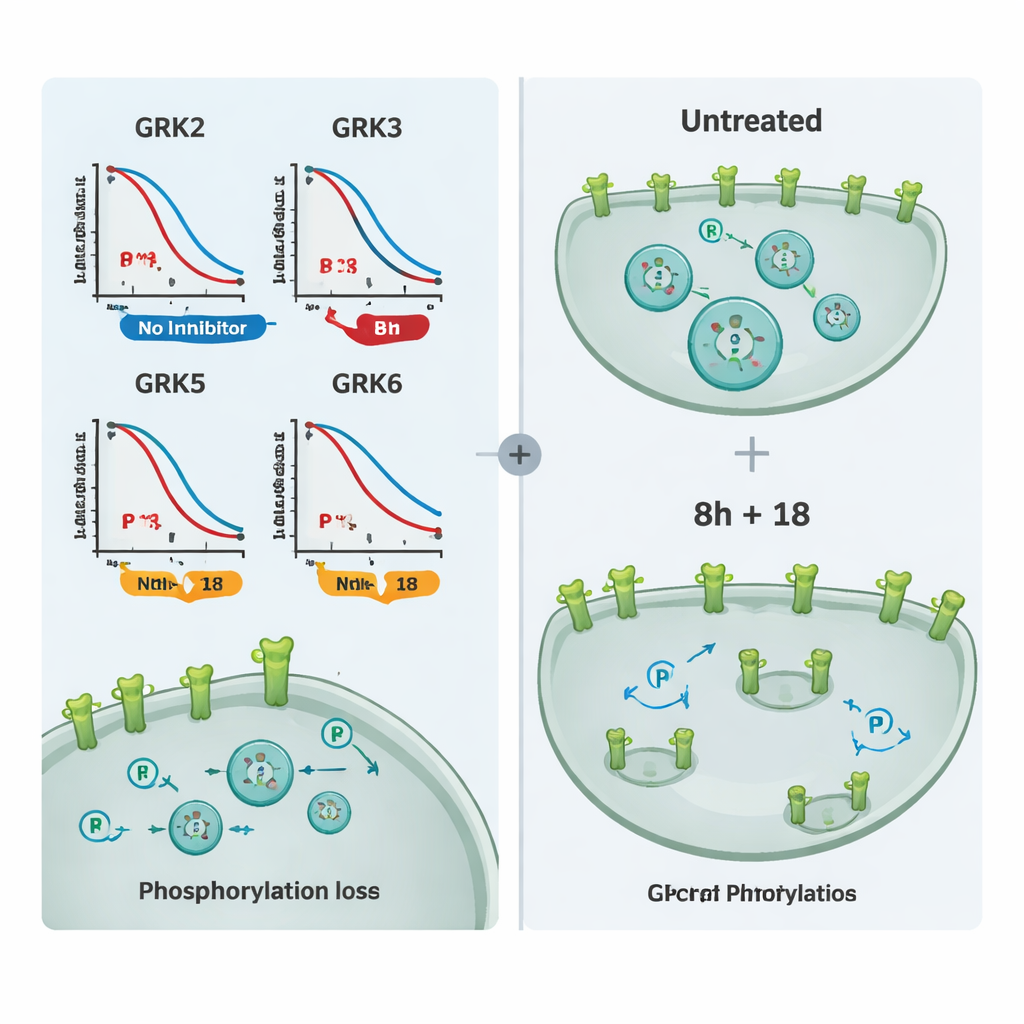
För att visa att dessa hämmare påverkar inte bara en testreceptor utan GPCR-biologi mer allmänt undersökte författarna flera medicinskt viktiga receptorer, inklusive mu-opioidreceptorn och vasopressin V2-receptorn. De mätte både fosforylering och receptorinternalisering med mikroskopi. Förening 8h eller 18 ensam reducerade delvis fosforylering och den inåtriktade rörelsen av receptorer för många mål, men kombinationen av 8h och 18 förhindrade nästan helt dessa förändringar och höll receptorerna på cellytan. Ytterligare experiment som följde rekrytering av beta-arrestin bekräftade att samma föreningar kunde justera signaleringen vid andra receptorer som regleras av överlappande uppsättningar av GRK:er.
Vad detta betyder för framtida läkemedel
För icke-specialister är huvudbudskapet att studien levererar en tillförlitlig uppsättning cellbaserade tester—och två särskilt användbara verktygsföreningar, 8h och 18—som låter forskare se, i levande celler, exakt hur olika GRK-isoformer skruvas ner. Istället för att gissa utifrån förenklade test-rörsdata kan forskare nu jämföra kandidat-hämmare sida vid sida och avgöra om de främst påverkar GRK2/3, GRK5/6 eller alla fyra samtidigt. Denna klarhet bör snabba på utvecklingen av läkemedel som mer precist modulerar GPCR-signalering, med potentiella fördelar för behandling av hjärtsjukdom, cancer, smärttillstånd och andra tillstånd där signalbalansen har rubbats.
Citering: Blum, N.K., Kiefer, M.C., Decker, A. et al. Cell-based and isoform-selective G protein-coupled receptor kinase assays for comprehensive inhibitor evaluation. Commun Biol 9, 287 (2026). https://doi.org/10.1038/s42003-026-09568-0
Nyckelord: GPCR-signalering, GRK-hämmare, beta-adrenerg receptor, cellbaserad assay, läkemedelsupptäckt