Clear Sky Science · sv
HBP1 förstärker progesteronreceptoraktivitet och IGFBP1-uttryck som driver endometriell decidualisering
Varför detta är viktigt för fertilitet
När en graviditet börjar kan embryot bara fästa i livmodern om slemhinnan genomgått en viktig omvandling som kallas decidualisering. Många fall av infertilitet och upprepade misslyckanden vid embryotransfer förblir oklara, och en växande mängd bevis tyder på att något går fel i denna omvandling snarare än i embryot självt. Denna studie avslöjar en tidigare underskattad molekylär "omkopplare", en transkriptionsfaktor kallad HBP1, som hjälper till att förbereda livmoderslemhinnan för implantation och kan erbjuda nya sätt att diagnostisera och behandla implantationsproblem.
En dold omkopplare i livmoderslemhinnan
Den inre slemhinnan i livmodern, endometriet, förändras regelbundet under varje menstruationscykel. Under östrogenets inflytande växer det, och under progesteron mognar det till en mottaglig bädd för ett embryo. I detta arbete fokuserade forskarna på humana endometriella stromaceller, de strukturella cellerna som omvandlas till större, mer sekretoriska deciduala celler vid implantation. Genom att granska befintliga data om genaktivitet och utföra nya experiment fann de att HBP1-nivåerna stiger kraftigt när dessa stromaceller börjar decidualisera, vilket tyder på att HBP1 är en del av det inbyggda tidssystemet som gör livmodern redo.
Hjälper celler att ändra form och sakta ner
För att testa om HBP1 bara är närvarande eller verkligen nödvändig justerade teamet dess nivåer uppåt och nedåt i odlade humana endometriella stromaceller. När HBP1 minskades sjönk klassiska markörer för decidualisering som IGFBP1, FOXO1 och prolaktin både på RNA- och protein-nivå. Cellerna misslyckades också med att genomgå den typiska formförändringen från smala, spindelliknande celler till bredare, polygonala celler och fortsatte i stället att proliferera. När HBP1 ökades steg IGFBP1-nivåerna och celldelningen avtog. Tillsammans visar dessa fynd att HBP1 hjälper celler att lämna tillväxtläget och gå in i det specialiserade deciduala tillståndet som stöder tidig graviditet.
Finjusterar hormonsignaler inne i cellen
Progesteron och dess receptor är centrala för att förbereda livmodern, men inte alla vävnader svarar lika bra på hormonet. Forskarna upptäckte att progesteronsignalering i sig ökar HBP1-nivåerna, vilket skapar en positiv återkopplingsslinga. Slående nog förändrade inte sänkning av HBP1 hur mycket progesteronreceptor cellerna bildade, men det dämpade aktiviteten hos viktiga progesteronresponsiva gener, inklusive FKBP4, FKBP5, FOSL2 och koaktivatorn SRC1. Med hjälp av genometomfattande metoder visade de att HBP1 binder nära många av dessa gener och är associerat med en ökning av en specifik histonmarkör, H3K4me3, som flaggar DNA som aktivt. I praktiken slår HBP1 inte på eller av receptorn; den gör receptorens målgener lättare att läsa av.
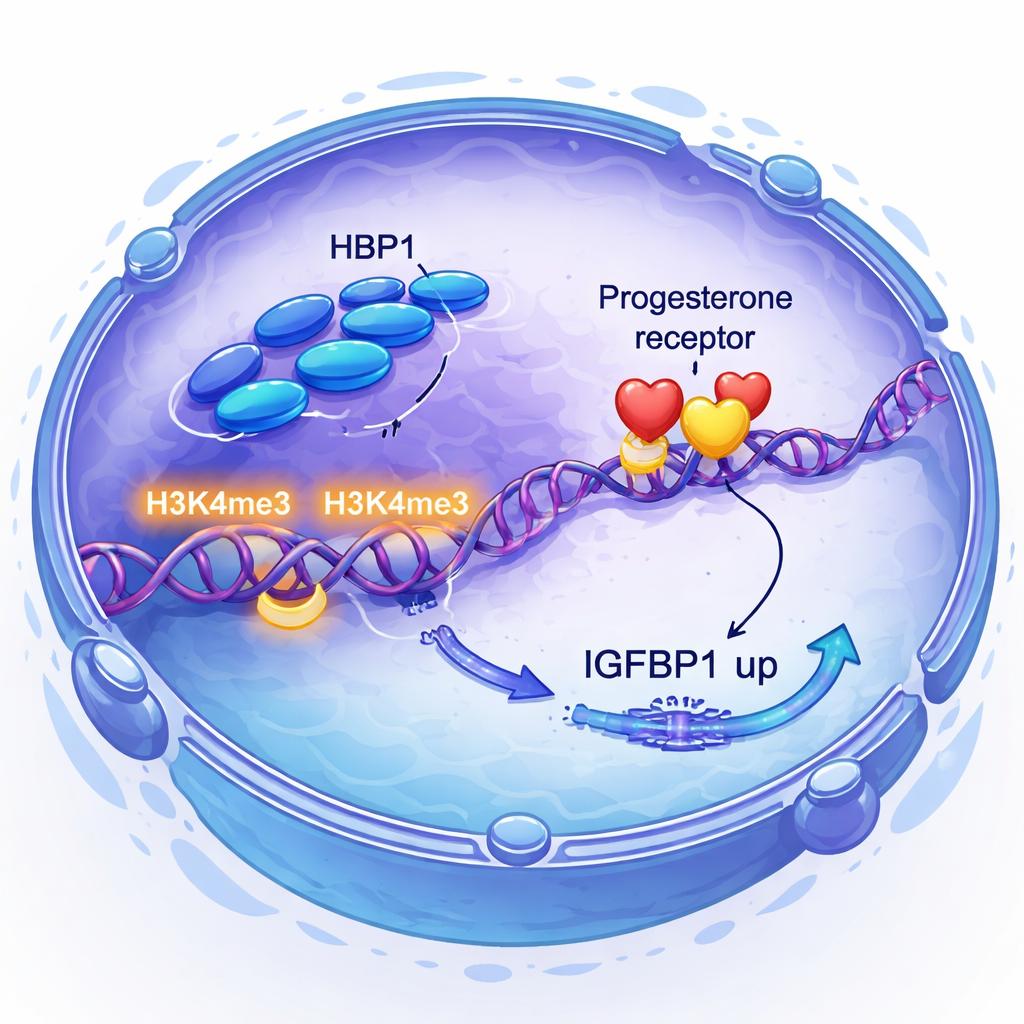
Direkt kontroll över en nyckelsignal för implantation
Teamet frågade sedan hur HBP1 kopplar till IGFBP1, ett protein som länge används som markör för frisk decidualisering och som är känt för att påverka kommunikationen mellan embryo och livmoder. Genom att kombinera RNA-sekvensering med kromatinimmunoprecipiteringssekvensering visade de att HBP1 sitter direkt på IGFBP1:s promotorregion och ökar H3K4me3 där, vilket driver ett högre IGFBP1-produktion. De fann också att minskning av HBP1 aktiverade PI3K–AKT-vägen, en tillväxtrelaterad signal som, när den är överaktiv, undertrycker IGFBP1. Blockering av denna väg återställde IGFBP1-nivåerna. Således stödjer HBP1 decidualisering på två sätt: genom att direkt aktivera IGFBP1 och genom att dämpa en tillväxtsignal som annars skulle hålla tillbaka deciduala gener.
Koppla ett molekylärt fel till misslyckad implantation
Slutligen undersökte forskarna endometriella prover från kvinnor som upplevt upprepade implantationsmisslyckanden och jämförde dem med vävnader från fertila kontrollpersoner under den mid-sekretoriska, implantationsberedda fasen. Kvinnor med upprepade misslyckanden hade märkbar lägre nivåer av HBP1 och dess nedströms-partners IGFBP1, FKBP5 och FOSL2, även om nivåerna av progesteronreceptor var likartade mellan grupperna. Detta mönster stämmer överens med idén om "progesteronresistens"—hormonet är närvarande, men vävnaden kan inte uppvisa ett fullständigt svar eftersom nyckelfaktorer som HBP1 saknas.
Vad detta betyder för patienter
Enkelt uttryckt antyder denna studie att HBP1 fungerar som en huvudinställning på kontrollpanelen för livmoderslemhinnan. När den är korrekt uppreglerad hjälper den progesteronsignaler att höras, uppmuntrar celler att sluta dela sig och specialisera sig, och ökar produktionen av implantationsvänliga molekyler som IGFBP1. När HBP1 är för låg kan slemhinnan se normal ut i mikroskopet men fungera dåligt, vilket leder till att embryon helt enkelt inte kan få fotfäste. Att förstå och mäta HBP1 och dess nätverk kan i framtiden hjälpa läkare att identifiera kvinnor i riskzonen för implantationsproblem och inspirera till nya behandlingar som återställer livmoderns mottaglighet.
Citering: Guo, Y., Tian, W., Nie, C. et al. HBP1 enhances progesterone receptor activity and IGFBP1 expression driving endometrial decidualization. Commun Biol 9, 286 (2026). https://doi.org/10.1038/s42003-026-09567-1
Nyckelord: endometrial decidualisering, embryoimplantation, progesteronsignalering, infertilitet, HBP1