Clear Sky Science · sv
Differentierad GABA-dynamik över hjärnans funktionella nätverk vid autism
Varför denna hjärnstudie är viktig
Många personer på autismspektrumet beskriver världen som överväldigande, där ljud, ljus och känslor upplevs som för intensiva eller märkligt dämpade. Forskare misstänker att en del av förklaringen ligger i hur hjärnceller balanserar «gå»- och «stanna»-signaler. Denna studie undersöker en nyckelkemikalie för «stopp», GABA, och ställer en praktisk fråga: hur svarar den autistiska hjärnan när vi stimulerar detta system med ett läkemedel? Svaret kan hjälpa till att förklara varför vissa mediciner ger oförutsägbara effekter vid autism och varför det är så svårt att hitta rätt dos.
Signaler som håller hjärnaktiviteten i balans
Våra hjärnor drivs av en ständig dragkamp mellan excitation (neuroner som avfyrar) och hämning (neuroner som dämpar aktiviteten). GABA är den huvudsakliga kemiska bromsen. Vid autism tyder flera års forskning på att denna balans är rubbad, särskilt i de hjärnsystem som hanterar sensorisk information som syn, hörsel och beröring. Men tidigare arbete har oftast varit statiskt: man har mätt hjärnans kemi eller struktur i vila och jämfört autistiska och icke-autistiska personer. Det som har saknats är ett dynamiskt test av hur GABA-systemet faktiskt reagerar när det pressas av ett läkemedel, särskilt över de storskaliga nätverk som stöder sensation, rörelse, uppmärksamhet och känslor.
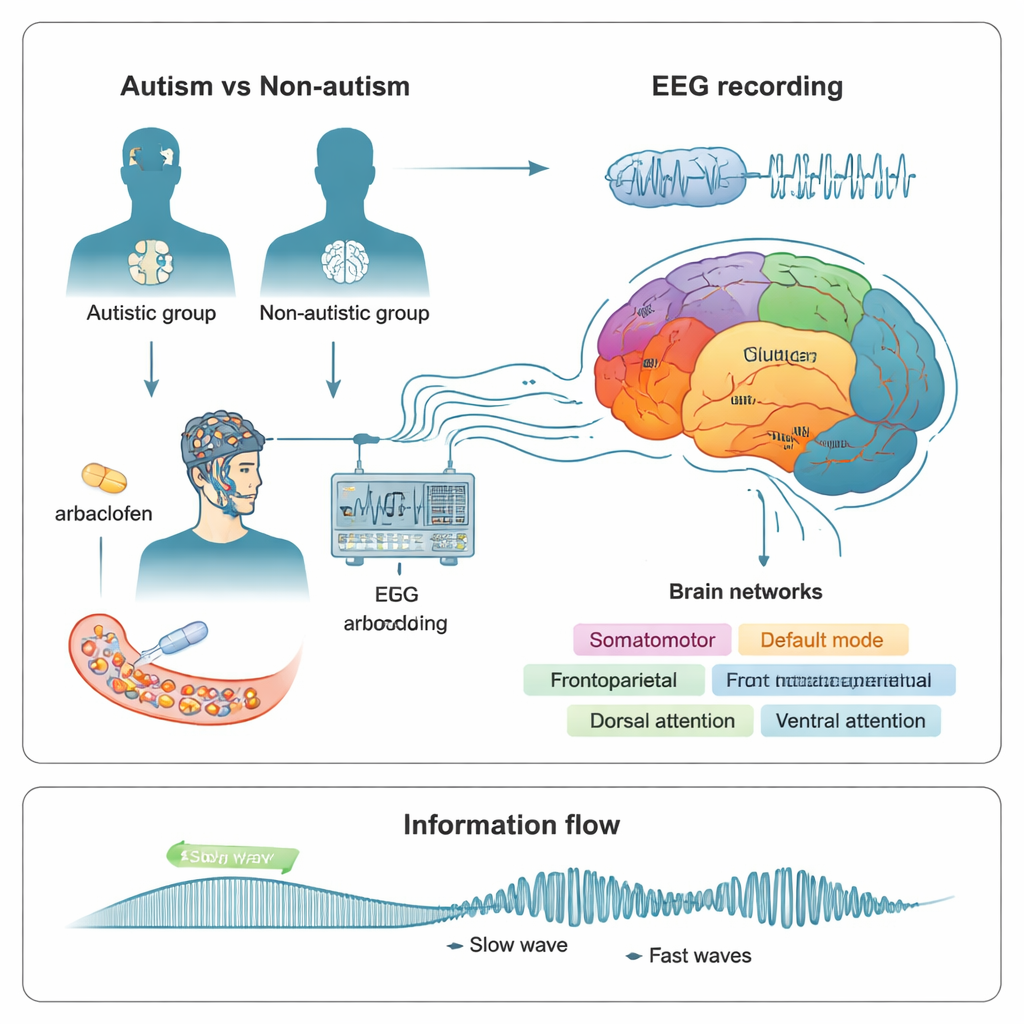
Lyssna på hjärnans rytmer
För att undersöka detta spelade forskarna in vilande hjärnaktivitet med EEG, som mäter mycket svaga elektriska signaler från skalpen. De studerade 24 icke-autistiska vuxna och 15 autistiska vuxna vid flera besök. Vid varje tillfälle svalde deltagarna antingen placebo eller en av två doser (15 mg eller 30 mg) arbaclofen, ett läkemedel som aktiverar en specifik typ av GABA-receptor kallad GABAB. Cirka tre timmar senare, när läkemedlet var verksamt, spelade teamet in EEG med öppna och stängda ögon och använde datormodeller för att spåra signalerna tillbaka till 400 platser över cortex. Dessa platser grupperades sedan i sju större funktionella nätverk, inklusive visuellt, somatomotoriskt (rörelse och beröring), limbiskt (känslor och minne) och flera nätverk för högre kognitiva processer och uppmärksamhet.
Hur långsamma och snabba hjärnvågor kommunicerar
I stället för att enbart titta på hur starka vissa hjärnvågor var, fokuserade teamet på hur olika frekvenser samverkar. I friska hjärnor hjälper långsamma vågor som sträcker sig över stora områden ofta till att koordinera snabbare, mer lokala burstar av aktivitet. Denna interaktion, kallad fas–amplitud-koppling, kan ses som en långsam rytm som öppnar och stänger «fönster» där snabb aktivitet är mer sannolik. Författarna mätte hur starkt långsamma rytmer i band som theta och alfa låste samman med snabbare beta- och gammaaktivitet, både inom och mellan de sju nätverken. Starkare koppling kan ibland vara användbar, men om den blir för snäv eller oflexibel kan det indikera en obalans i hur information flyter genom hjärnan.
Autistiska hjärnor visar tajtare koppling i vila
Under placebo visade autistiska deltagare konsekvent högre koppling mellan theta- och beta-rytmer över de flesta hjärnnätverk när ögonen var stängda, jämfört med icke-autistiska försökspersoner. Det limbiska systemet utmärkte sig: där var alla fyra kopplingsmått som teamet undersökte förhöjda, vilket tyder på ovanligt starka länkar mellan långsamma, utbredda rytmer och snabb lokal aktivitet i regioner som är involverade i känslor och minne. Det somatomotoriska nätverket visade också förhöjd koppling mellan theta och gamma. Dessa mönster stöder idén att excitation–inhibition-balansen är förändrad på nivån av dynamiska hjärnrytmer vid autism, särskilt i sensoriska och emotionella nätverk.
Doseringen spelar roll — och olika nätverk beter sig olika
När forskarna tillförde arbaclofen blev bilden mer komplex och dosberoende. Hos autistiska deltagare förde den högre dosen 30 mg den förhöjda theta–beta-kopplingen i visuella och somatomotoriska nätverk närmare intervallet för icke-autistiska deltagare, vilket tyder på ett mer typiskt mönster för sensorisk informationsflöde. Däremot förändrades nätverk som stöder planering, självrefererande tankar och uppmärksamhet mycket lite. Det limbiska systemet uppvisade ett annat beteende: en låg dos på 15 mg förde dess överdrivna koppling — både inom nätverket och i dess förbindelser med andra nätverk — närmare kontrollnivåerna. Men vid 30 mg återkom många av dessa avvikelser, och atypiska limbiska länkar till andra nätverk, såsom det somatomotoriska, dök upp igen. Med andra ord verkade vissa emotionella kretsar svara bäst på lägre doser och kunna bli överstimulerade vid högre doser.
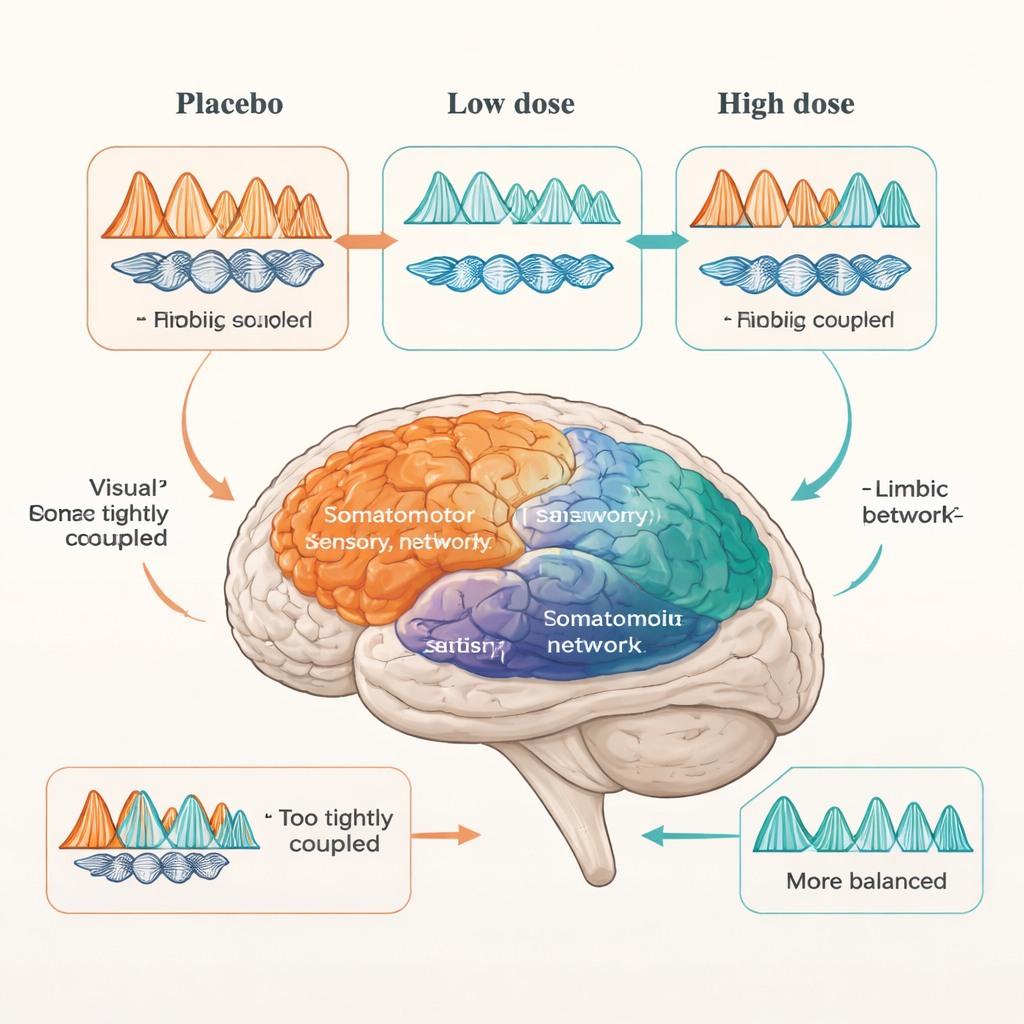
Vad detta betyder för verkliga behandlingar
För en lekmannaläsare är huvudbudskapet att den autistiska hjärnan inte svarar på GABA-verkande läkemedel på ett enkelt, enhetligt sätt. Olika hjärnnätverk — sensoriska, emotionella och högre kognitiva system — visar distinkta känslighetsmönster, och vissa kretsar är särskilt doskänsliga. Det hjälper till att förklara varför mediciner som riktar in sig på hämning ibland kan ge paradoxa eller blandade effekter vid autism, genom att hjälpa i ett område samtidigt som de stör ett annat. Även om denna studie inte testar om arbaclofen förbättrar vardagliga symtom, visar den att noggrant valda doser kan styra vissa autistiska hjärnnätverk mot en mer typisk balans i aktiviteten. Framtida arbete kan använda denna typ av hjärnbaserade «stress-test» för att individualisera behandlingar, med målet att återställa en mer flexibel och bättre avstämd kommunikation mellan hjärnans nätverk.
Citering: Huang, Q., Chen, D., Pereira, A.C. et al. Differential GABA dynamics across brain functional networks in autism. Commun Biol 9, 283 (2026). https://doi.org/10.1038/s42003-026-09563-5
Nyckelord: autism, GABA, hjärnnätverk, EEG, arbaclofen