Clear Sky Science · sv
Radionuklid‑stimulerad dynamisk terapi framkallar kompletterande immunogen nekroptos och apoptos som cancercellsdöd
Vända cancerns knep mot sig själv
Cancer är ökänd för att slingra sig undan våra bästa behandlingar, särskilt i aggressiva brösttumörer som sprider sig i kroppen. Denna studie undersöker en nytänkande metod kallad radionuklid‑stimulerad dynamisk terapi (RaST), som använder diagnostiska spårämnen och ljusaktiverade nanopartiklar för att döda cancerceller på sätt som också väcker immunsystemet. För läsaren är arbetet viktigt eftersom det visar hur befintliga bilddiagnostiska verktyg och smarta material kan återanvändas för att skapa långvarig, immundriven cancerkontroll snarare än temporär tumörkrympning.
Ett nytt sätt att belysa tumörer inifrån
Traditionella ljusbaserade cancerbehandlingar fungerar bara där en extern stråle når, som vid hud- eller ytliga tumörer. RaST kringgår denna begränsning genom att använda ett radioaktivt socker, liknande det spårämne som redan används i PET‑skanningar, som naturligt ansamlas i snabbväxande cancerceller. När detta spårämne rör sig genom tumören avger det ett svagt blått sken känt som Cerenkov‑strålning. Forskarna designade små titandioxid‑nanopartiklar belagda med ett cancerinriktande protein så att de också söker sig till tumören. När spårämnet och nanopartiklarna möts, tänds det interna ljuset i partiklarna, vilka i sin tur genererar utbrott av reaktiva syrearter — mycket reaktiva molekyler som skadar cancerceller inifrån.
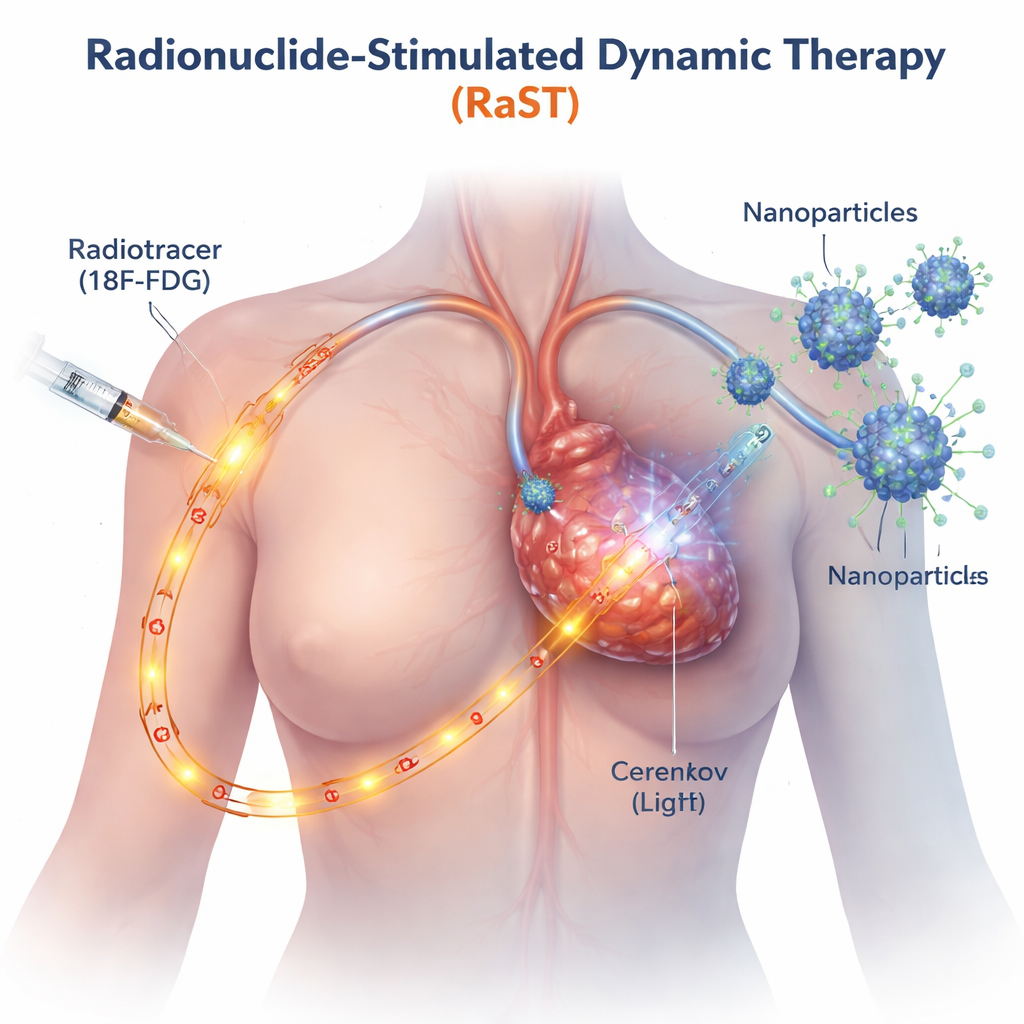
Utlösning av två distinkta dödsvägar
Teamet ville veta inte bara om RaST dödade cancerceller, utan hur. Med flera aggressiva bröstcancercellinjer i laboratoriet fann de att noggrant avvägda doser av radioaktivt spårämne och nanopartiklar samarbetade för att skada tumörceller mer effektivt än någon av komponenterna för sig, även i typer som är kända för att motstå standardkemoterapi. Detaljerad avbildning och proteinmätningar visade att RaST aktiverade två reglerade celldödsprogram samtidigt. Det ena var apoptos, ofta beskrivet som cellens "självmord", där celler plockas isär på ett ordnat sätt. Det andra var nekroptos, en mer explosiv dödsform där celler sväller, spricker och spiller ut molekylära nödsignaler i omgivningen. Dessa signaler, kända som skadedomassocierade molekyler och inflammatoriska cytokiner, kan fungera som nödraketer som drar till sig och aktiverar immunceller.
Inkallande av immunsystemet för varaktig kontroll
För att se om denna inflammatoriska typ av tumördöd var betydelsefull i levande organismer testade forskarna RaST i musmodeller av bröstcancer. Hos möss som saknade centrala immunsvar gjorde RaST lite för att stoppa tumörtillväxt eller lungmetastaser, trots att behandlingen gav riklig lokal celldöd. Men hos möss med intakt immunsystem gav samma behandling partiella och fullständiga tumörsvar och förhindrade spridning till lungorna. Tumörer som exponerats för RaST blev fyllda med immunceller — särskilt myeloida celler såsom makrofager och dendritiska celler — som är skickliga på att ta upp dött material och presentera tumörfragment för T‑celler. Blodprover visade vågor av immunstimulerande och immunreglerande signaler över tid, vilket tyder på att RaST först tänder en attack mot cancern och senare skiftar mot ett mer balanserat tillstånd när tumörer krymper eller stabiliseras.
Jaga dolda rester och skydda mot återfall
Även hos möss där tumörerna verkade fullständigt botade av RaST avslöjade ett mycket känsligt avbildningsfärgämne senare små fickor av kvarvarande cancerceller inbäddade i lymfkörtlar. Anmärkningsvärt nog utvecklade dessa djur fortfarande inga nya tumörer eller distanta metastaser under många månader. Kemiska analyser visade att titandioxid‑nanopartiklarna, som initialt var rikliga i ben och lever, gradvis omfördelades till mjälten och lymfkörtlarna — just de nav där immunceller patrullerar. Denna långsamma migration håller sannolikt en lokal källa av reaktivt syre tillgänglig för immunceller, vilket hjälper dem att känna igen och kontrollera dessa dolda cancerrester innan de kan växa ut eller spridas.
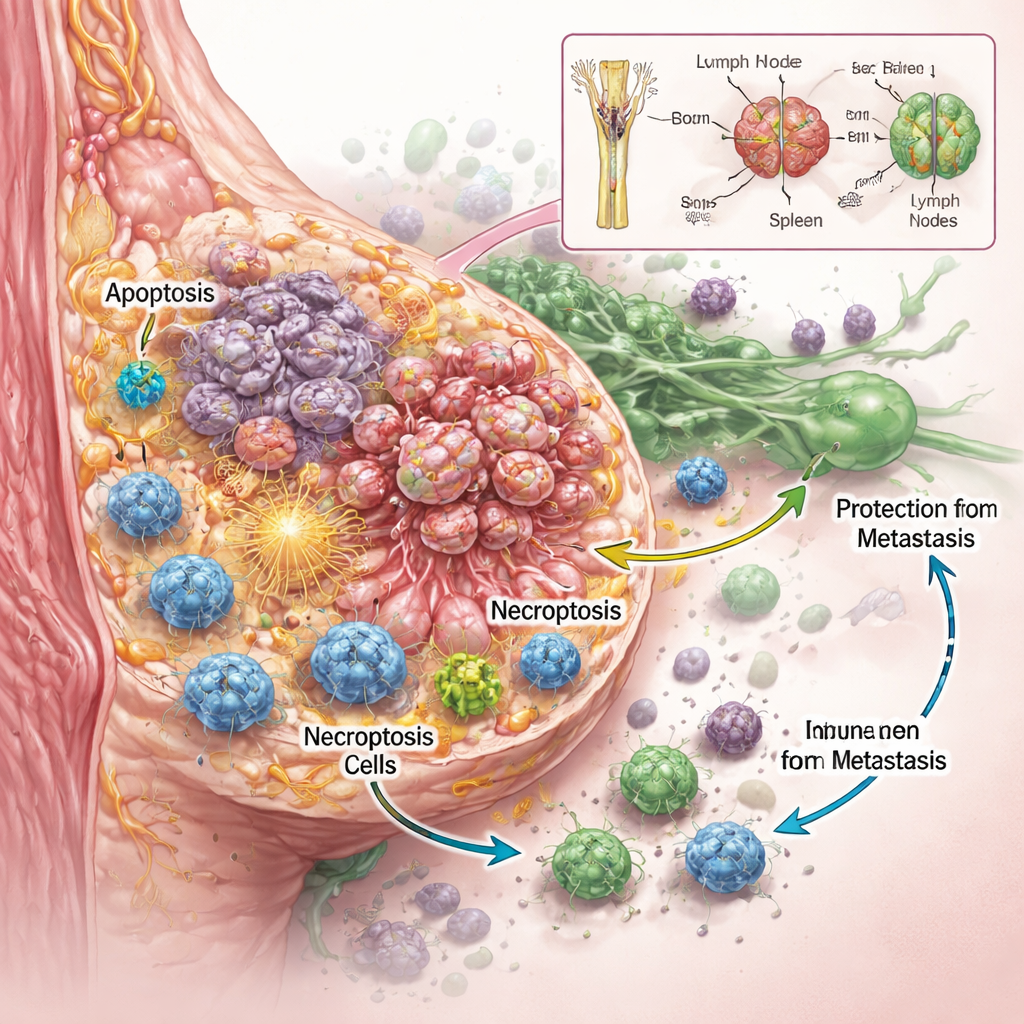
Vad detta kan innebära för framtida cancerbehandling
Enkelt uttryckt visar detta arbete att RaST är mer än bara ett sätt att förgifta tumörceller. Genom att kombinera radioaktiva spårämnen, ljusresponsiva nanopartiklar och kroppens egna försvar tvingar metoden cancerceller in i två former av programmerat dödande som högljutt larmar immunsystemet. I immunintakta djur leder detta till varaktig kontroll av aggressiva brösttumörer och blockerar metastasering, även när några cancerceller finns kvar i lymfkörtlar. Mycket återstår innan denna strategi kan prövas brett på människor, men studien pekar mot framtida behandlingar som inte enbart syftar till att krympa tumörer utan till att omforma förhållandet mellan cancer, celldöd och immunitet så att kroppen själv kan hjälpa till att hålla sjukdomen i schack på lång sikt.
Citering: Egbulefu, C., Black, K., Su, X. et al. Radionuclide-stimulated dynamic therapy induces complementary immunogenic necroptosis and apoptosis cancer cell death pathways. Commun Biol 9, 275 (2026). https://doi.org/10.1038/s42003-026-09555-5
Nyckelord: bröstcancer, nanopartiklar, immunterapi, radionuklidterapi, nekroptos