Clear Sky Science · sv
Glykofagi är en gammal bilateriansk väg som stödjer metabol anpassning genom evolution av STBD1:s struktur
Hur ostron avslöjar dolda energitrick
Djur överlever svåra perioder genom att utnyttja lagrad bränsle, men de förlitar sig inte alla på samma slags ”batteri”. Den här studien granskar Stillahavsobservon och visar att, till skillnad från många andra djur som lutar sig mot fett, förlitar sig ostron i hög grad på lagrat socker i form av glykogen. Arbetet blottlägger en relativt okänd cellulär återvinningsväg — kallad glykofagi — som hjälper ostron att snabbt tömma och återfylla sina sockerreserver, och spårar hur detta system har utvecklats över djurriket.
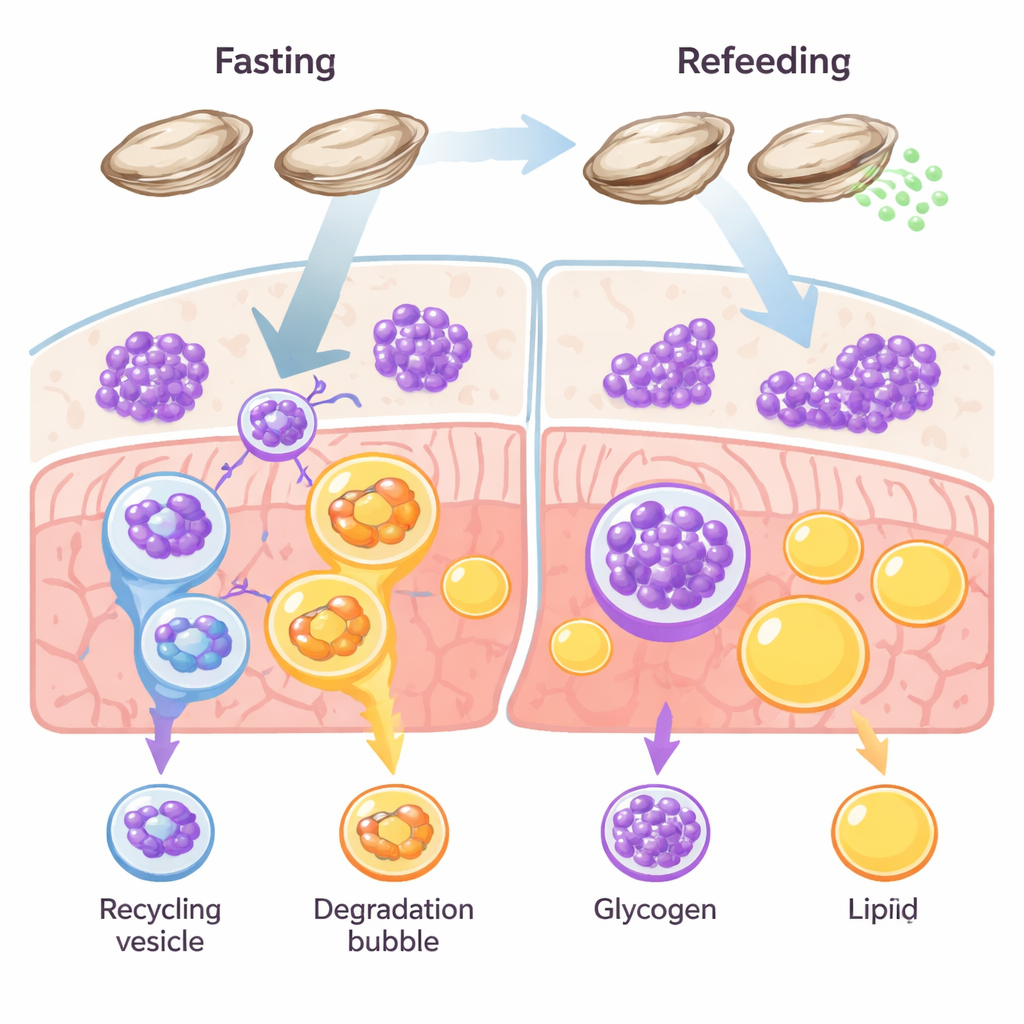
En socker-centrerad överlevnadsstrategi
De flesta djur sköter flera energireserver, främst fett och glykogen. Hos ryggradsdjur som fiskar och däggdjur dominerar ofta fett som den långsiktiga reserven. Ostron bryter mot denna regel. Deras vävnader är fulla av glykogen, och tidigare forskning har antytt att dessa musslor förbrukar socker snarare än fett när föda är knapp eller när de bildar ägg och spermier. Författarna ville testa om glykofagi — en riktad nedbrytning av glykogen inne i cellerna — fungerar som en primär överlevnadsväg hos ostron under svält och återhämtning.
Att se celler växla från lagring till förbrukning
Teamet svältade Stillahavsostron i två veckor och matade dem sedan igen, och följde hur deras vävnader svarade över tid. Under fastan visade mikroskopiska färgningar en ökning av autofagimarkörer — cellulära ”städnings”-signaler — just där glykogen lagrades, samtidigt som själva glykogenet minskade. Fettreserverna förändrades däremot knappt. När ostronen matades igen återkom glykogenet snabbt och autofagisignalerna sjönk. Samtidigt steg och föll nivåerna av ett nyckelreceptorprotein kallat STBD1, som specifikt kopplar glykogen till autofagimaskineriet, i takt med glykogenanvändningen. En annan receptor kopplad till fettåtervinning, p62, förblev i stort sett oförändrad. Tillsammans pekar dessa mönster på en dedikerad, sockerfokuserad återvinningsväg: glykofagi, inte fettbrännande lipofagi, bär huvudansvaret för ostronens energibalans.
Det molekylära kroket som fångar glykogen
Glykofagi beror på att STBD1 fungerar som ett molekylärt krok: det binder glykogen och överlämnar det till små adapterproteiner som bygger återvinningsvesiklar. Hos ostron visade sig STBD1 vara konfigurerat annorlunda än sin ryggradsdjur-motsvarighet. Ostronproteinet bär sitt glykogenfångande område, känt som CBM20-domänen, i främre änden (N-terminalen), medan ryggradsdjurs STBD1 placerar samma modul i bakänden (C-terminalen) och inkluderar en extra fettrik svans som förankrar det i cellulära membran. Datorbaserade modeller och simuleringar föreslog att ostronets N-terminala layout ger CBM20 ett starkare, mer mångsidigt grepp om grenade sockerkedjor. Laboratorieexperiment stöder detta: renat ostron-STBD1 band till glykogen starkare än fisk- eller mus-STBD1, och när alla versioner uttrycktes i humana celler drev ostronproteinet en mer markant minskning av glykogen under inducerad autofagi.
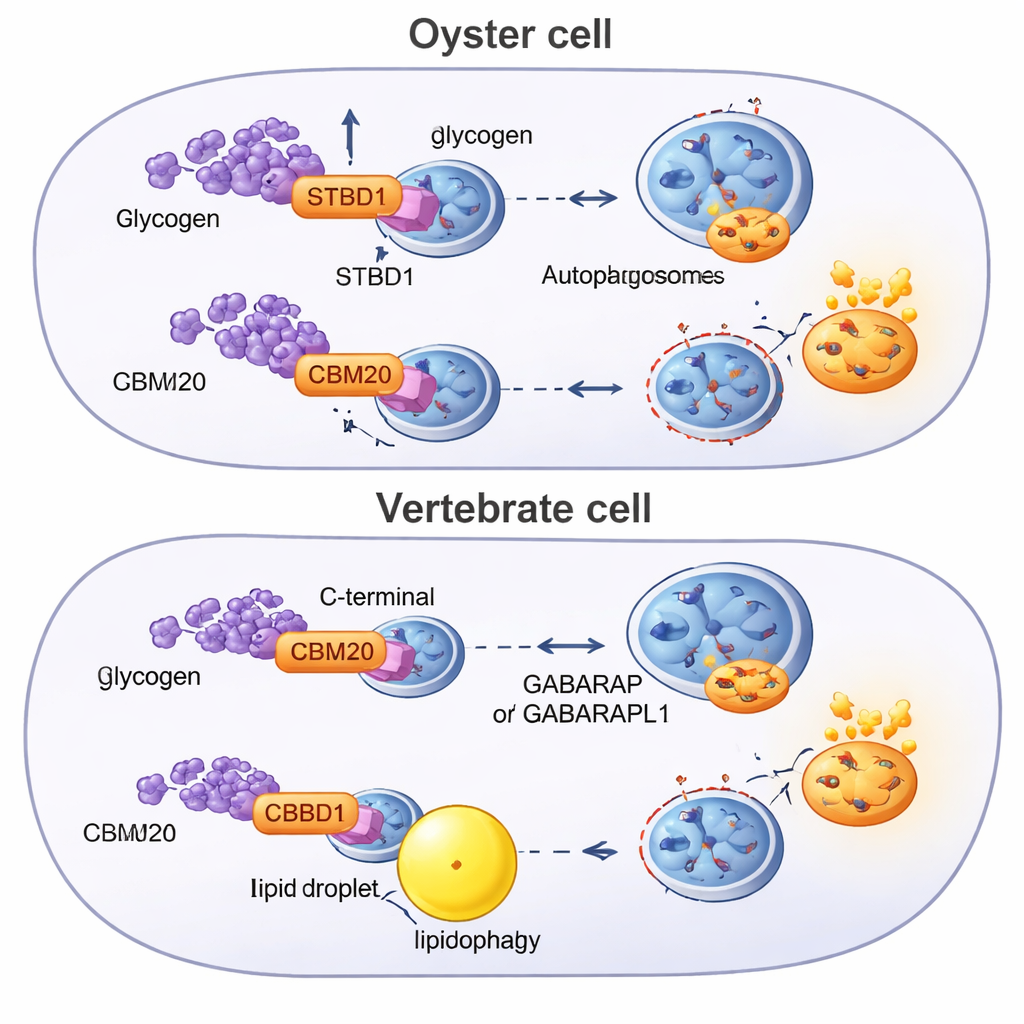
Omlänkning av en uråldrig väg över djuren
För att förstå var detta system uppstod skannade forskarna genom genomesekvenser från flera dussin djur efter CBM20-bärande proteiner och byggde evolutionära träd. De fann att STBD1 är en bilateriansk uppfinning — den dök upp i den gemensamma förfadern till djur med tvåsidiga kroppar — men dess struktur har omorganiserats i olika linjer. Ostron och andra lophotrokozoer tenderar att bevara den ursprungliga N-terminala CBM20-designen, ibland till och med duplicera den sockerbindande modulen. Kordater, gruppen som inkluderar ryggradsdjur, visar en distinkt version där CBM20 har flyttats till proteinets svans. Denna omarrangemang korrelerar med svagare glykogenbindning och med en metabol strategi som lutar mer mot fettnedbrytning via lipofagi, understödd av andra autofagireceptorer och adapterproteiner som ostron saknar.
Vad detta betyder för livets energival
För icke-specialister är huvudbudskapet att djur har utvecklat mer än ett sätt att klara energibrist. Ostron visar upp en gammal, sockercentrerad strategi: en hög-affinitetsvariant av STBD1 fångar snabbt glykogen och matar in det i cellulära återvinningsenheter, vilket gör glykofagi till en viktig energikälla under stress. Ryggradsdjur, däremot, verkar ha bytt bort en del av det starka sockergreppet mot ett mer balanserat eller fettfokuserat tillvägagångssätt, understött av andra proteinpartners och domänupplägg. Genom att knyta detaljerad proteinstruktur till hela organismers bränsleval visar denna studie hur små molekylära ”omkopplingar” kan hjälpa olika grenar av djurens utveckling att anpassa sig till sina egna miljöer och livsstilar.
Citering: Ren, L., Bai, Y., Shi, C. et al. Glycophagy is an ancient bilaterian pathway supporting metabolic adaptation through STBD1 structural evolution. Commun Biol 9, 268 (2026). https://doi.org/10.1038/s42003-026-09546-6
Nyckelord: glykofagi, glykogenmetabolism, ostronsbiologi, autofagi, metabolismens evolution