Clear Sky Science · sv
Epigenetisk och metabol omprogrammering i metastaserande feokromocytom och paragangliom drivna av SDHB‑mutationer
Varför dessa sällsynta tumörer spelar roll
Feokromocytom och paragangliom är sällsynta tumörer som utvecklas från hormonproducerande nervceller, ofta i närheten av binjurarna. De flesta växer långsamt och kan botas med kirurgi, men ungefär en av fem sprider sig så småningom till andra organ och blir livshotande. Denna studie ställer en enkel men avgörande fråga: vad gör att vissa av dessa tumörer blir farliga? Genom att noggrant granska hur dessa cancerformer styr av- och påslagning av gener och hur de får energi, avslöjar forskarna en dold svaghet som en dag skulle kunna utnyttjas med nya behandlingar.
Från tyst tillväxt till dödlig spridning
Forskarna fokuserade på tumörer som bär förändringar i genen SDHB. SDHB hjälper mitokondrierna — cellens kraftverk — att driva delar av citronsyracykeln, en central energiproducerande väg. När SDHB skadas byggs en molekyl som kallas succinat upp, och cellerna börjar bete sig som om de levde i låg syretillgång, även när de inte gör det. Forskarna studerade vävnad från 34 patienter och jämförde tumörer som förblev lokala med sådana som redan hade spridit sig. Med hjälp av en högupplöst DNA‑"metylerings"‑karta, som visar hur kemiska markörer skruvar upp eller ner geners aktivitet, fann de att metastaserande tumörer hade ett starkare mönster av genavstängning än godartade tumörer, särskilt när SDHB var muterat.
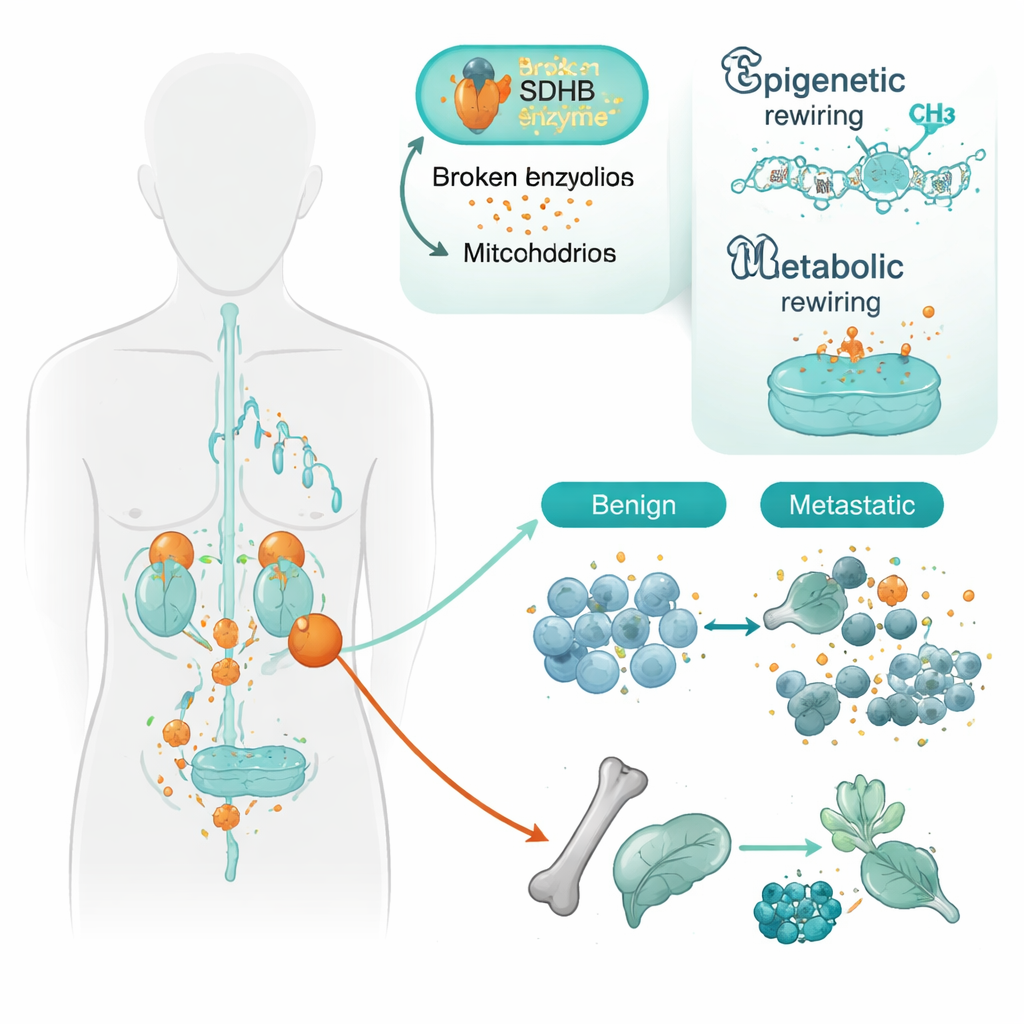
Omprogrammering av cellidentitet
Många av de gener som tystades i aggressiva tumörer var sådana som hjälper nervlika celler att mogna och bevara sin specialiserade identitet. Det inkluderar genfamiljer som styr hur celler fäster vid varandra, organiserar sitt DNA och bestämmer vilken celltyp de ska bli. Ett särskilt exempel var ett cell‑adhesionsgen kallat PCDHGC3. Även i icke‑spridande SDHB‑mutanta tumörer var detta gens kontrollregion redan delvis avstängd; i metastaser blev avstängningen ännu starkare. En annan gen, SATB2, som är inblandad i att organisera stora DNA‑regioner, tystades endast i metastaserande tumörer oavsett SDHB‑status. Tillsammans tyder dessa mönster på att SDHB‑förlust "förbereder" celler för ett mindre moget, mer rörligt tillstånd, och att ytterligare epigenetiska förändringar sedan hjälper dem att bryta sig loss och sprida sig.
Omkoppling av hur tumörer använder socker
Överraskande nog handlade inte alla förändringar om genavstängning. En mindre grupp gener blev mindre metylerade och mer aktiva, och dessa var starkt involverade i transport av socker in i celler. Bland dem stack fruktostransportören SLC2A5 ut. Dess produkt, känd som GLUT5, för in fruktos — en sockerart som finns i frukt och i många processade livsmedel — i cellerna. I laboratoriemodeller av tumörlika celler utsatta för låg syretillgång slog SLC2A5 gradvis på, medan andra sockertransportörer reagerade mer inkonsekvent. Författarna skapade sedan patient‑härledda cellkulturer från PPGL‑tumörer och visade att när glukos var knapp, hjälpte tillsatt fruktos dessa celler att fortsätta dela sig, särskilt under låg‑syrerade förhållanden som efterliknar tumörmiljön.
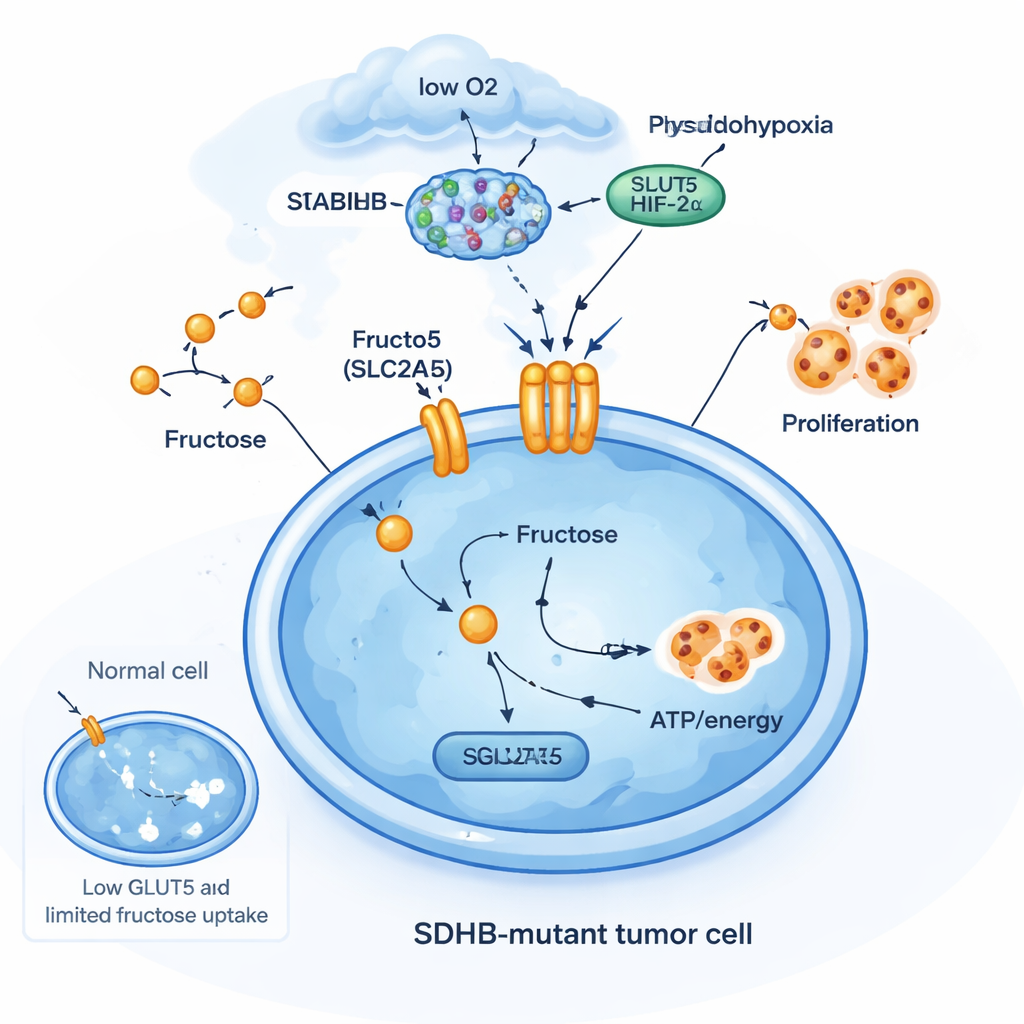
En fruktosdriven överlevnadsstrategi
För att förstå varför SDHB‑mutationer spelar roll här redigerade teamet flera celltyper för att ta bort SDHB. I kromaffinliknande celler från binjuren och i en njurcancercellinje med konstant aktivering av syre‑känsliga faktorn HIF2α ökade förlust av SDHB nivåerna av SLC2A5. Men i mer vanliga cancercellinjer som saknade dessa neuroendokrina eller HIF2α‑egenskaper ledde samma SDHB‑utslag inte till att SLC2A5 slog på. Detta visar att fruktostransportören inte är en del av en generell stressreaktion; det är en mycket specifik anpassning i vissa celltyper som redan lever i ett "pseudo‑hypoxiskt" tillstånd. I dessa celler samarbetar SDHB‑förlust, succinatuppbyggnad och HIF2α‑aktivitet för att öppna en ny metabolisk dörr: fruktosupptag som bränsle för tillväxt när syre och glukos är begränsade.
Vad detta betyder för patienter
Kort sagt visar studien en dubbel omställning i SDHB‑mutanta metastaserande PPGL. För det första är deras DNA‑kontrollsystem omkopplat så att celler drivs mot ett mindre specialiserat, mer plastiskt tillstånd som är benäget att invadera. För det andra är deras energisystem omkopplat för att utnyttja fruktos som ett alternativt bränsle i hårda, lågt syresatta och glukosfattiga nischer. Genom att identifiera fruktostransportören SLC2A5/GLUT5 som en nyckelspelare i denna process pekar arbetet på en möjlig hälsena: att blockera fruktosupptag eller dess metabolism skulle selektivt kunna svälta dessa tumörer medan de flesta normala vävnader skonas. Även om sådana terapier ännu inte finns, är kartläggningen av detta epigenetiska och metabola landskap ett viktigt steg mot mer precisa, metabolismfokuserade behandlingar för patienter med högrisk SDHB‑mutanta PPGL.
Citering: Cubiella, T., Alba-Linares, J.J., San-Juan-Guardado, J. et al. Epigenetic and metabolic rewiring in metastatic pheochromocytomas and paragangliomas driven by SDHB mutations. Commun Biol 9, 266 (2026). https://doi.org/10.1038/s42003-026-09543-9
Nyckelord: feokromocytom, paragangliom, SDHB‑mutation, epigenetik, fruktosmetabolism