Clear Sky Science · sv
Multi-omisk analys av mänskliga PHACTR1‑signalnätverk
Varför detta blodkärnsgen spelar roll för dig
Hjärtattacker, stroke och högt blodtryck går alla tillbaka till blodkärlens tillstånd. Ett enda gen, PHACTR1, återkommer i stora genetiska studier av dessa tillstånd, men forskarna har inte förstått varför. Denna studie använde en vidsträckt, ”på alla nivåer” undersökning inne i mänskliga celler för att kartlägga vad PHACTR1 faktiskt gör, och avslöjade hur det kan påverka celltillväxt, energianvändning och järnhantering — processer som i slutändan formar artärernas hälsa.
En helhetskartläggning inne i cellerna
I stället för att fokusera på en molekyl åt gången använde forskarna en strategi kallad multi-omik — att samtidigt mäta tusentals RNA, proteiner, små metaboliter och fetter (lipider) i celler. De konstruerade humana celler så att de antingen producerade extra PHACTR1 eller hade genen nedreglerad, vilket efterliknar naturliga genetiska skillnader hos människor. Genom att jämföra dessa förändrade celler med normala kontroller över fyra molekylära lager, och sedan mata data genom avancerad vägprogramvara, byggde de en global karta över hur förändringar i PHACTR1 sprider sig genom cellens inre maskineri. 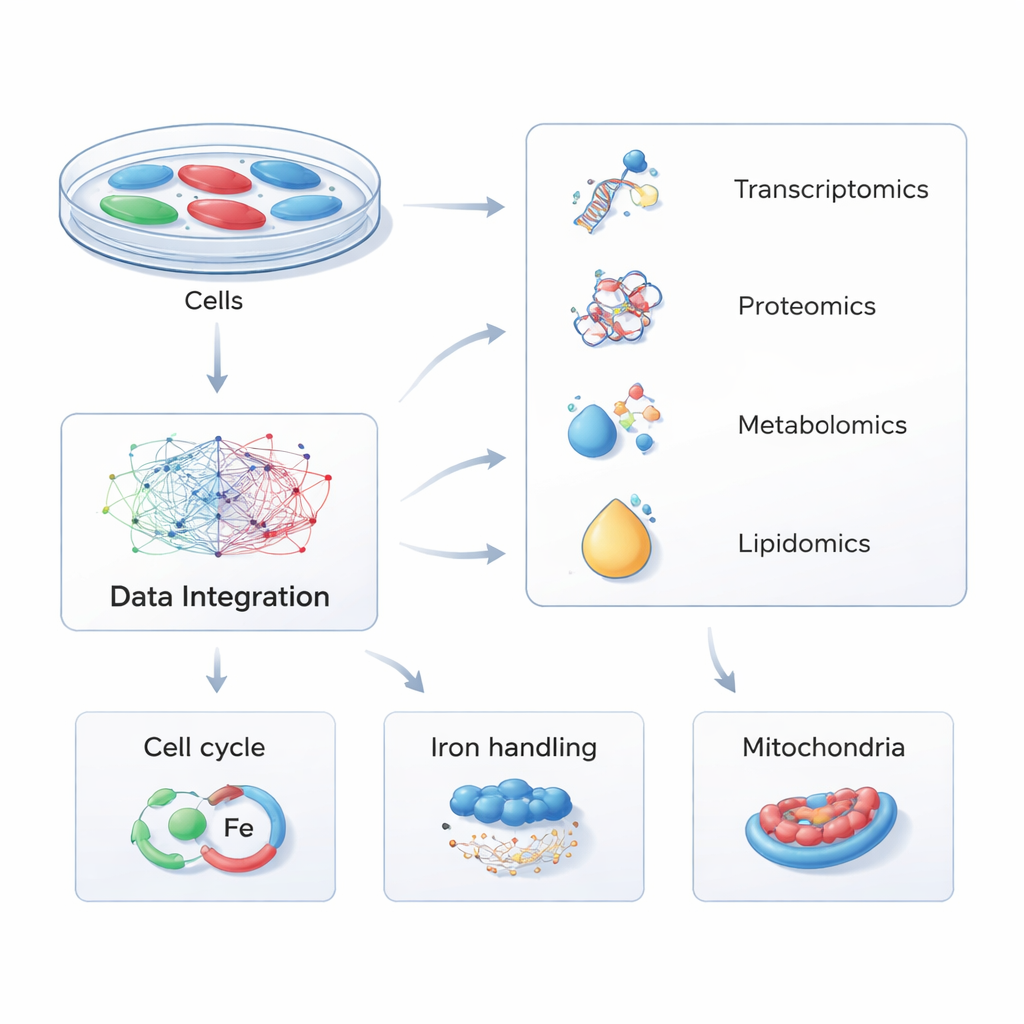
Bortom cellskelettet: styrning av tillväxtcykler
PHACTR1 var tidigare mest känt för att hjälpa till att organisera cellens inre skelett av aktinfibrer. De nya uppgifterna visade att det också har en stark roll i att reglera cellcykeln — den koreografi genom vilken celler kopierar sitt DNA och delar sig. Celler med extra PHACTR1 lämnade vilofasen G1 och ansamlades i DNA-kopierings- och fördelningsförberedande faser, med färre celler som framgångsrikt gick in i full mitos. Nyckelregulatorer som Cyclin B1, Cdt1 och andra cellcykelproteiner påverkades. När teamet upprepade experimenten i primära humana endotelceller — cellerna som bekläder blodkärl — såg de återigen förändringar i kärnregulatorer för cellcykeln. Det tyder på att PHACTR1 hjälper avgöra när kärlcellers vilar, delar sig eller stannar upp, en balans som är avgörande både för att reparera kärlväggar och för bildning av farliga vävnadsöverväxten.
Hantering av järn och skydd mot skada
Integrationen av multi-omik pekade också på järnrelaterade vägar och en specialiserad form av järndriven celldöd kallad ferroptos. Även om cellerna inte aktivt dog via ferroptos minskade ökande PHACTR1 nivåerna av större järnhanterande proteiner, inklusive ferritin tung kedja (det huvudsakliga järnlagringsskalet) och heme oxygenas 1 (som återvinner järn från hem). I primära endotelceller påverkade PHACTR1 på liknande sätt dessa proteiner och viktiga försvarare mot oxidativ skada. Eftersom felhanterat järn kan driva inflammation, oxidativ stress och instabila aterosklerotiska plack, antyder dessa resultat att PHACTR1 kan finjustera hur kärlceller lagrar och detoxar järn, vilket potentiellt påverkar vilka som blir mer sårbara för vissa kärlsjukdomar.
Mitokondrier, energi och artärhälsa
En annan överraskning var PHACTR1:s roll i mitokondrierna, cellens kraftverk. Teamet fann PHACTR1‑protein i isolerade mitokondrier och såg att ändrade nivåer formade mitokondriernas nätverk. När PHACTR1 var högt var mitokondrierna mer förlängda, och ett protein kallat Drp1 var kemiskt modifierat på en plats som minskar mitokondriell delning. Nivåer av ett scaffold‑protein, AKAP1, som hjälper organisera signalering på mitokondriens yta, steg och sjönk i takt med PHACTR1. Dessa strukturella skiften motsvarade förändringar i hur cellerna producerade energi: hög PHACTR1 minskade mitokondriell ATP‑produktion och kopplades till en ansamling av vissa fettsyraderiverade molekyler som signalerar långsam fettförbränning, medan låg PHACTR1 fick celler att förlita sig mer på sockerförbrännande glykolys. Analyser av mänskliga artärprover visade att PHACTR1 och AKAP1 tenderar att uttryckas samtidigt, vilket binder denna mitokondriella kontrollkrets direkt till verkliga blodkärl. 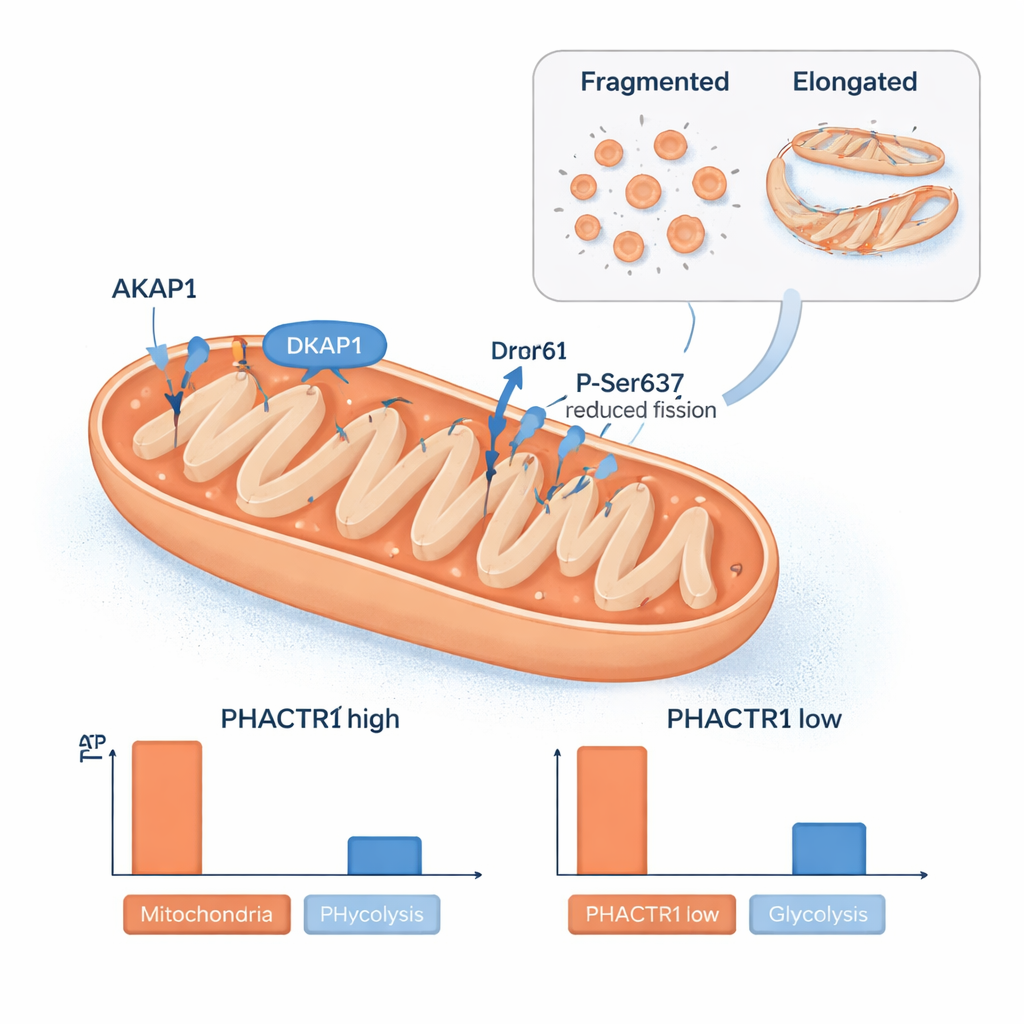
Vad allt detta betyder för blodkärlen
Sammantaget visar detta arbete att PHACTR1 inte är en gen för ett enda ändamål utan en huvudkoordinator som rör vid hur kärlceller delar sig, lagrar järn och driver sin energiomsättning. Genom att kartlägga dessa kopplingar över tusentals molekyler hjälper studien förklara varför naturliga skillnader i PHACTR1 är kopplade till ett så brett spektrum av kärlrelaterade sjukdomar — från kranskärlssjukdom till spontana artärriftningar och migrän. För icke‑specialister är budskapet att en gen som flaggats i mänsklig genetik nu spåras till konkreta cellulära beteenden som påverkar placktillväxt, kärlstabilitet och energibalans. På sikt kan förståelsen av dessa PHACTR1‑styrda nätverk öppna dörren för mer precisa behandlingar som finjusterar cellcykler, järnhantering eller mitokondriell funktion tillbaka mot ett friskare tillstånd hos personer med risk för hjärt‑kärlsjukdom.
Citering: Wolhuter, K., Ma, L., Bryce, N.S. et al. Multi-omic analysis of human PHACTR1 signaling networks. Commun Biol 9, 265 (2026). https://doi.org/10.1038/s42003-026-09542-w
Nyckelord: PHACTR1, kärlsjukdom, multi-omik, mitokondrier, järnmetabolism