Clear Sky Science · sv
Målinriktning av PAK4 främjar gemcitabinin inducerad pyroptos i pankreascancer via NLRP1/caspas-3/GSDME-axeln
Varför det kan spela roll att döda cancerceller på ett "eldigt" sätt
Pankreascancer tillhör de dödligaste cancerformerna, och även våra bästa cytostatika slutar ofta fungera när tumörer utvecklar resistens. Denna studie undersöker en oväntad vändning: samma läkemedel, gemcitabin, kan döda cancerceller på ett mer explosivt, inflammatoriskt sätt kallat pyroptos — om en viktig molekylär "broms" kallad PAK4 stängs av. Att förstå och rikta in sig på denna broms skulle kunna göra befintliga behandlingar effektivare för många patienter.
En envis cancer som avfärdar behandling
Pankreas ductalt adenokarcinom upptäcks oftast sent och svarar dåligt på behandling, så gemcitabin förblir ett hörnstenläkemedel trots sina begränsningar. Gemcitabin dödar vanligen celler genom apoptos, en prydlig, tyst form av programmerad celldöd. Men mer än hälften av de pankreastumörer som undersöktes i denna studie producerade höga nivåer av ett protein kallat GSDME, vilket kan vända denna tysta död till pyroptos — en snabb, "explosiv" form av celldöd som skadar cellmembranet och frisätter inflammatoriska signaler. Det väckte en viktig fråga: om tumörer kan genomgå pyroptos, varför är så många ändå resistenta mot gemcitabin?
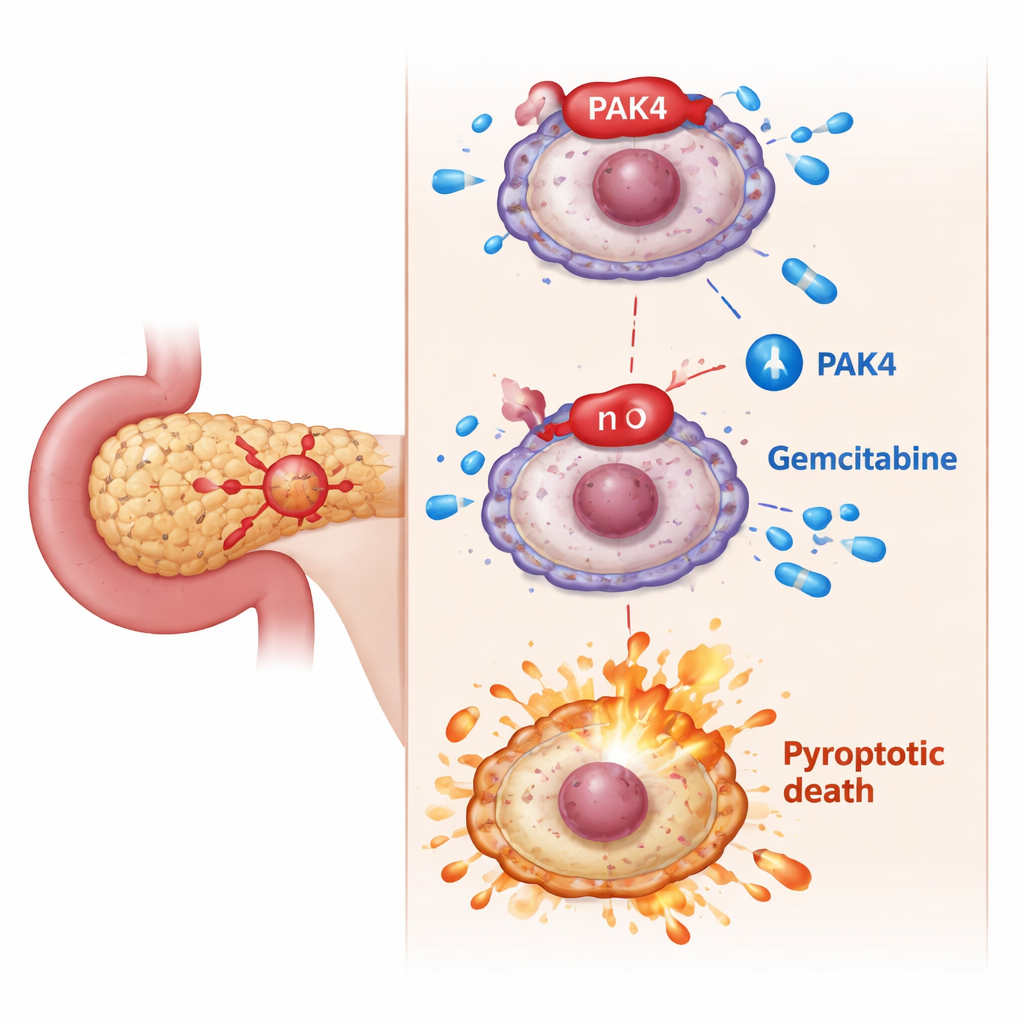
Den dolda bromsen: PAK4 blockerar eldig celldöd
Forskarna riktade in sig på PAK4, ett tillväxtfrämjande protein som är känt för att vara överaktivt i pankreascancer och kopplat till sämre svar på gemcitabin. I cellexperiment var cancerceller med höga PAK4-nivåer svårare att döda med gemcitabin. När teamet minskade PAK4 blev gemcitabin plötsligt mycket mer dödligt: cellerna visade klassiska pyroptotiska kännetecken — svullnad, ballongliknande blåsor, rupturerade membran och ökad frisättning av intracellulärt innehåll. På molekylär nivå berodde denna förskjutning på att GSDME klyvdes till en aktiv fragment av ett annat protein, caspas-3. Att blockera caspas-3 stoppade GSDME från att utlösa pyroptos, vilket bekräftar att PAK4 normalt fungerar som en broms för denna dödsväg.
Hur PAK4 demonterar cellens dödsalarm
När de grävde djupare fann forskarna att PAK4 inte angriper GSDME direkt. Istället saboterar det en upstream "alarmsensor" kallad NLRP1. Hos patienter var högre NLRP1-nivåer kopplade till bättre överlevnad, vilket tyder på att den hjälper kroppen att hålla tumörer i schack. I cancerceller, när NLRP1 avlägsnades, sjönk gemcitabininducerad celldöd och GSDME-aktivering kraftigt, vilket visar att NLRP1 matar in i pyroptosmolekylerna. PAK4- och NLRP1-nivåerna var omvänt relaterade i tumörprover: där PAK4 var hög var NLRP1 låg. Studien visade att aktiv PAK4 verkar via ett annat protein, E3-ligasen Mdm2, för att märka NLRP1 för nedbrytning av cellens avfallssystem. Genom att markera NLRP1 på detta sätt förhindrar PAK4 aktivering av en kaskad — via caspas-9 och caspas-3 — som normalt skulle kulminera i GSDME-driven pyroptos.
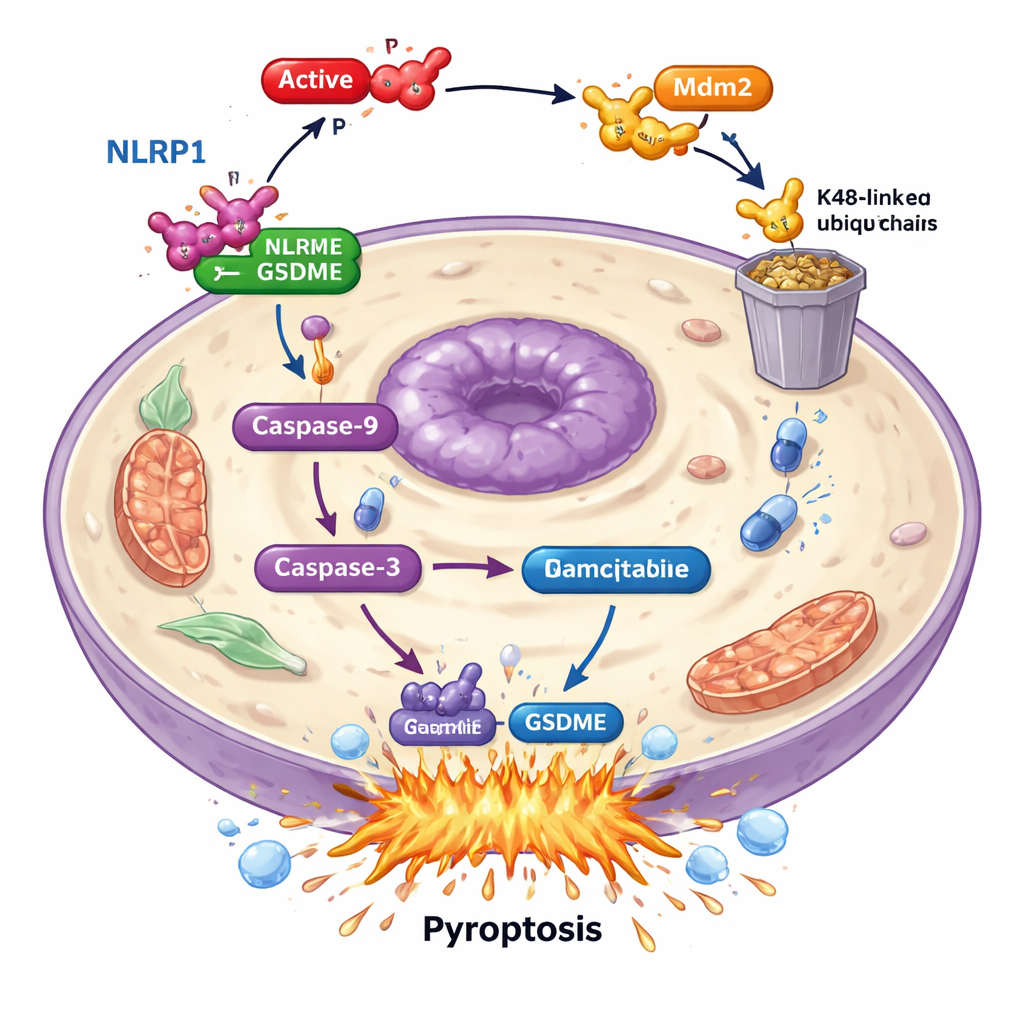
Stänga av PAK4 för att överladda cytostatika
Eftersom PAK4 fungerar som en broms på pyroptos testade teamet om blockering av dess aktivitet kunde återväcka gemcitabins dödskraft. De använde en småmolekylär PAK4-hämmare kallad PF-3758309. Ensamt drev denna hämmare redan pankreascancerceller mot pyroptos, med ökad caspas-3-aktivering, GSDME-klyvning och cellmembranruptur. I kombination med gemcitabin blev effekten ännu starkare: fler celler dog genom pyroptos och molekylära tecken på dödsvägen förstärktes. I musmodeller med mänskliga pankreastumörer gjorde både minskad PAK4 och behandling med PAK4-hämmaren att gemcitabin krympte tumörer mer effektivt och ökade pyroptotiska markörer i cancrarna.
Vad detta betyder för patienter och framtida behandlingar
Enklare uttryckt avslöjar detta arbete ett molekylärt lås — PAK4 — som hindrar pankreascancerceller från att dö på ett särskilt destruktivt sätt under cytostatikabehandling. Genom att inaktivera PAK4 skulle läkare kunna tvinga gemcitabinbehandlade tumörer in i pyroptos, göra läkemedlet mer effektivt och potentiellt stimulera immunsystemet mot cancern. Även om mer arbete i patientnära modeller och kliniska prövningar behövs, föreslår studien en tydlig färdplan: rikta in sig på PAK4–Mdm2–NLRP1–GSDME-vägen för att omvandla resistenta tumörer till sådana som svarar, med hjälp av läkemedel vi redan har i smartare kombinationer.
Citering: Lu, T., Song, Y., Liang, K. et al. Targeting PAK4 promotes Gemcitabine-induced pyroptosis in pancreatic cancer via NLRP1/caspase-3/GSDME axis. Commun Biol 9, 260 (2026). https://doi.org/10.1038/s42003-026-09538-6
Nyckelord: pankreascancer, gemcitabinresistens, pyroptos, PAK4, målinriktad terapi