Clear Sky Science · sv
Fetal reversion från olika härstamningar upprätthåller tarmens stamcellsreserv och ger stresstålighet
Hur tarmen läker sig själv under påfrestning
Tarmens slemhinna är en av kroppens mest aktiva vävnader. Den bryter ner mat, absorberar näringsämnen och skyddar mot mikrober — samtidigt som den förnyas varannan till var tredje dag. Denna artikel undersöker hur den sköra ytan överlever hårda påfrestningar — från inflammation till cellgifter — genom att tillfälligt vrida tillbaka celler till ett mer fosterlikt, flexibelt tillstånd som hjälper tarmen att reparera sig och motstå skador.
Tarmens dagliga monteringslinje
I friska tarmar sitter en specialiserad grupp celler, så kallade crypt base columnar-celler (CBCs), längst ner i små gropar kallade kryptor. Dessa stamcellsliknande celler delar sig konstant och skickar sina avkommor uppåt mot de fingerlika villi som skjuter in i tarmkanalen. Under resan mognar cellerna till olika roller, såsom absorberande enterocyter som tar upp näring, eller sekretoriska celler som producerar slem och antimikrobiella ämnen. Under normala förhållanden håller detta flöde uppifrån och ner slemhinnan förnyad och ordnad.
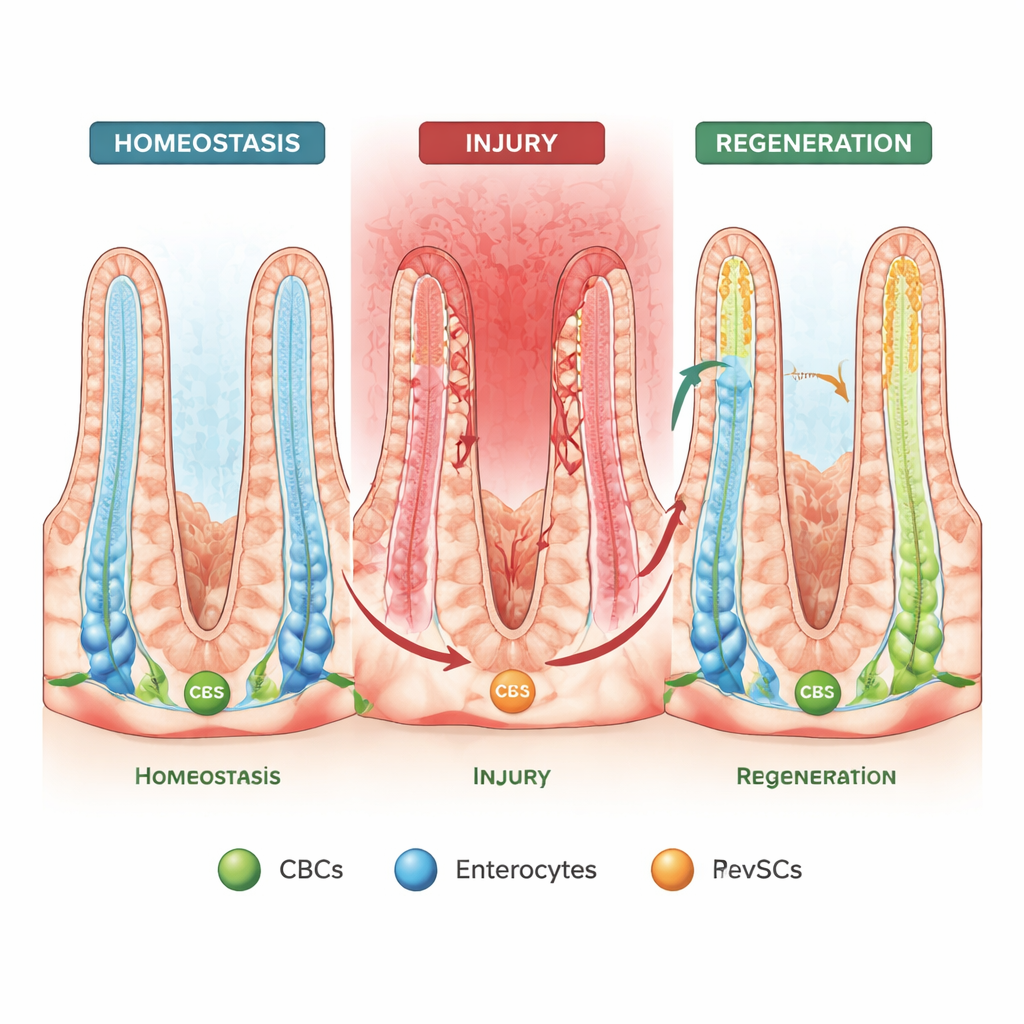
Cellernas förmåga att köra monteringslinjen baklänges
När tarmens slemhinna skadas och CBCs går förlorade visade tidigare arbete att vissa mogna celler kan "gå tillbaka" ner i kryptan och återfå stamcellsegenskaper, ett beteende som kallas spatial plastisitet. Ett annat, nyare fenomen är "fetal reversion", där celler antar ett genaktivitetsmönster som liknar den utvecklande tarmen. I denna studie kopplar författarna samman dessa två idéer med hjälp av avancerade organoidkulturer (mini-tarmar), single-cell RNA-sekvensering och härstamningsspårning i möss. De identifierar en särskild fosterliknande population kallad revival-stamceller (revSCs) som kan uppstå både från CBCs och vanliga absorberande enterocyter, och som sedan kan återskapa ett komplett utbud av tarmsceller.
Mini-tarmar avslöjar dold flexibilitet
För att observera dessa förändringar i realtid odlade teamet mus- och humana intestinala organoider i två olika geléer. I Matrigel uppförde sig organoiderna som normal vuxenvävnad, rik på CBCs och mogna celltyper. I en kollagen-gel dominerades organoiderna däremot av revSC-liknande celler med ett fosterspecifikt genuttryck. Single-cell-analyser visade att revSCs kunde spåras tillbaka längs två huvudsakliga vägar: från klassiska CBCs och från absorberande enterocyter. Sorteringsexperiment bekräftade att CBCs har högst förmåga att omvandlas till revSCs, men även mer mogna celler kunde göra det när de placerades i rätt miljö. Avgörande var att renade revSCs kunde flyttas tillbaka till Matrigel och då regenerera CBCs och alla huvudsakliga tarmlinjer, vilket visar att det fosterlika tillståndet både är reversibelt och fullt funktionellt.
Villusceller och verkliga skador
Studien går ett steg längre genom att fråga om denna flexibilitet också uppträder utanför laboratoriet. Forskarna märkte enterocyter i villi hos möss och odlade sedan antingen villusfragment eller exponerade djuren för ett tarmskadande cellgift, 5-fluorouracil (5-FU). I kollagen bildade villusfragment — normalt betraktade som fattiga på stamceller — nya organoider som antog revSC-egenskaper och senare återfick CBC-markörer när de förflyttades tillbaka till standardförhållanden. När dessa "villusderiverade" organoider transplanterades i kolitmodeller återuppbyggde de frisk tarmepitel. I levande möss behandlade med 5-FU började märkta enterocyter uttrycka revSC-markörer och senare framträdde de som långa klonala band som inkluderade nya CBCs vid kryptans bas, vilket bekräftar att mogna celler trätt in för att fylla på stamcellsbassängen.
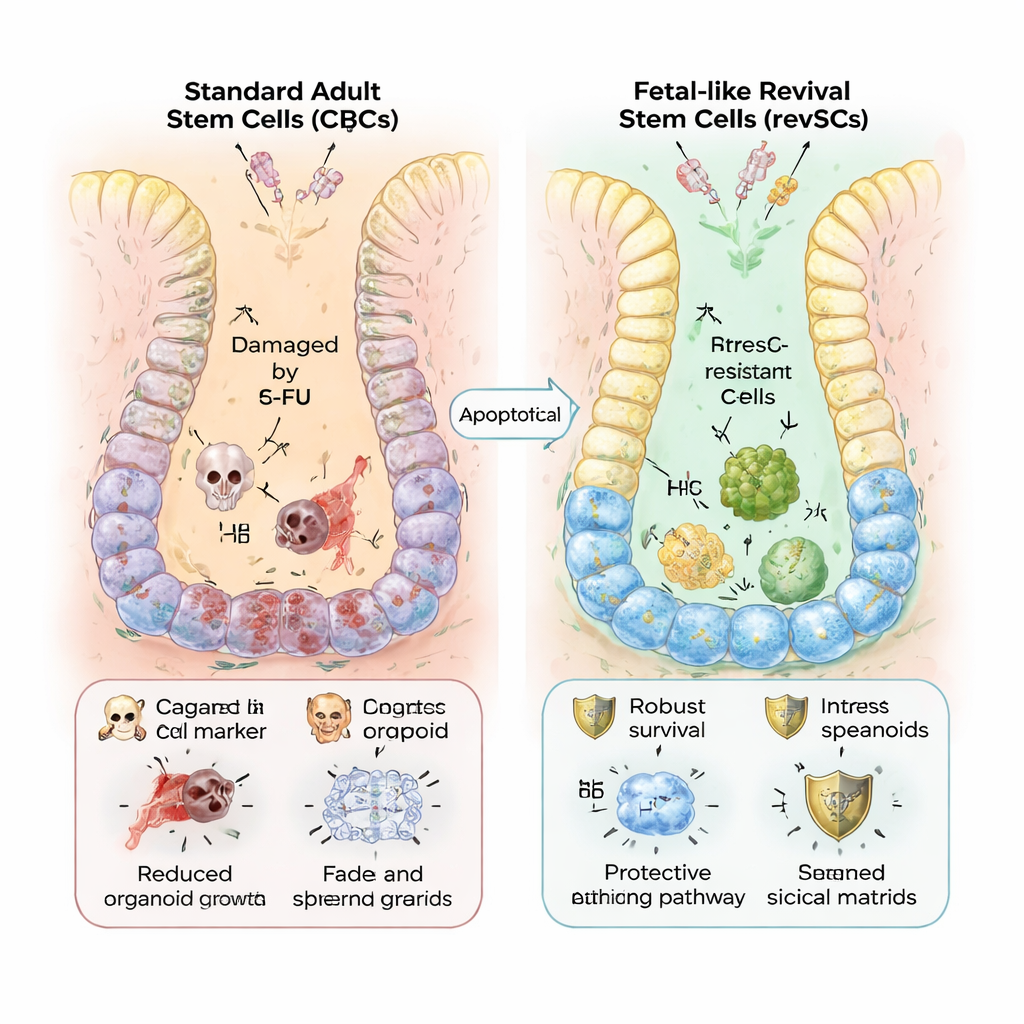
Stresståliga reparationsgrupper
Varför ta omvägen via ett fosterliknande tillstånd? Författarna visar att revSCs är mycket bättre på att tåla stress. När organoider utmanades med 5-FU krympte de som odlades i standard-Matrigel och visade breda genprogram kopplade till DNA-skada och hetsigt proliferativt svar. Organoider odlade i kollagen och rika på revSCs fortsatte däremot att växa och uppvisade ett lugnare, mer riktat svar. Genanalyser visade högre aktivitet i antioxidantssystem, anti-dödsproteiner och värmechock-chaperoner — molekylära sköldar som hjälper celler att överleva inflammation och toxiska angrepp. Liknande mönster observerades i både mus- och humana celler, och samma revSC-gener är förhöjda i inflammerade mänskliga tarmar.
Vad detta betyder för tarmsjukdom och terapi
För en icke-specialist är slutsatsen att tarmens slemhinna har en inbyggd nödbroms. När inflammation eller läkemedel hotar dess vanliga stamceller kan både stamceller och vanliga absorberande celler tillfälligt återgå till ett fosterliknande, stresståligt revSC-tillstånd. Därifrån kan de återskapa den normala stamcellsplattformen och bygga upp vävnaden igen. Detta arbete förenar två regenerationsbegrepp — spatial plastisitet och fetal reversion — i en enda reparationshierarki, och antyder att man med försiktighet skulle kunna utnyttja detta flexibla, fosterlika program för att förbättra behandlingar av tillstånd som inflammatorisk tarmsjukdom och kolorektal cancer, samtidigt som det varnar för att missriktad reversion kan driva tumörtillväxt.
Citering: Kirino, S., Uefune, F., Miyake, K. et al. Fetal reversion from diverse lineages sustains the intestinal stem cell pool and confers stress resilience. Commun Biol 9, 255 (2026). https://doi.org/10.1038/s42003-026-09533-x
Nyckelord: tarmstamceller, vävnadsregeneration, cellplastisitet, inflammatorisk tarmsjukdom, organoider