Clear Sky Science · sv
Fluvastatin undertrycker initiering och progression av bröstcancer genom att rikta in sig på CYP4Z1
Varför ett kolesteroldrog spelar roll för bröstcancer
Många kvinnor som behandlas för bröstcancer utvecklar onormala blodfettvärden och löper en fortsatt risk för att sjukdomen återkommer eller sprider sig. Denna studie undersöker en intressant tanke: kan en vanlig kolesterolsänkande tablett, fluvastatin, återanvändas för att bromsa eller förebygga bröstcancer genom att oskadliggöra ett protein som driver särskilt farliga, stamcellsliknande tumörceller?
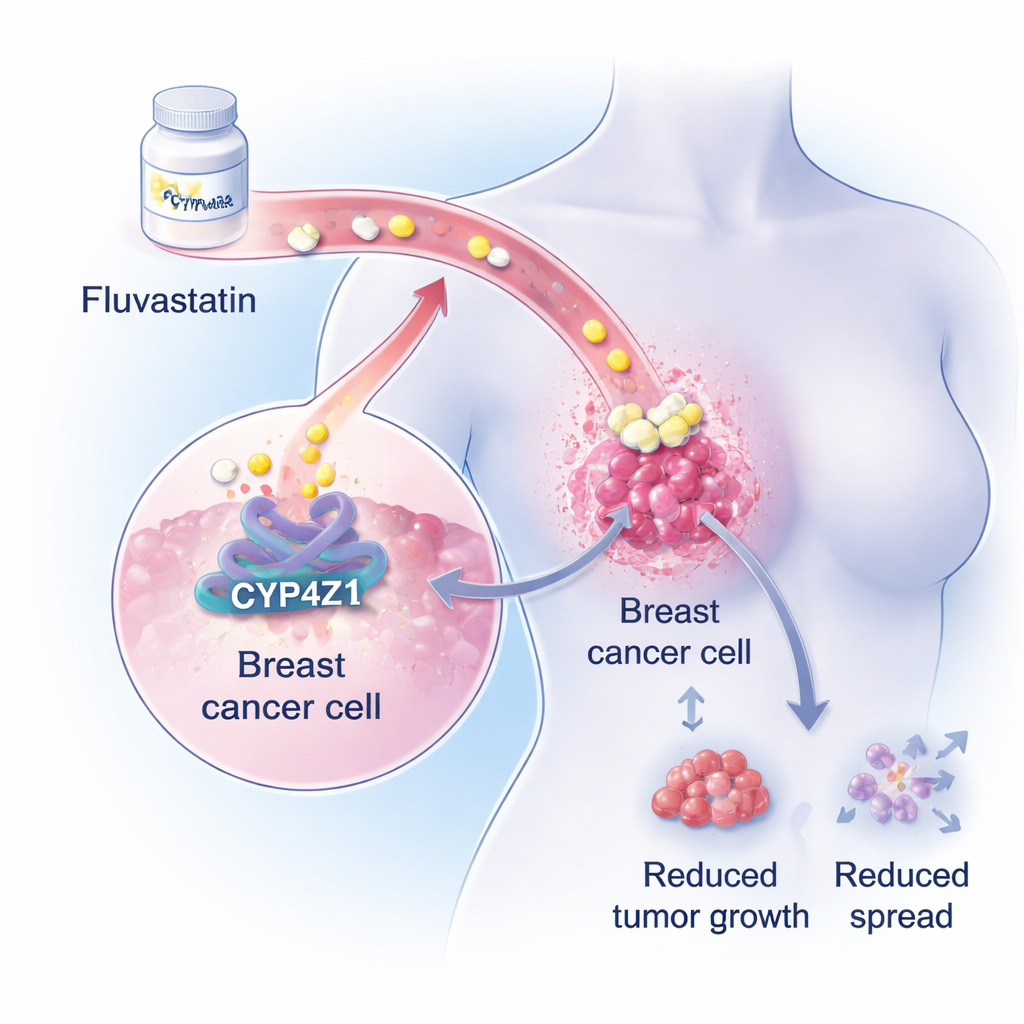
En dold drivkraft inne i brösttumörer
Forskarna fokuserar på ett lite känt protein kallat CYP4Z1, som finns i höga nivåer i bröstcancerceller men inte i frisk bröstvävnad. Tidigare arbete visade att CYP4Z1 får cancerceller att bete sig mer som stamceller — celler som kan förnya sig oändligt, motstå cytostatika och återstarta tumörer efter behandling. I omfattande genetiska och biokemiska analyser visar teamet nu att överaktivt CYP4Z1 kraftigt förstärker fettbyggande vägar inne i bröstcancerceller, särskilt produktionen av triglycerider, en huvudlagringsfett. Eftersom många bröstcancerpatienter redan utvecklar rubbade blodfetter under cytostatikabehandling antydde denna fettfrämjande roll för CYP4Z1 en möjlighet för befintliga lipidsänkande läkemedel.
Att återanvända fluvastatin från hjärthälsa till cancerbehandling
För att pröva denna idé screenade forskarna ett litet bibliotek med 23 FDA‑godkända läkemedel som används för att sänka blodfetter. Fluvastatin, en allmänt förskriven statin för högt kolesterol, framträdde som en tydlig kandidat: det blockerade direkt CYP4Z1:s enzymaktivitet på ett dosberoende sätt. Vid doser som var mycket mindre skadliga för normala bröstkörtelceller än för cancerceller minskade fluvastatin kraftigt viktiga markörer för stamcellslikhet, cancercellernas förmåga att bilda fria ”tumörsfärer” och deras kapacitet att migrera och invadera genom vävnadsliknande barriärer i laboratorietester. Det gjorde också tumörceller mer känsliga för cytostatikumet adriamycin, vilket antyder att det kan förbättra befintliga behandlingar.
Att testa läkemedlet i levande djur
Teamet utvärderade därefter fluvastatin i musemodeller. Hos möss som implanterats med humana bröstcancerceller saktade periodisk fluvastatinbehandling tumörtillväxten, sänkte nivåerna av en markör för stamcellslikhet (ALDH1A1) och delningsmarkören Ki67 i tumörerna, och minskade antalet metastatiska noduli som dök upp i lungorna. Viktigt är att möss som fick fluvastatin bibehöll sin kroppsvikt och visade inga större avvikelser i blod eller benmärg, vilket talar för en gynnsam säkerhetsprofil vid den testade dosen. I en mer realistisk genetisk modell — möss konstruerade för att utveckla brösttumörer drivna av ett cancerframkallande gen — introducerade forskarna dessutom human CYP4Z1 i bröstmuskeln. Dessa möss utvecklade fler för‑cancerösa och cancerösa lesioner samt fler lever‑ och lungmetastaser än kontrollmöss. Fluvastatinbehandling minskade avsevärt både antalet bröstlesioner och avlägsna metastaser, särskilt i möss som bar den extra CYP4Z1‑genen.
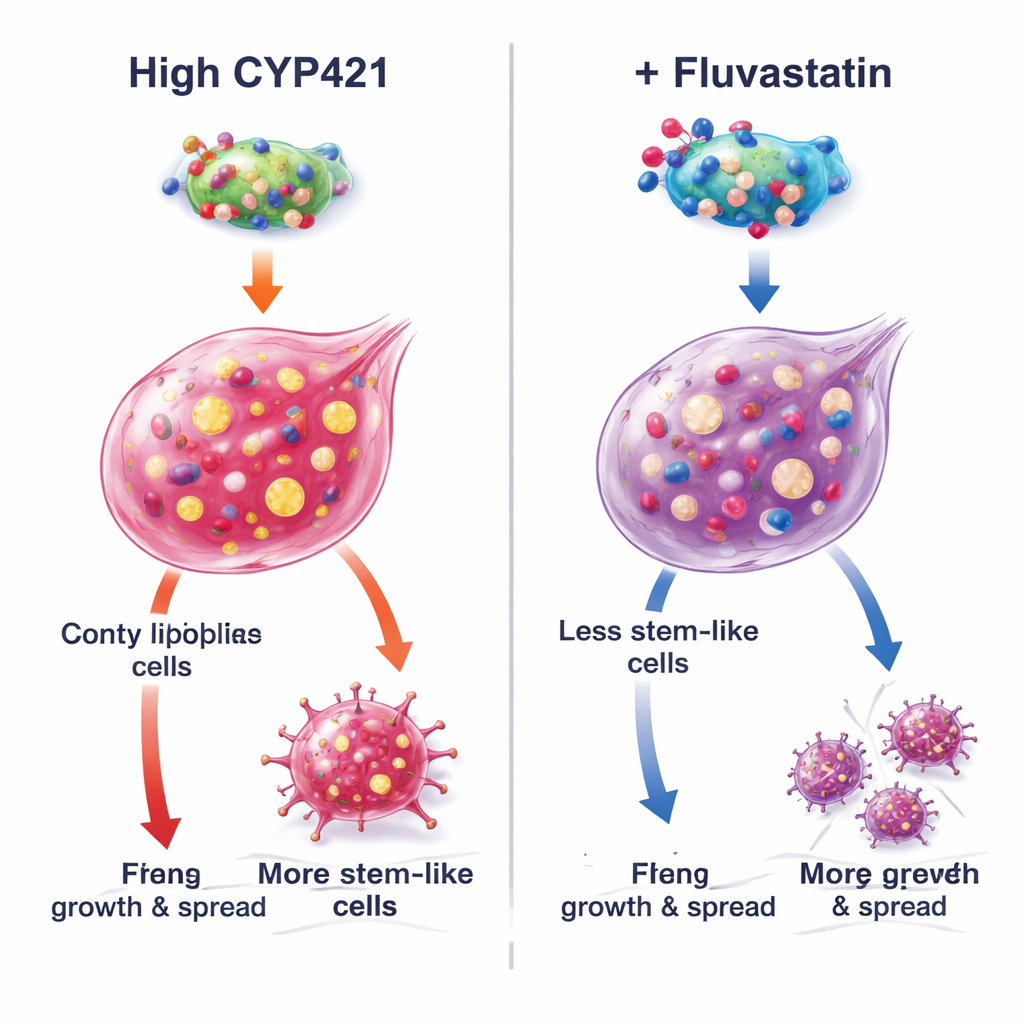
Hur fluvastatin oskadliggör ett cancerfrämjande protein
För att förstå mekanismen kombinerade författarna datorbaserad modellering med exakt proteinengineering. De förutspådde att fluvastatin kilas in i CYP4Z1:s aktiva säte vid tre kritiska aminosyror (Lys109, Pro444 och Arg450). När dessa positioner muterades föll CYP4Z1:s aktivitet och fluvastatin kunde inte längre hämma den ytterligare, vilket bekräftar dessa platser som inbindningspunkter. I celler som naturligt saknar CYP4Z1 ökade tillsats av det normala proteinet stamcellsegenskaper och aktiverade den tillväxtfrämjande PI3K/AKT‑signaleringen, medan fluvastatin vände dessa effekter. Mutanta varianter av CYP4Z1 var mindre potenta och mindre responsiva på läkemedlet. Ytterligare experiment visade att fluvastatins effekt försvagades när triglyceridproduktionen artificiellt ökades, eller när CYP4Z1 nedreglerades, vilket understryker att läkemedlets starkaste effekter kommer från blockering av detta specifika protein och dess fettbyggande följder snarare än från att utlösa celldöd genom järndriven "ferroptos."
Vad detta betyder för patienter
Sammantaget tyder studien på att fluvastatin, utöver att sänka kolesterol, kan hämma de tidigaste stadierna och senare spridningen av bröstcancer i experimentella modeller genom att rikta in sig på CYP4Z1, ett protein som driver fettmetabolism och stamcellsliknande beteende i tumörer. Eftersom fluvastatin redan är godkänt och dess säkerhet är väl kartlagd erbjuder dessa fynd en lovande väg mot snabbare klinisk prövning som tilläggsbehandling, särskilt hos patienter vars tumörer starkt uttrycker CYP4Z1. Även om mer arbete krävs för att pröva detta tillvägagångssätt hos människor och för att identifiera eventuella ytterligare mål för läkemedlet, öppnar forskningen dörren för att använda ett välbekant hjärtmedel som en del av en ny strategi mot aggressiva, återfallsbenägna bröstcancerformer.
Citering: Li, H., Chen, Y., Shi, W. et al. Fluvastatin suppresses breast cancer initiation and progression via targeting CYP4Z1. Commun Biol 9, 254 (2026). https://doi.org/10.1038/s42003-026-09532-y
Nyckelord: bröstcancer, fluvastatin, cancerstamceller, lipidmetabolism, läkemedelsomplacering