Clear Sky Science · sv
Differentierat uttryckta miRNA i tinningbarken hos patienter med Alzheimers sjukdom och deras koppling till tau-patologi
Varför små hjärnströmbrytare spelar roll vid Alzheimer
Alzheimers sjukdom berövar människor minnet och självständigheten i en långsam process, men vi saknar fortfarande behandlingar som stoppar eller vänder förloppet. Denna studie undersöker några av hjärnans minsta kontrollströmbrytare — korta RNA-molekyler kallade microRNA — som påverkar vilka proteiner cellerna tillverkar. Genom att studera hjärnvävnad från personer med Alzheimer frågade forskarna om förändringar i dessa microRNA hänger samman med en central sjukdomsegenskap: ansamling och spridning av abnormt tau-protein inne i nervceller.
Att läsa budskap i en sårbar hjärnregion
Gruppen fokuserade på tinningbarken, en region viktig för språk och minne som drabbas hårt vid Alzheimer. Efter döden samlades prov från 36 individer — 13 utan Alzheimer och 23 med sjukdomen — från två europeiska hjärnbanker. Forskarna extraherade RNA från vävnaden och använde höggenomströmningssekvensering för att räkna hundratals olika microRNA. Eftersom hjärnvävnad försämras efter döden kontrollerade de noggrant RNA-kvaliteten och valde 19 prover med acceptabel integritet för den mest detaljerade analysen, och använde sedan alla 36 prover för att bekräfta sina huvudresultat.
Upptäckt av en microRNA-signatur för Alzheimer
Bland 449 upptäckta microRNA framträdde 13 som konsekvent förändrade i tinningbarken hos Alzheimerpatienter. Åtta var minskade och fem ökade jämfört med kontrollhjärnor. Flera av de starkaste signalerna involverade microRNA som redan misstänkts spela roll vid Alzheimer: miR-129-5p, miR-132-3p och miR-146b-5p var alla lägre, medan miR-151a-5p var högre. Dessa molekyler är rikliga i hjärnan och är kända för att reglera gen-nätverk som är viktiga för neuronernas hälsa. Med en andra, mer riktad teknik (RT-qPCR) validerade författarna att dessa samma microRNA förändrades i samma riktning, även när de inkluderade prover med lägre kvalitet, vilket stärker förtroendet för att mönstret är verkligt.
Koppla små strömbrytare till förvärrade tau-trassel
Alzheimers svårighetsgrad i hjärnan graderas ofta med Braak-stadie, som speglar hur långt tau-trassel spridit sig genom olika regioner. Forskarna fann att nivåerna av miR-129-5p, miR-132-3p och miR-146b-5p sjönk stadigt i takt med ökat Braak-stadie, medan miR-151a-5p tenderade att öka. De mätte också direkt en starkt fosforylerad, trasselbenägen form av tau i samma prover. Hjärnor med mer av detta abnorma tau visade samma mönster: mindre miR-129-5p, miR-132-3p och miR-146b-5p, och mer miR-151a-5p. Med andra ord följde microRNA-förändringarna både mikroskopisk stadieindelning och biokemiska tecken på tau-patologi, vilket antyder att de är nära kopplade till sjukdomsprocessen snarare än slumpmässiga åskådare.
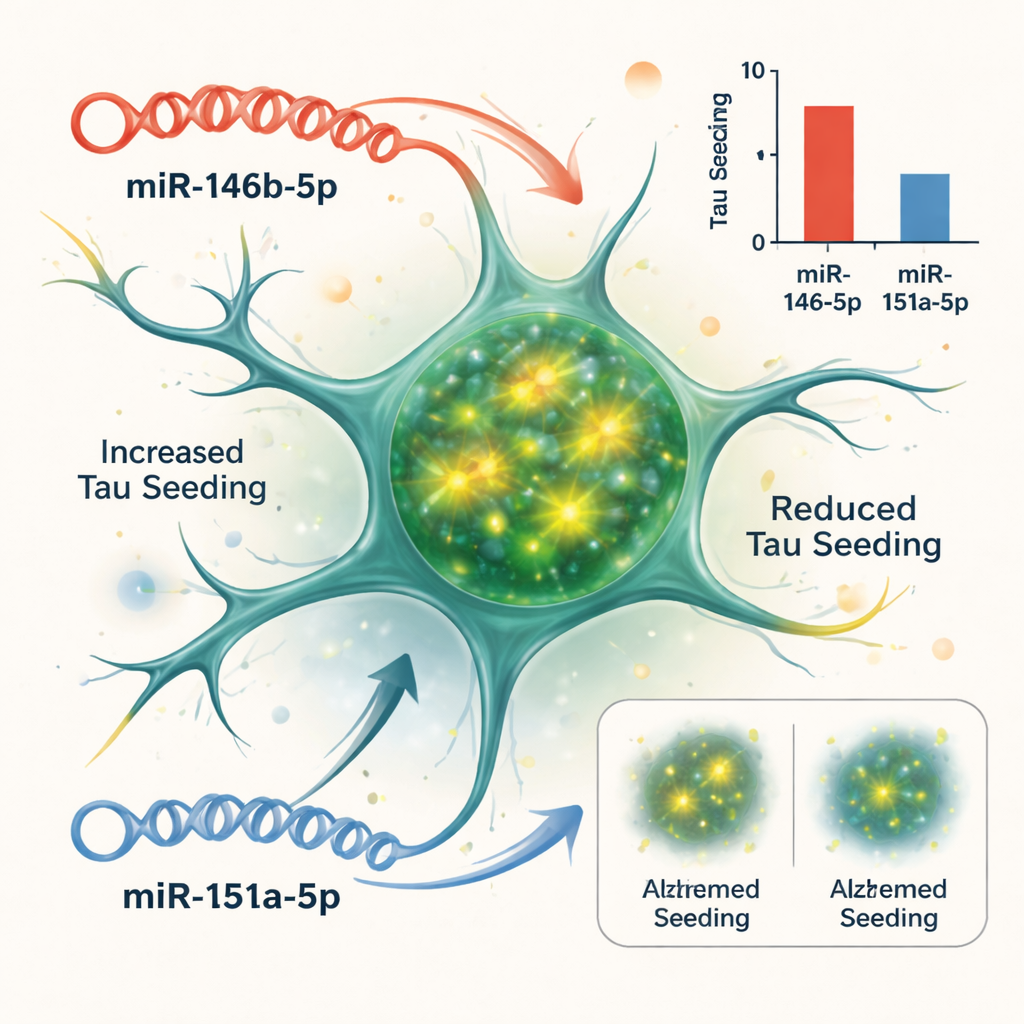
Test av orsak och verkan i en cellmodell
Korrelation bevisar inte att microRNA driver sjukdom, så gruppen använde ett cellbaserat system som rapporterar hur lätt tau-aggregat kan ”så” nya klumpar. De använde biosensorceller konstruerade för att lysa upp när tau-fibriller bildas inuti dem. När de tillsatte tau-rik vävnad från Alzheimer-hjärnor gav cellerna en stark fluorescenssignal. Genom att öka eller blockera specifika microRNA i dessa celler kunde forskarna se vilka som förändrade denna tau-seeding. Två utmärkte sig: att öka miR-146b-5p förvärrade tau-seeding, medan blockade minskade seeding; i motsats minskade ökningar av miR-151a-5p tau-seeding, medan hämning gjorde seedingen mer robust. Andra testade microRNA hade liten effekt i detta assay.
Vad detta kan innebära för framtida diagnos och behandling
För att förstå vad dessa microRNA kan göra använde författarna beräkningsverktyg för att kartlägga deras förutsagda gentargets i kända biologiska vägar. De nedreglerade microRNA — särskilt miR-129-5p, miR-132-3p och miR-146b-5p — kopplades till nätverk involverade i nervcellsöverlevnad, kemisk signalering vid synapser och Alzheimers-relaterade vägar. Detta tyder på att förlusten av deras normala ”bromsande” inflytande kan störa flera skyddssystem samtidigt, medan ökningen av miR-151a-5p kan representera ett sent, partiellt försök av hjärnan att motverka tau-aggregation. Även om detta arbete bygger på postmortem-vävnad och förenklade cellmodeller, stärker det idén att specifika microRNA både speglar och modulerar tau-patologi. I längden skulle mätning av dessa molekyler i cerebrospinalvätska eller blod kunna hjälpa till att följa sjukdomens förlopp, och att noggrant justera deras nivåer i hjärnan kan erbjuda en ny väg för att bromsa eller förhindra spridningen av toxisk tau.
Citering: Nagaraj, S., Quintanilla-Sánchez, C., Ando, K. et al. Differentially expressed miRNAs in the temporal cortex of Alzheimer’s disease patients and their association to tau pathology. Commun Biol 9, 253 (2026). https://doi.org/10.1038/s42003-026-09530-0
Nyckelord: Alzheimers sjukdom, microRNA, tau-patologi, tinningbarken, neurodegeneration