Clear Sky Science · sv
Målstyrd blockering av gen-splitsning kan rubba primära mikroRNA inbäddade i introner
Dolda budskap inne i våra gener
Många nya genterapier verkar genom att påverka våra cellers RNA-meddelanden, men dessa RNA bär ofta på extra ”anteckningar i marginalen” som forskare bara börjar förstå. Denna studie visar att läkemedel utformade för att korrigera felaktig splitsning av gener av misstag kan öka små reglerande RNA som ligger begravda i introner—de icke-kodande regionerna mellan gensegmenten—med överraskande effekter på hjärnans konnektivitet och utveckling.
Genterapier som skriver om RNA
Antisense-oligonukleotider, eller ASO:er, är korta syntetiska bitar av genetiskt material som fäster vid RNA och ändrar hur det läses eller bearbetas. Flera ASO:er testas redan eller används för sällsynta genetiska sjukdomar, särskilt sådana som beror på fel i hur RNA splitsas—steget som syr ihop kodande segment av en gen. De flesta säkerhetstester fokuserar på om en ASO återställer rätt protein och undviker uppenbara biverkningar. Men många gener bär också icke-kodande RNA, inklusive mikroRNA, inuti sina introner. Dessa små molekyler kan kraftigt finjustera genaktivitet, och upp till hälften av kända mikroRNA i ryggradsdjur härrör från introner. Den nya studien frågar: vad händer med dessa inbäddade mikroRNA när vi tvingar fram ändrad splitsning med ASO:er?
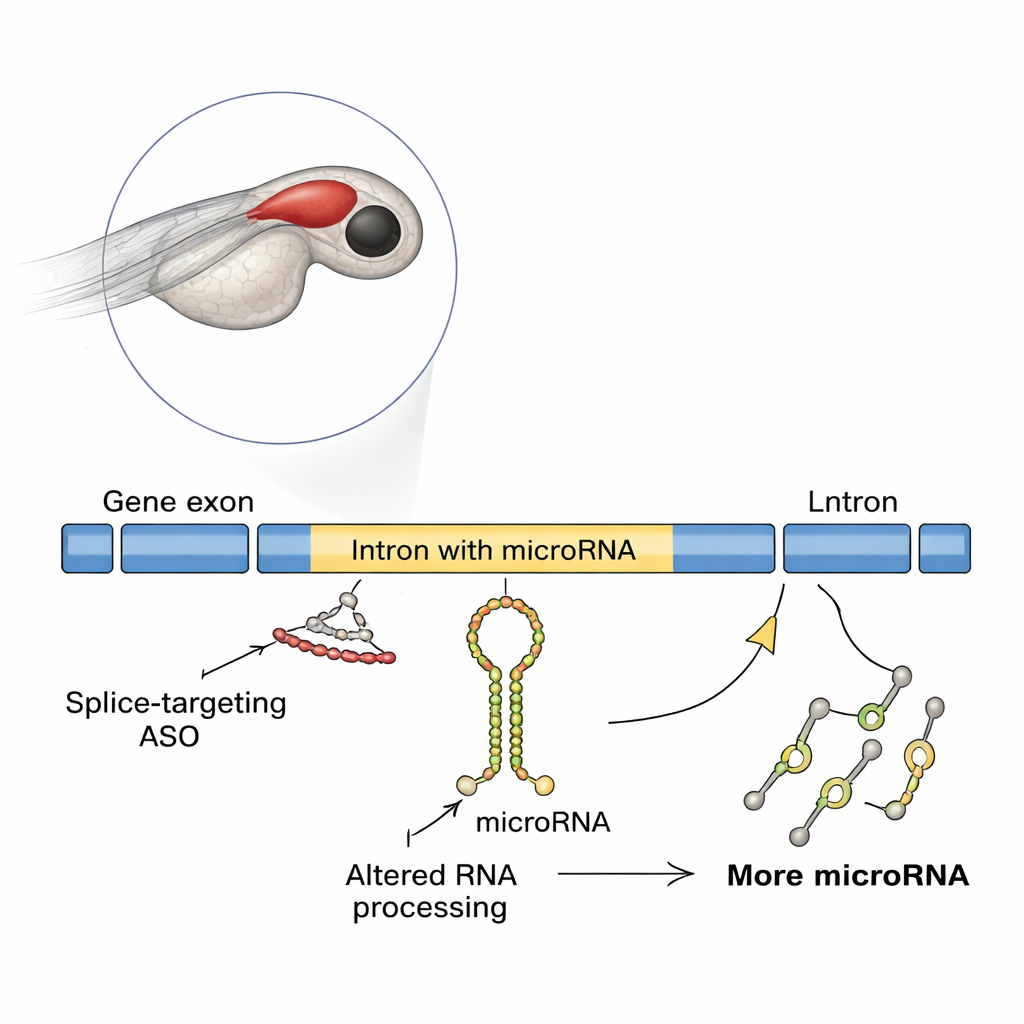
En överraskande effekt i utvecklande fiskhjärnor
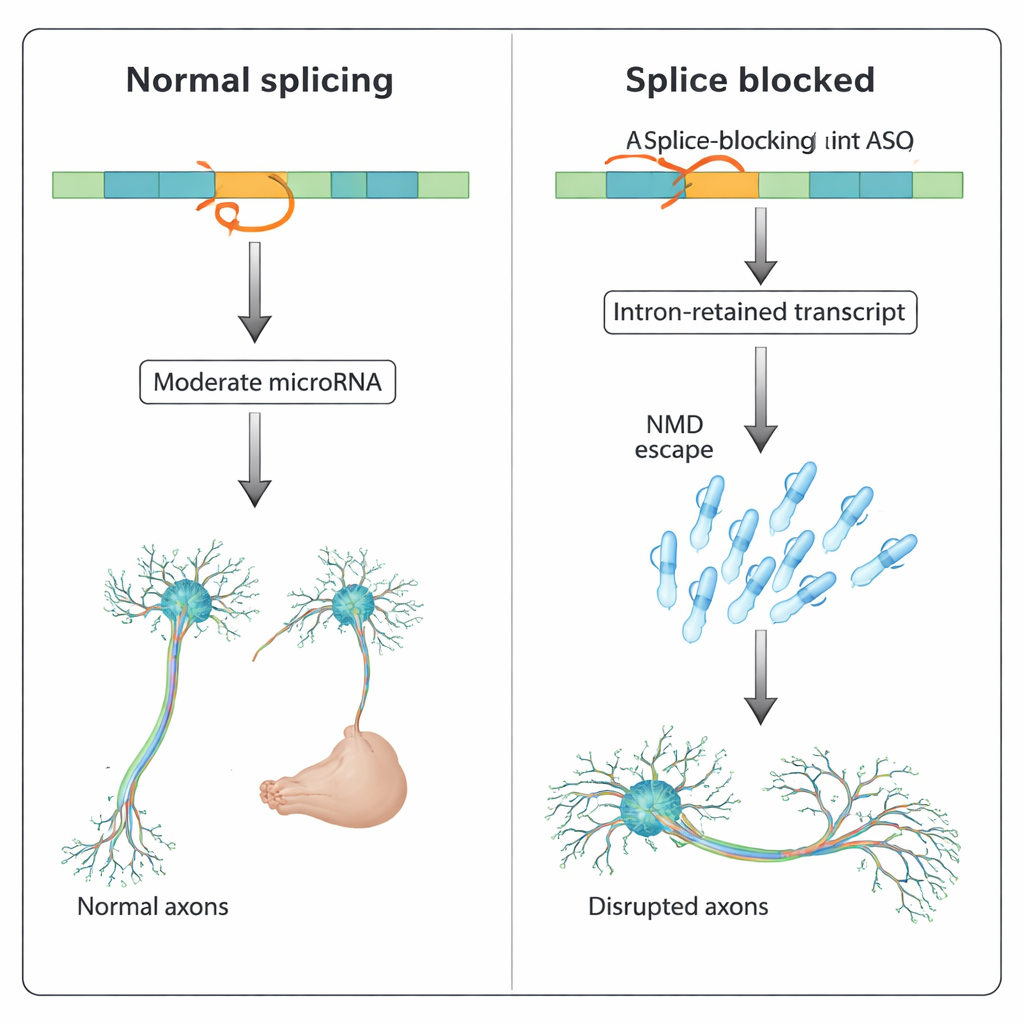
Forskarna använde zebrafisk, en populär ryggradsmässig modell vars genomskinliga embryo gör det lätt att följa hjärnans utveckling. De fokuserade på en gen kallad slit3, som hjälper till att vägleda nervfibrer och innehåller ett mikroRNA kallat mir-218a-1 inne i en av sina introner. När teamet blockerade starten av slit3-translation såg utvecklingen av hormonutsöndrande hypofysaxoner normal ut. Men när de använde en annan ASO som blockerade splitsning vid en specifik slit3-splitsningsplats minskade de axoner som skulle projicera till bakre hypofysen drastiskt, även om antalet oxytocinproducerande neuroner var oförändrat. Molekylära tester visade att denna splitsningsblockerande ASO orsakade intronretention i genens RNA, oväntat ökade nivåerna av slit3-transkriptet, dess långa intron och det intron-inbäddade primära mir-218a-1-transkriptet.
MikroRNA, inte förlust av protein, driver defekterna
För att reda ut vad som orsakade axelproblemet jämförde författarna flera scenarier. Att blockera moget mir-218a-1 ensam ändrade inte slit3-nivåerna, och en separat ASO riktad mot en annan splitsningsplats nära mikroRNA:t gav varken axonala defekter eller en ökning av mir-218a-1. Avgörande var att när den splitsningsblockerande slit3-ASO:n kombinerades med en ASO som neutraliserar mir-218a-1 återhämtade sig axonal koppling till stor del. På samma sätt orsakade inte samma splitsningsblockerande slit3-ASO längre axonala defekter hos zebrafisk genetiskt saknande mir-218a-1, medan injektion av en syntetisk mir-218a-mimik kunde återskapa fenotypen i normala fiskar. Dessa experiment pekar mot förhöjt intronalt mikroRNA—snarare än ett trunkerat Slit3-protein—som den huvudsakliga orsaken till utvecklingsstörningen.
Ett bredare mönster över flera gener
Teamet frågade sedan om denna effekt är unik för slit3. De sökte i zebrafiskgenomet och fann dussintals proteinkodande gener som hyser intronala mikroRNA, många involverade i utveckling och signalering. Två sådana gener, pank2 och dnm2a, hade tidigare visat allvarliga utvecklingsproblem när deras splitsning blockerades av ASO:er, inklusive hjärnvätskeansamling, hjärtsvullnad och kroppsfel—problem som genetiska knockouter av samma gener inte återgav. I denna studie räddade samtidig injektion av ASO:er som specifikt blockerade de intronala mikroRNA:n mir-103 (i pank2) eller mir-199-5p (i dnm2a) delvis dessa ASO-inducerade fenotyper. I vissa fall återställde mikroRNA-blockaden också värdgenens uttryck, medan den i andra fall inte gjorde det, vilket tyder på att förhöjd mikroRNA-aktivitet i sig kan vara skadlig även när de övergripande nivåerna ändras bara måttligt.
Vad detta betyder för framtida behandlingar
Resultaten visar att splitsningsinriktade ASO:er kan göra mer än att orsaka exonskippning eller intronretention: de kan stabilisera intronretainerade transkript som undkommer cellens kvalitetskontroll och öka primära intronala mikroRNA, vilka sedan felreglerar nätverk av målgener. I utvecklande neuroner kan sådan okontrollerad mikroRNA-aktivitet förvränga axontillväxt och kopplingar. För läkemedelsutvecklare innebär detta att ovanliga eller ”off-target” fenotyper i djurtester kanske inte alltid härrör från generella toxikologiska vägar som p53-aktivering, utan från oavsiktliga effekter på dolda intronala RNA. Noggrann jämförelse mellan translationsblockerande och splitsningsblockerande ASO:er, samt övervakning av intronala mikroRNA-uttryck, kan hjälpa till att upptäcka dessa risker tidigt och förfina ASO-design innan de når patienter.
Citering: Ali, M.H., Ramesh, A.R., Nedunchezhian, N. et al. Targeted blocking of gene splicing can dysregulate intron-embedded primary microRNAs. Commun Biol 9, 252 (2026). https://doi.org/10.1038/s42003-026-09529-7
Nyckelord: antisense-oligonukleotider, mikroRNA, RNA-splitsning, zebrafiskutveckling, säkerhet vid genterapi