Clear Sky Science · sv
Nimbolide förbättrar ARDS och ulcerös kolit genom att störa aktiveringen av NLRP3‑inflammasomen
Varför det är viktigt att dämpa okontrollerad inflammation
Många allvarliga sjukdomar, från livshotande lungsvikt till smärtsam tarmsjukdom, drivs inte bara av mikrober eller skador utan av kroppens eget immunsystem som går på övervarv. Denna studie undersöker om en naturlig förening kallad nimbolide, utvunnen från neemträdet, kan fungera som en precis "broms" på en kraftfull inflammatorisk maskin inne i våra immunceller och därigenom öppna en säkrare väg för behandling av tillstånd som akut respiratoriskt distressyndrom (ARDS) och ulcerös kolit.
En besvärlig larmfunktion inne i immunceller
I centrum för denna berättelse står ett molekylärt larmsystem kallat NLRP3‑inflammasomen. När immunceller känner fara — signaler från infektioner, skadat vävnad eller kristaller — kan det snapas ihop som en Lego‑struktur bestående av tre delar: sensorn NLRP3, adaptern ASC och enzymet Caspase‑1. När komplexet väl bildats aktiverar det potenta budbärarmolekyler såsom IL‑1β och IL‑18 och kan utlösa en brännande form av celldöd kallad pyroptos. Medan denna reaktion hjälper till att rensa bort hot, bidrar överaktivering till kroniska och akuta sjukdomar, inklusive artrit, diabeteskomplikationer, Alzheimers sjukdom, ARDS och inflammatorisk tarmsjukdom. Läkemedelsutvecklare har försökt tygla NLRP3 med syntetiska föreningar, men många kandidater har fallit på grund av toxicitet, biverkningar eller dålig farmakologisk profil, vilket skapar ett tydligt behov av säkrare och mer selektiva inhibitorer.
Upptäckt av en potent växtbaserad inhibitor
Forskarlaget screenade 126 naturliga föreningar för att se vilka som bäst blockerade IL‑1β‑frisättning från musimmunceller. Nimbolide framträdde som särskilt effektiv och minskade IL‑1β‑sekretionen med mer än 80 % vid testade doser. Ytterligare experiment visade att nimbolide kraftigt minskade aktivering av Caspase‑1, frisättning av IL‑1β och pyroptotisk celldöd i makrofager härledda från musbenmärg, med potens liknande en referensförening kallad MCC950. Viktigt är att nimbolide inte dämpade frisättningen av andra immunsignaler som IL‑6, vilket tyder på att det verkar fokuserat snarare än att slå av immunsystemet generellt. När det testades mot olika triggers som alla aktiverar NLRP3 — såsom ATP, nigericin, alumkristaller och imiquimod — minskade nimbolide konsekvent inflammasomaktiviteten, även i humana THP‑1‑celler. Däremot blockerade det inte två närliggande inflammasomer, AIM2 och NLRC4, vilket framhäver dess specificitet för NLRP3.
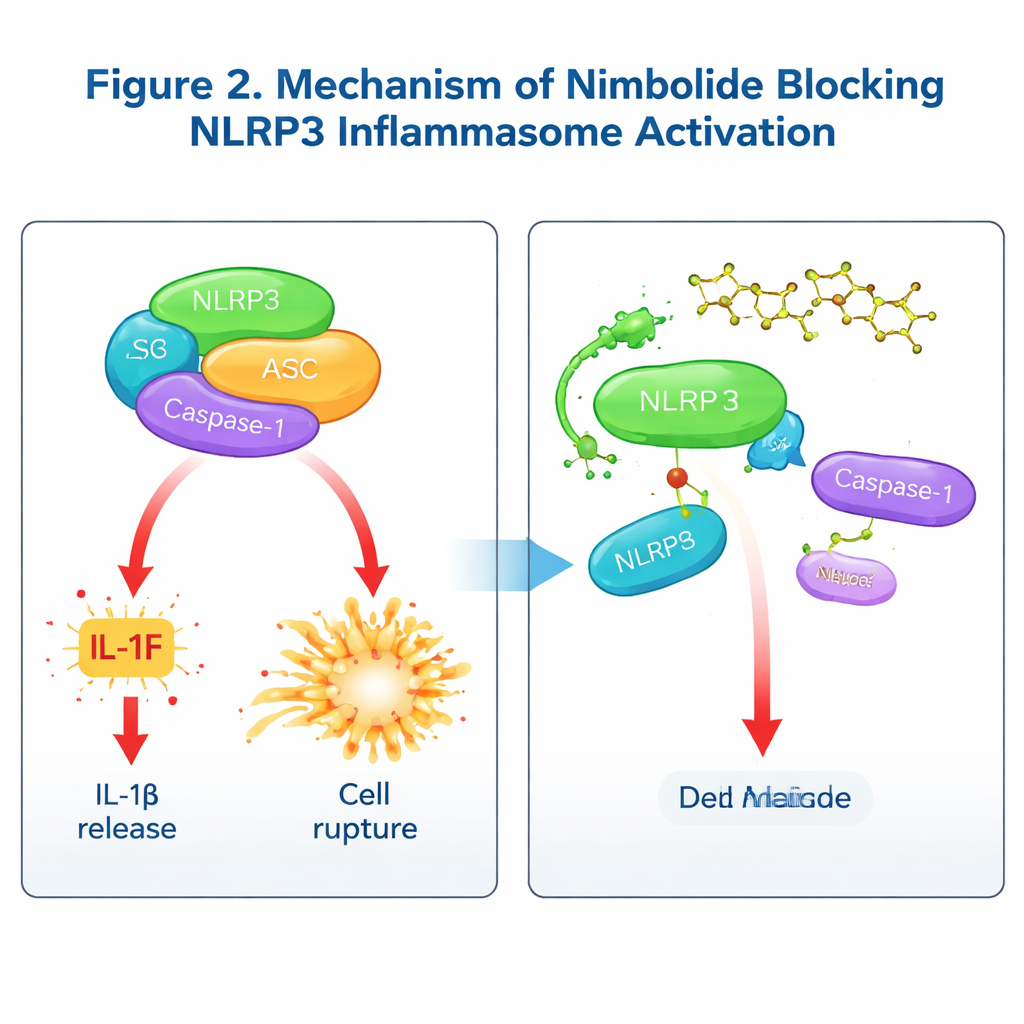
Hur nimbolide blockerar den inflammatoriska maskinen
För att förstå hur nimbolide verkar undersökte teamet om det stör tidiga "priming"‑steg styrda av NF‑κB‑vägen, eller senare skeden när inflammasomen fysiskt monteras. Kortvarig behandling, given efter priming, lämnade nyckelsignaler och genuttryck i primingfasen intakta men minskade ändå IL‑1β och Caspase‑1‑aktivering, vilket visar att nimbolide främst verkar på monteringssteget. Detaljerade biokemiska tester visade att nimbolide inte påverkar kalium‑ eller kalciumflöden, mitokondriell skada eller interaktionen mellan NLRP3 och dess hjälpprotein NEK7. Istället stör det det avgörande handslaget mellan NLRP3 och ASC, minskar ASC‑klustring till specks och förhindrar att NLRP3 bildar högre ordnings oligomerer. Genom bindningsanalyser och molekylär modellering visade författarna att nimbolide binder direkt till NACHT‑regionen i NLRP3 vid en specifik aminosyra, Lys565. När denna plats muterades kunde nimbolide inte längre skydda NLRP3 från nedbrytning eller bryta dess koppling till ASC, vilket bekräftar Lys565 som den viktiga dockingpunkten. Noterbart är att medan andra läkemedel ofta riktar sig mot NLRP3:s ATPas‑aktivitet, blockerar nimbolide monteringen utan att påverka ATP‑användningen, vilket ger en distinkt verkningsmekanism.
Test av nimbolide vid lungsjukdom och tarmsjukdom
Laget undersökte sedan om denna molekylära effekt översätts till verkligt skydd i sjukdomsmodeller. I möss som fick ett bakterietoxin för att inducera ARDS minskade nimbolide‑behandling före skadan lungvävnadsskador, vätskeansamling och läckage av protein in i luftutrymmena. Det fanns färre invaderande immunceller i lungorna och lägre nivåer av IL‑1β i både lungvävnad och blod. Liknande fördelar sågs i en modell där toxinet levererades direkt till luftvägarna. I en separat modell för ulcerös kolit, där möss drack en kemikalie som skadar kolon, begränsade nimbolide viktminskning, förbättrade avföringskonsistens och blödningspoäng, bevarade kolonlängd och minskade mikroskopiska tecken på inflammation och vävnadsnedbrytning, samtidigt som IL‑1β i kolon sänktes. Avgörande var att i genetiskt modifierade möss som saknar NLRP3 var sjukdomen redan mildare och nimbolide gav ingen ytterligare nytta, vilket understryker att dess skyddande effekter beror på att blockera NLRP3.
Vad detta kan innebära för framtida behandlingar
För icke‑specialister är huvudlärdomen att nimbolide fungerar som en smart broms på en av kroppens mest kraftfulla inflammatoriska strömbrytare. Genom att fästa vid en exakt plats på NLRP3 och förhindra att inflammasomen snäpper ihop sig, lugnar det överdriven inflammation i både lungor och tarm utan att brett stänga av immunförsvaret. Medan nimbolide i sig fortfarande behöver förbättras vad gäller till exempel stabilitet och leverans innan det kan bli ett läkemedel, positionerar denna forskning det som en lovande utgångspunkt — och en ritning — för att utforma nästa generationens läkemedel mot NLRP3‑drivna sjukdomar såsom ARDS och ulcerös kolit.
Citering: Xu, H., Lin, Y., Luo, W. et al. Nimbolide ameliorates ARDS and ulcerative colitis by disrupting NLRP3 inflammasome activation. Commun Biol 9, 246 (2026). https://doi.org/10.1038/s42003-026-09524-y
Nyckelord: nimbolide, NLRP3 inflammasom, inflammation, acute respiratory distress syndrome, ulcerös kolit