Clear Sky Science · sv
MAT2A ökar PARN-transkription via SRF för att snabba upp glykolys och driva malign progression i osteosarkom
Varför denna studie om bencancer är viktig
Osteosarkom är den vanligaste bencancern hos barn och tonåringar, och behandlingsalternativen har knappt förändrats på årtionden. Många unga patienter har fortfarande dålig prognos, särskilt om cancern sprider sig eller är resistent mot kemoterapi. Denna studie avslöjar ett dolt "huvudströmbrytare"-protein kallat MAT2A som hjälper osteosarkomceller att växa, omprogrammera sin energianvändning och bilda aggressiva tumörer — och visar att ett läkemedel riktat mot MAT2A kan bromsa eller krympa dessa tumörer i laboratoriemodeller.
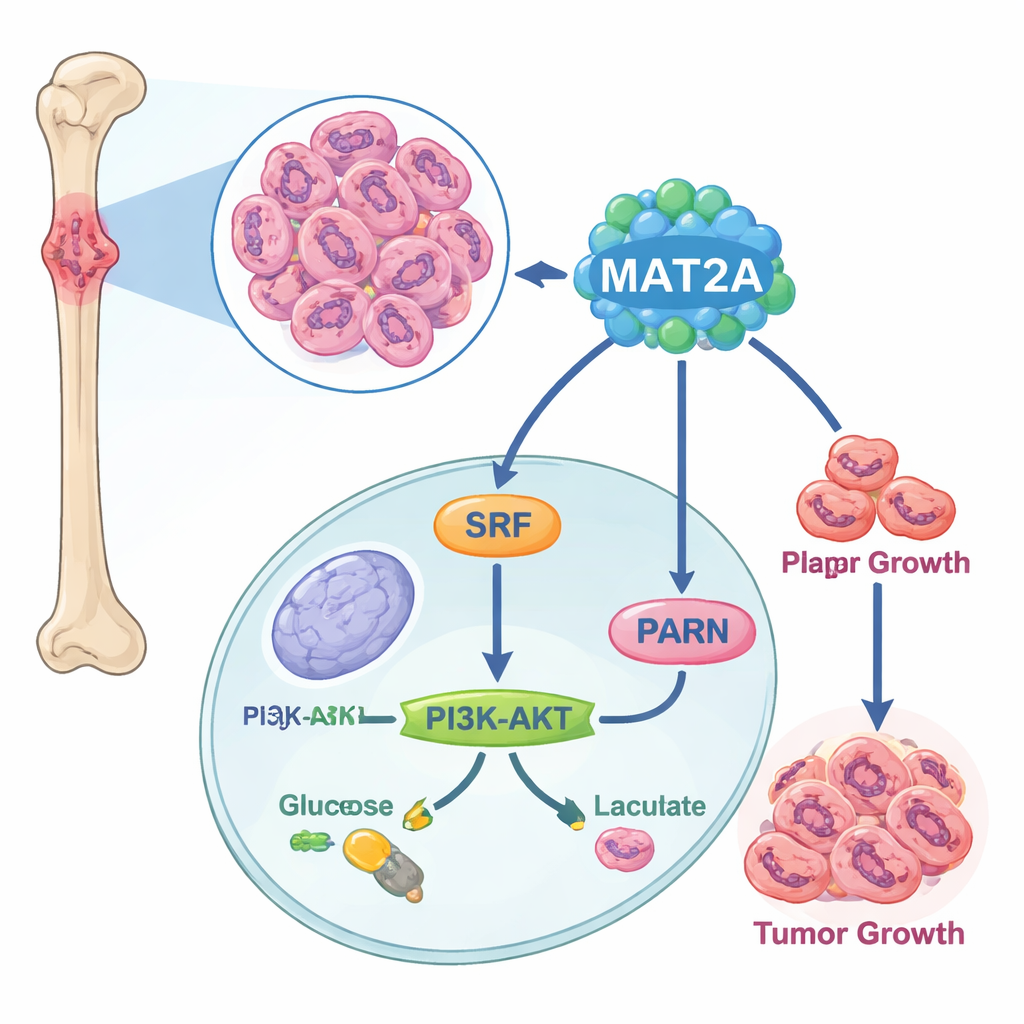
En dold motor inne i tumörceller
Forskarnas arbete började med att jämföra bencancervävnad med normal benvävnad på enskild-cellnivå. De fann att osteosarkomvävnad innehåller fler tumörbyggande celler och färre immunceller, och att en gen i synnerhet—MAT2A—var ovanligt aktiv i cancerceller. Analyser av publika cancerregister och odlade cellinjer bekräftade att MAT2A-nivåerna var mycket högre i osteosarkom än i friska benceller, och att patienter med högre MAT2A tenderade att ha mer avancerad sjukdom och spridning till lymfkörtlar. Detta placerade MAT2A i centrum som en möjlig drivkraft för sjukdomen snarare än en passiv åskådare.
Att sänka MAT2A bromsar cancerutveckling
För att pröva hur viktigt MAT2A verkligen är för tumörers beteende använde teamet genetiska verktyg för att minska MAT2A-nivåerna i osteosarkomcellinjer. När MAT2A tystades blev cancercellerna långsammare i delning och mer benägna att genomgå programmerad celldöd. I möss som fick implantat av dessa modifierade celler växte tumörerna betydligt långsammare och blev mycket mindre, trots att djurens kroppsvikt förblev stabil. Dessa experiment visade att osteosarkomceller är starkt beroende av MAT2A både för överlevnad och för sin förmåga att bilda tumörer.
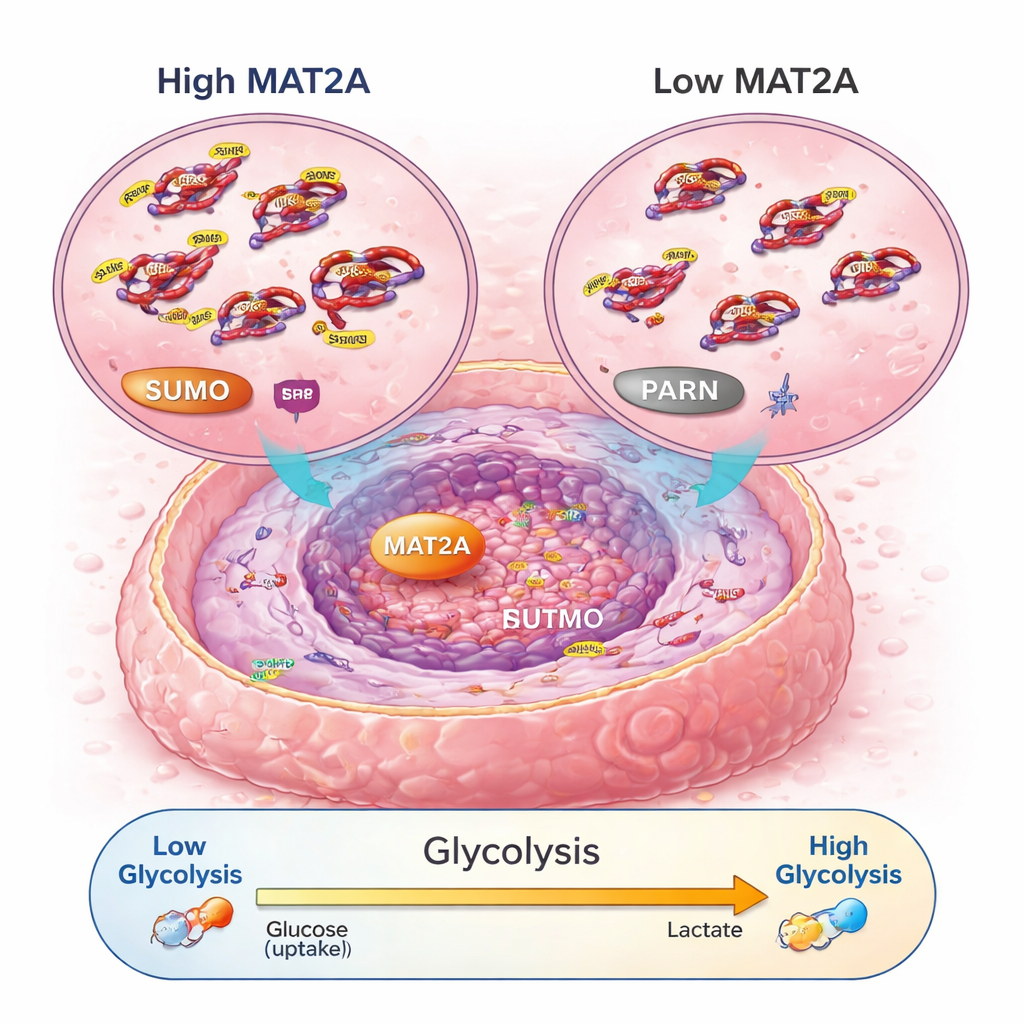
En signalväg som ökar cellernas bränsleanvändning
Vidare upptäckte forskarna att MAT2A gör mer än sin vanliga metaboliska uppgift. Inne i cellkärnan binder det till en transkriptionsfaktor kallad SRF och hjälper till att hålla SRF stabilt och aktivt genom att främja en kemisk märkning känd som SUMO. I sin tur slår SRF på en gen kallad PARN, som sedan aktiverar den välkända PI3K–AKT-vägen och ökar maskineriet för aerob glykolys — ett snabbt men ineffektivt sätt för celler att framställa energi som cancerceller föredrar. När MAT2A minskade producerade cancerceller mindre ATP (deras energivaluta), tog upp mindre glukos, producerade mindre mjölksyra och återgick mot lugnare, syreberoende respiration. Att störa PARN eller AKT kunde upphäva MAT2A:s tillväxt- och glykolyseffekter, vilket bekräftar att denna kedja—MAT2A till SRF till PARN till PI3K–AKT—fungerar som en nyckelkrets för energi och tillväxt i osteosarkom.
En icke-traditionell roll och ett läkemedelsbart mål
Påfallande nog stödde en variant av MAT2A som saknade sin vanliga enzymatiska aktivitet fortfarande SRF-stabilitet och PARN-aktivering, vilket betyder att denna cancerframkallande roll inte är beroende av dess vanliga kemiska reaktion. Istället fungerar MAT2A mer som ett stommeprotein som organiserar andra proteiner. Detta har praktiska konsekvenser: läkemedel behöver inte nödvändigtvis blockera dess katalytiska centrum för att försvaga tumörer. Forskarna testade en småmolekylinhibitor kallad FIDAS-5, designad för att rikta MAT2A, både i cellkulturer och i musmodeller. Behandlingen minskade kärn-SRF, sänkte PARN- och PI3K–AKT-signalering, dämpade glykolys, bromsade celltillväxt och utlöste cancercelldöd. Hos möss krympte eller bromsade FIDAS-5 tumörer utan märkbar viktminskning, vilket tyder på acceptabla biverkningar i detta sammanhang.
Vad detta betyder för patienter och framtida terapier
För icke-specialister är kärnbudskapet att osteosarkomceller är beroende av MAT2A för att hålla sina tillväxtprogram och sina sockerförbränningsmotorer igång på högvarv. Genom att stabilisera nyckelregulatorer och förstärka en kedja av signaler hjälper MAT2A tumörer att växa snabbare och bli mer aggressiva. Att blockera detta protein—antingen med genbaserade metoder eller ett läkemedel som FIDAS-5—skär av det stödet, tvingar cancerceller att sakta ner, använda energi mindre frenetiskt och i slutändan dö. Trots att mycket arbete återstår innan sådana behandlingar når kliniken positionerar denna studie MAT2A som ett lovande nytt mål i kampen mot bencancer och öppnar en möjlig väg till mer precisa och mindre toxiska terapier för unga patienter.
Citering: Ren, Z., Chen, H., Qiao, Q. et al. MAT2A enhances PARN transcription via SRF to accelerate glycolysis and drive malignant progression in osteosarcoma. Commun Biol 9, 241 (2026). https://doi.org/10.1038/s42003-026-09518-w
Nyckelord: osteosarkom, MAT2A, cancermetabolism, PI3K AKT-vägen, målinriktad terapi