Clear Sky Science · sv
Strategiska framsteg för cryo-EM-strukturella studier av små (<100 kDa) GPCR:er
Varför små cellomkopplare är viktiga för medicinen
Mycket av modern medicin fungerar genom att försiktigt påverka små omkopplare i våra cellmembran, kallade G-proteinkopplade receptorer (GPCR:er). Dessa omkopplare känner av hormoner, dofter och läkemedel, och ungefär en tredjedel av alla godkända läkemedel verkar via dem. För att kunna designa säkrare och mer träffsäkra läkemedel behöver forskare detaljerade 3D-bilder av dessa receptorer, särskilt i deras "av"- eller inaktiva former, som många läkemedel riktar sig mot. Den här artikeln förklarar hur forskare lär sig att se några av de minsta GPCR:erna med kryo-elektronmikroskopi (cryo-EM), en kraftfull avbildningsmetod som kan fånga molekyler frysta i ett nära naturligt tillstånd.
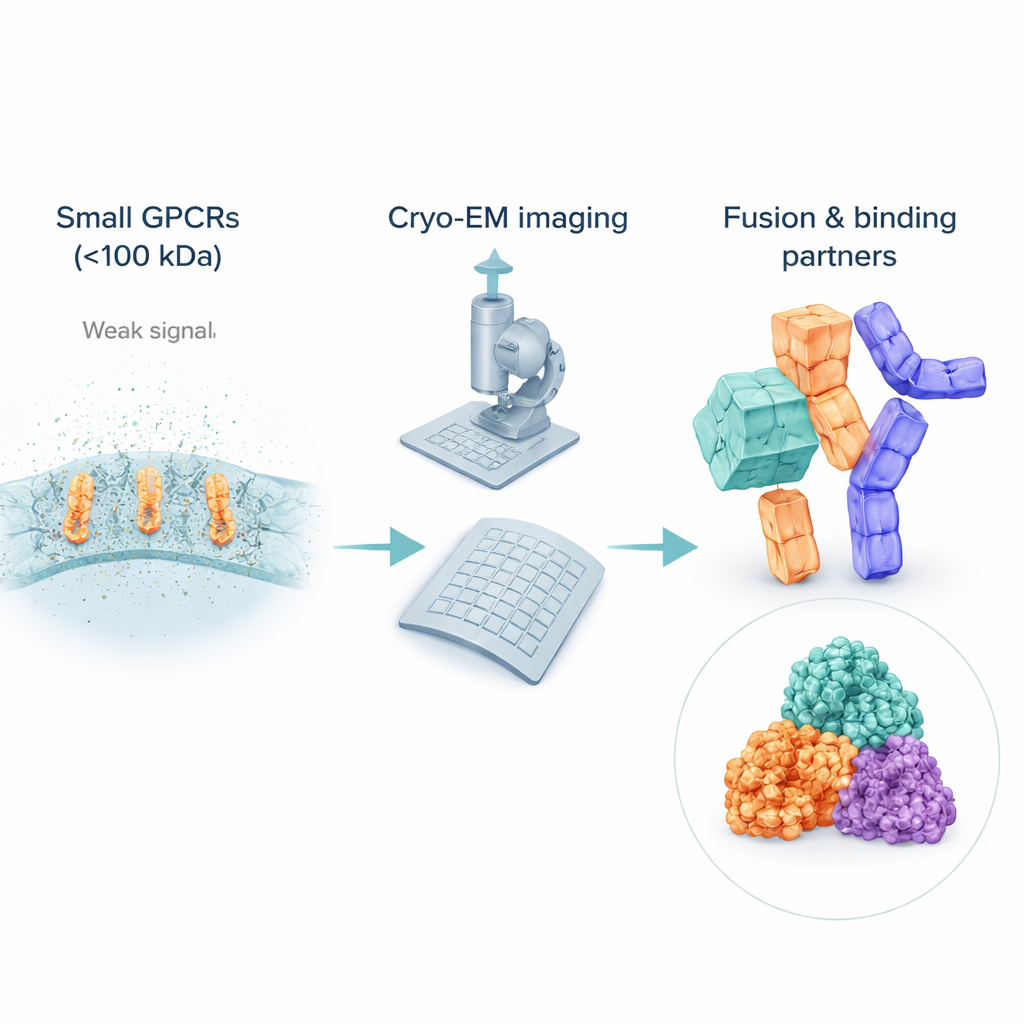
Utmaningen att se mycket små receptorer
Trots att cryo-EM har revolutionerat den strukturella biologin har metoden fortfarande problem med små, flexibla molekyler. Många inaktiva GPCR:er väger långt mindre än 100 kilodalton, vilket gör dem svåra att upptäcka och justera i brusiga bilder. För att hålla dem lösliga kapslarar forskare ofta in dessa receptorer i detergentbubblor eller lipidlika miljöer, vilka för elektronstrålen kan framstå som "större" än själva receptorn och därigenom dränka signalen från det intressanta proteinet. Till skillnad från aktiva receptorer som är bundna till skrymmande partner som G-proteiner saknar inaktiva GPCR:er ofta framträdande yttre kännetecken, så datorer har svårare att medelvärdesbilda många bilder till en skarp 3D-vy. Följaktligen kommer de flesta inaktiva GPCR-strukturer fortfarande från äldre röntgenmetoder, vilket lämnar ett gap i cryo-EM-täckningen just där många läkemedel verkar.
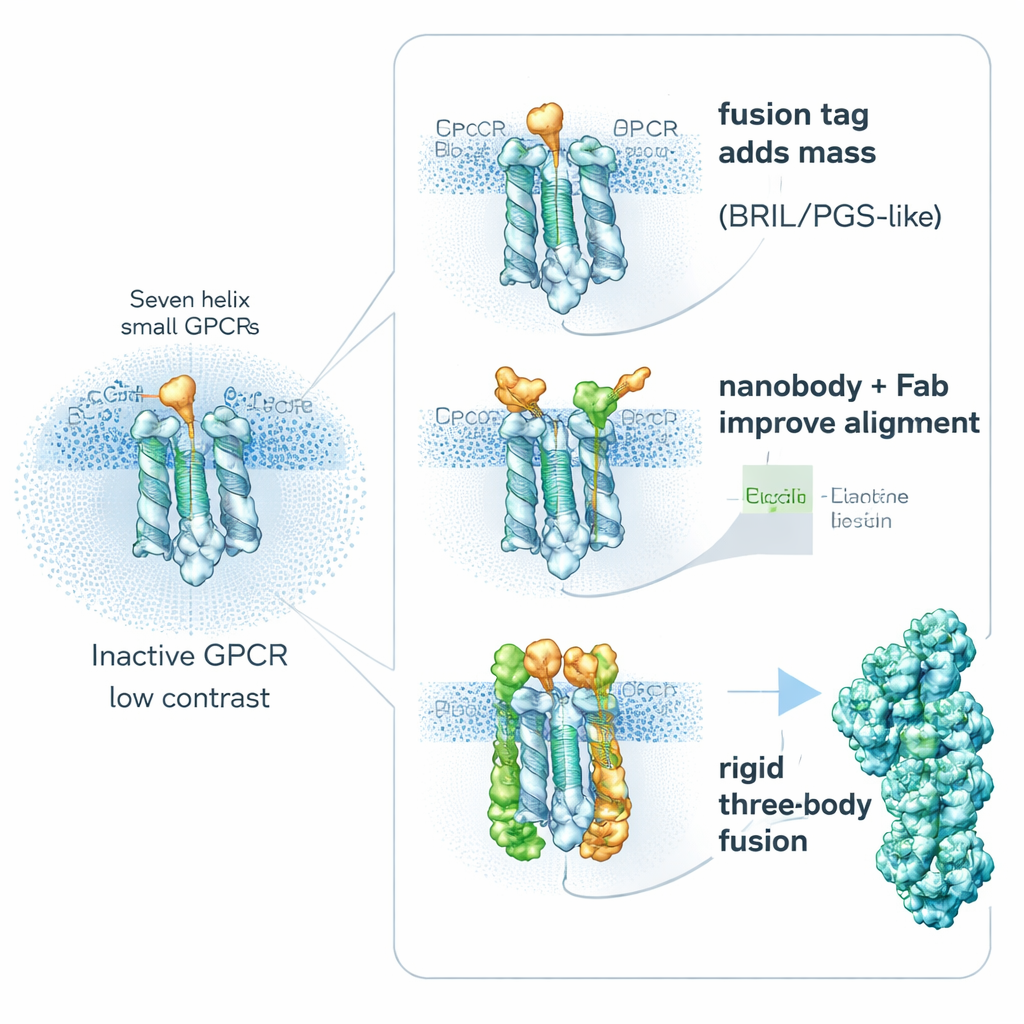
Göra receptorer "tyngre" med inbyggda hjälpare
En viktig strategi är överraskande enkel: gör receptorn medvetet "tyngre". Forskare fuserar genetiskt små, stabila hjälpproteiner på flexibla delar av GPCR:er för att öka deras storlek och stelhet, utan att blockera viktiga läkemedelsbindande områden. Populära hjälpare inkluderar BRIL (en fyr-helix-bunt), PGS (en värmestabil enzymfragment) och ett större klämliknande protein kallat calcineurin. Dessa fusionspartner sätts ofta in i en rörlig inre loop som förbinder två helixar. Genom att styva upp detta område minskar de den suddighet som kommer från molekylär rörelse och ger igenkännbara former som hjälper datorer att justera partiklar. Studier visar att exakt position och orientering av fusionsstycket kan avgöra projektets framgång: i en receptor förbättrade en annorlunda placerad PGS-tag upplösningen från suddiga 6 ångström till betydligt klarare 3,7 ångström.
Låna antikroppar och designade bindare som handtag
En annan väg undviker att bygga in stora fusioner i receptorn och fäster istället högaffinitets "handtag" utanpå. Små antikroppsfragment kallade nanokroppar och närbesläktade bindare kan framställas för att känna igen inaktiva GPCR:er och haka fast vid flexibla inre slingor. Ett framstående exempel är Nanobody-6, som först skapades som en sensor för en opioidreceptor och sedan återanvändes, med måttliga justeringar, för att stabilisera flera andra GPCR:er i deras inaktiva former. Eftersom den binder avcentrerat ger den varje partikel en tydlig orienteringsledtråd, vilket gör medelbildningen mer pålitlig. Forskare förlänger ofta denna idé genom att lägga till ett andra lager—ett vanligt antikroppsfragment som känner igen nanokroppen själv—och skapar därigenom ett skrymmande, mer stelt komplex som framträder tydligt i cryo-EM. Andra ingenjörsbundna bindare, såsom DARPins, kan användas som modulära distanser eller som förbindelser till större proteinkorgar och ytterligare öka signalen från mycket små mål.
Smartare provdesign och AI-förstärkt bildbehandling
Att fusera hjälpare eller lägga till bindare är bara en del av historien. Översikten betonar att bra strukturer börjar med noggrant konstruerade receptorpreparat: trimning av lösa svansregioner, införande av stabiliserande mutationer och användning av moderna strukturprediktionsverktyg för att identifiera delar som sannolikt orsakar problem. På avbildningssidan kompletteras eller ersätts äldre knep som phase plates, vilka ökar kontrasten för svaga partiklar, av artificiell intelligens. Djupinlärningsprogram kan plocka ut små partiklar gömda i brusiga mikrografer, och nya algoritmer kan sortera bilder i olika former när receptorer antar många konformationer. Tillsammans med fiduciala hjälpare driver dessa framsteg cryo-EM mot att pålitligt lösa membranproteiner som tidigare ansågs för små eller för dynamiska för att studera.
Vad detta innebär för framtida läkemedel
Artikeln avslutar med slutsatsen att det inte finns någon enskild "magisk" hjälpare som fungerar för alla receptorer, men en växande verktygslåda av fusionspartner, antikropps‑liknande bindare och AI-drivna metoder öppnar stadigt upp det inaktiva landskapet hos GPCR:er för cryo-EM. För icke-experter är den viktigaste slutsatsen att genom att få små receptorer att framstå som större och mer ordnade för mikroskopet kan forskare slutligen skaffa detaljerade ögonblicksbilder av de exakta former som många läkemedel föredrar att binda. Dessa strukturella ritningar bör påskynda designen av läkemedel som mer precist stänger av dessa cellulära omkopplare—eller finjusterar deras aktivitet—med färre biverkningar.
Citering: Singh, S.K., Agrawal, M., Pattanayak, A. et al. Strategic advances for cryo-EM structural studies of small (<100 kDa) GPCRs. Commun Biol 9, 237 (2026). https://doi.org/10.1038/s42003-026-09516-y
Nyckelord: G-proteinkopplade receptorer, kryo-elektronmikroskopi, läkemedelsforskning, strukturell biologi, nanokropps‑ramverk