Clear Sky Science · sv
Koppla molekylär spänning till cellulära dragkrafter: en multiskalig ansats till fokala adhesionsmekanik
Hur celler känner och drar i sin omgivning
Varje gång en cell rör sig, delar sig eller omformar en vävnad drar den diskret i sin omgivning. Dessa små mekaniska drag är avgörande vid sårläkning, cancerspridning och organutveckling, men de är svåra att se och ännu svårare att mäta. Denna studie presenterar ett nytt sätt att betrakta dessa krafter ur två perspektiv samtidigt: hur hårt en hel cell drar i ett mjukt material, och hur mycket kraft individuella ”molekylära fjädrar” inuti cellens förankringspunkter bär. Genom att koppla ihop dessa vyer hjälper arbetet till att förklara hur celler känner av stelhet och reglerar sitt grepp om omvärlden.
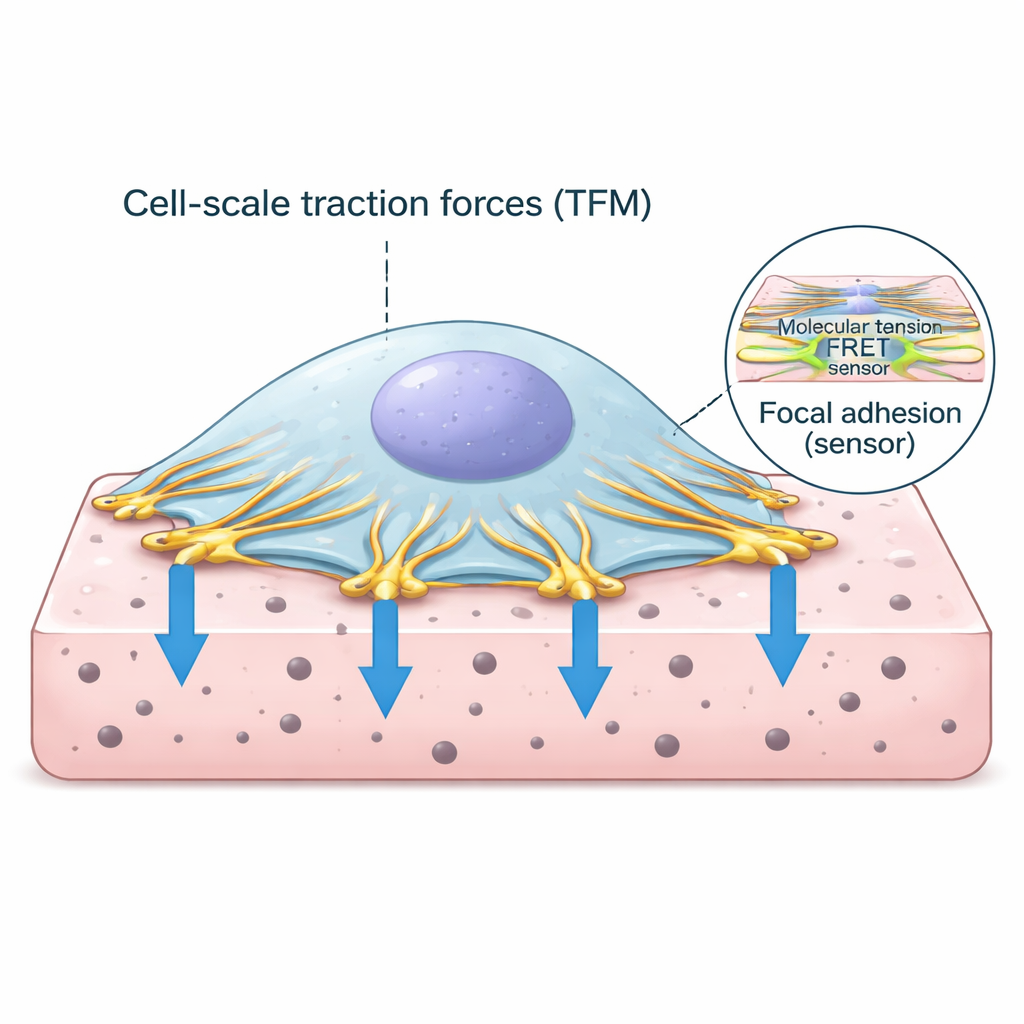
Cellens grepppunkter mot omvärlden
Celler flyter inte enkelt i vävnader; de förankrar sig genom specialiserade kontaktpunkter kallade fokala adhesioner. På dessa platser kopplas cellens interna stomme av aktinfibrer till proteiner som sträcker sig genom cellmembranet och hakar fast i den omgivande matrisen. Ett av nyckelproteinerna i detta ankarkomplex är vinculin, som fungerar som en kraftkänslig länk. När cellens kontraktila maskineri drar i aktin känner vinculin lasten och hjälper till att stärka förbindelsen. Att förstå hur mycket kraft som passerar genom dessa länkar, och hur det relaterar till cellens övergripande dragkraft, är centralt för att avkoda hur vävnader håller sig friska eller blir sjuka.
Två fönster in i cellulära krafter
Forskarlaget kombinerade två kraftfulla tekniker i ett enda arbetsflöde. Först mäter traction force microscopy hur mycket en cell deformera ett mjukt, geléliknande substrat genom att följa rörelsen hos små fluorescerande pärlor i gelen. Utifrån dessa pärlrörelser kan man beräkna fördelningen av tryck- och dragkrafter under cellen. För det andra bär ett specialkonstruerat vinculinprotein en fluorescerande spänningssensor som ändrar sitt ljussignal när den sträcks. Med avancerad livstidsavbildning omvandlade teamet denna ljussignal till en avläsning av molekylär spänning på vinculin. De designade tunna, plana hydrogel som kunde avbildas med hög upplösning och skrev egen mjukvara för att justera, segmentera och analysera båda dataset ner till individuella adhesionsställen.
Hur stelhet förändrar cellens insats
När celler odlades på mjukare respektive styvare geler förändrades deras beteende på ett tydligt sätt. På styvare substrat spred sig cellerna mer och utövade starkare dragkrafter på gelytan. Samtidigt visade den fluorescerande avläsningen från vinculin-sensorn högre molekylär spänning inne i de fokala adhesionerna. Intressant nog förändrades inte adhesionsstrukturerna i grunden—såsom deras antal eller genomsnittliga storlek—så mycket mellan mjuka och styva geler. Istället förändrades hur krafterna organiserades. Stora, radiellt orienterade adhesioner med mer vinculin tenderade att bära högre dragkrafter, vilket tyder på att både geometrin och den molekylära sammansättningen av dessa platser hjälper till att bestämma hur hårt cellen drar.
En komplex relation mellan lokala och molekylära krafter
När man tittade närmare på individuella adhesioner framkom att sambandet mellan lokal traction och vinculin-spänning inte är universellt. I vissa celler visade adhesioner som genererade högre traction också högre vinculin-spänning, vilket antyder att engagerade, lastbärande kontakter delar kraft mer direkt över sina molekylära länkar. I andra celler uppträdde det motsatta mönstret: regioner med stark traction var associerade med lägre vinculin-spänning, medan andra adhesioner bar mer molekylär last utan att producera stora utåtriktade drag. Många celler visade ingen tydlig koppling alls. Dessa olika beteenden speglar sannolikt olika celltillstånd—såsom aktiv utbredning, stabil adhesion eller retraktion—och tyder på att celler kan omfördela krafter i sitt adhesionsnätverk på flera sätt.
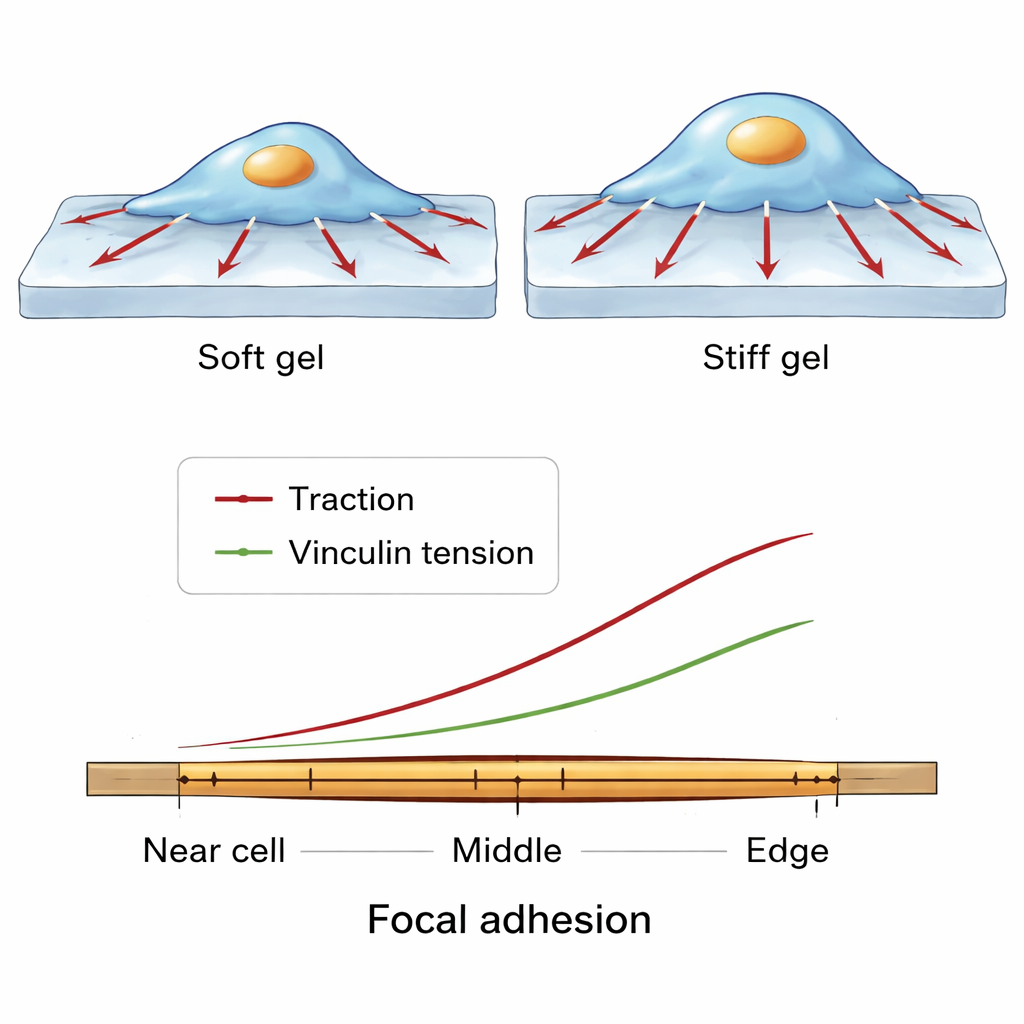
Finskaliga kraftmönster längs en enskild grepppunkt
Teamet zoomade sedan ännu närmare och undersökte hur krafterna varierar längs längden av en enskild fokal adhesion, från sidan närmare cellens centrum till kanten nära cellens periferi. Över många celler och förhållanden uppstod ett konsekvent mönster. Vinculinmolekyler var mest tätt packade mot mitten av adhesonen. Både den traction som utövas på substratet och den molekylära spänningen på vinculin ökade dock mot den yttre, mer perifera änden. Detta tyder på en balansakt: i centrala regioner kan många vinculinmolekyler dela lasten, så att varje enskild känner mindre spänning, medan i den yttre kanten bär färre molekyler relativt mer kraft, vilket stödjer starkt lokalt drag samtidigt som adhesonen hålls samman.
Vad detta betyder för hälsa och sjukdom
Genom att förena hela-cellens tractionkartor med protein-nivåns spänningsmätningar erbjuder denna studie en multiskalig bild av hur celler hanterar sitt mekaniska grepp. Arbetet visar att när omgivningen blir stelare drar celler både hårdare och belastar sina vinculin-länkar mer, men att det detaljerade sambandet mellan utåtagerande krafter och molekylär spänning varierar från adhesion till adhesion och från cell till cell. Samtidigt verkar ett robust rumsligt mönster för kraftfördelning inom enskilda adhesioner vara bevarat. För icke-specialisten är huvudbudskapet att celler finjusterar både var och hur de drar, omfördelar kraft över många små molekylära ”fjädrar” för att anpassa sig till olika mekaniska miljöer—en princip som kan ligga bakom processer så skilda som vävnadsutveckling, fibros och cancerinvasion.
Citering: Aytekin, S., Kimps, L., Coucke, Q. et al. Linking molecular tension and cellular tractions: a multiscale approach to focal adhesion mechanics. Commun Biol 9, 236 (2026). https://doi.org/10.1038/s42003-026-09514-0
Nyckelord: cellmekanik, fokala adhesioner, vinculin, traction force microscopy, mekanotransduktion