Clear Sky Science · sv
Tidsmässig dynamik för kollateral RNA-klyvning av LbuCas13a i humana celler
Att förvandla ett bakteriellt försvar till en precisionstödare som dödar celler
Forskare har funnit ett sätt att omskola ett bakteriellt immunsystemprotein till en högst selektiv "självförstörings"-omkopplare för humana celler. Genom att utnyttja ett CRISPR-enzym kallat LbuCas13a kan de känna igen ett valt RNA-meddelande inne i en cell och därefter sönderdela nästan allt annat RNA i den cellen. För lekmän är detta intressant eftersom RNA-meddelanden styr vilka proteiner en cell tillverkar; att kunna radera dem på kommandot öppnar möjligheter för nya cancerbehandlingar, antiviral strategi och kraftfulla forskningsverktyg.
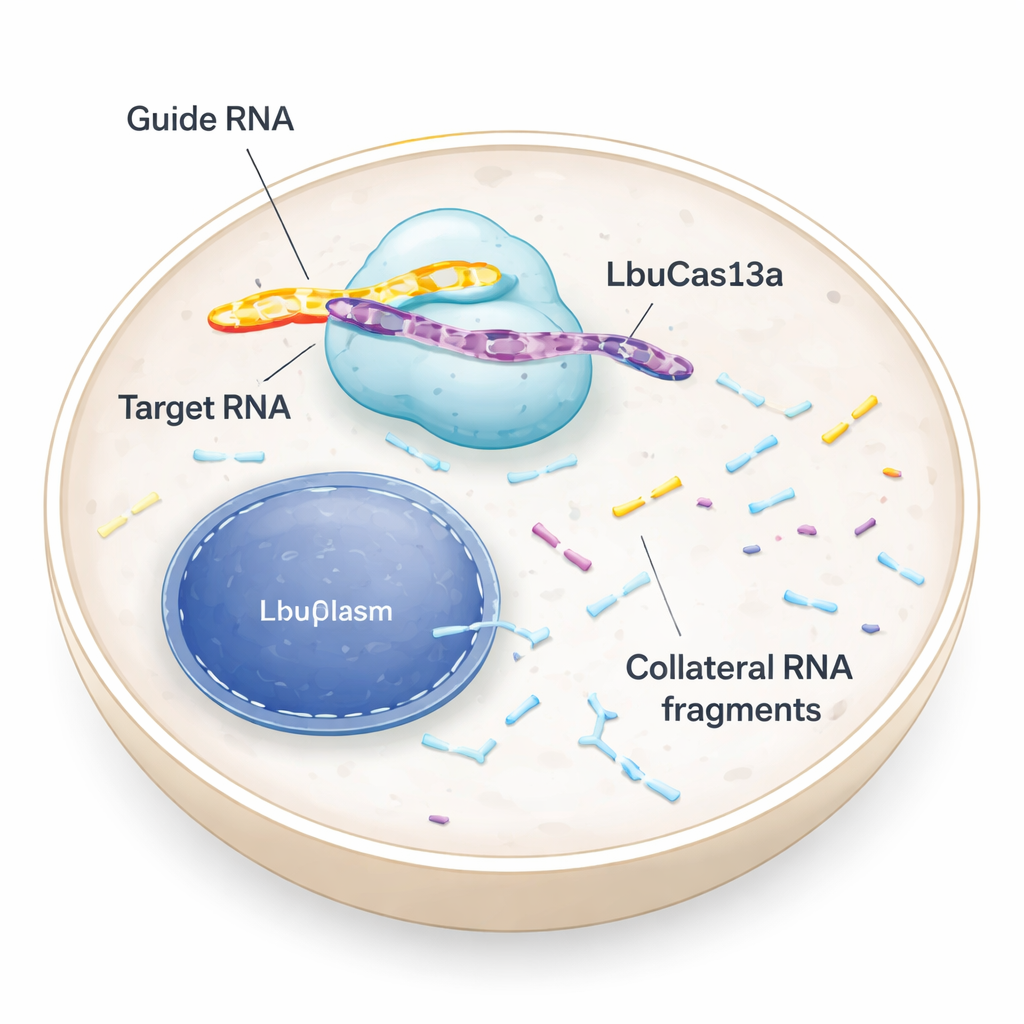
En molekylär sax som riktar sig mot RNA, inte DNA
De flesta har hört talas om CRISPR-verktyg som klipper DNA och skriver om den genetiska koden. LbuCas13a är annorlunda: det känner igen och klyver RNA, de temporära meddelandena som bär instruktioner från DNA till cellens proteinmaskineri. I bakterier är Cas13-enzymer en del av ett antiviralt försvar. När de upptäcker ett viralt RNA klyver de inte bara den inkräktaren utan börjar också klippa många andra RNA i närheten. Denna så kallade "kollaterala" aktivitet kan trycka infekterade celler in i vila eller död, vilket hjälper till att skydda den bakteriella populationen. Tidigare tester i djur- och humana celler antydde att Cas13:s kollaterala klippning var svag eller frånvarande, så enzymet användes främst som en precis RNA-avstängare. Den nya studien omprövar detta antagande och visar att, under rätt förhållanden, kan kollateral aktivitet i humana celler vara både stark och användbar.
Att släppa lös kollateral klippning i humana celler
Forskargruppen jämförde flera Cas13-varianter och fann att LbuCas13a var särskilt potent. De levererade renat LbuCas13a-protein förladdat med ett kort guide-RNA direkt in i humana celler, en form av molekylär "proteininjicering" kallad ribonukleoprotein (RNP)-leverans. När guiden matchade ett mål-RNA — såsom en fluorescerande markörgen eller rikliga naturliga budbärare som GAPDH och 18S ribosomalt RNA — skar enzymet först det målet och började sedan tugga i många andra RNA. Inom cirka 50 minuter förändrades cellens totala RNA-profil dramatiskt, med karakteristiska klyvningsfragment som framträdde. Denna kollaterala effekt observerades med olika leveransmetoder och i en rad celltyper, vilket visar att den inte var en tillfällighet i en enda cellinje eller för ett enda artificiellt mål.
Från RNA-sönderdelning till celldöd och selektion
Vad händer med en cell vars RNA-meddelanden plötsligt försvinner? Med hjälp av live-cell-avbildning såg forskarna att celler som uttryckte mål-RNA gradvis gick in i apoptos, en ordnad form av programmerad celldöd som kännetecknas av typiska "tidiga varnings"-signaler innan cellen bryts ned. Viktigt är att närliggande celler som inte uttryckte mål-RNA förblev i stort sett opåverkade, vilket visar att självförstörelsen är specifik. Gruppen utnyttjade sedan denna egenskap som ett selektionsverktyg. När de blandade mål-bärande celler med normala celler och aktiverade LbuCas13a utplånades de mål-bärande cellerna selektivt över flera dagar. Att upprepa behandlingen flera gånger sänkte deras andel ännu mer. De visade att detta kunde berika för framgångsrikt genredigerade celler och också justeras för att angripa cancerceller som överproducerar en onkogen, här CDK4, samtidigt som närbesläktade celler som producerar mycket mindre av det RNA:t skonas.
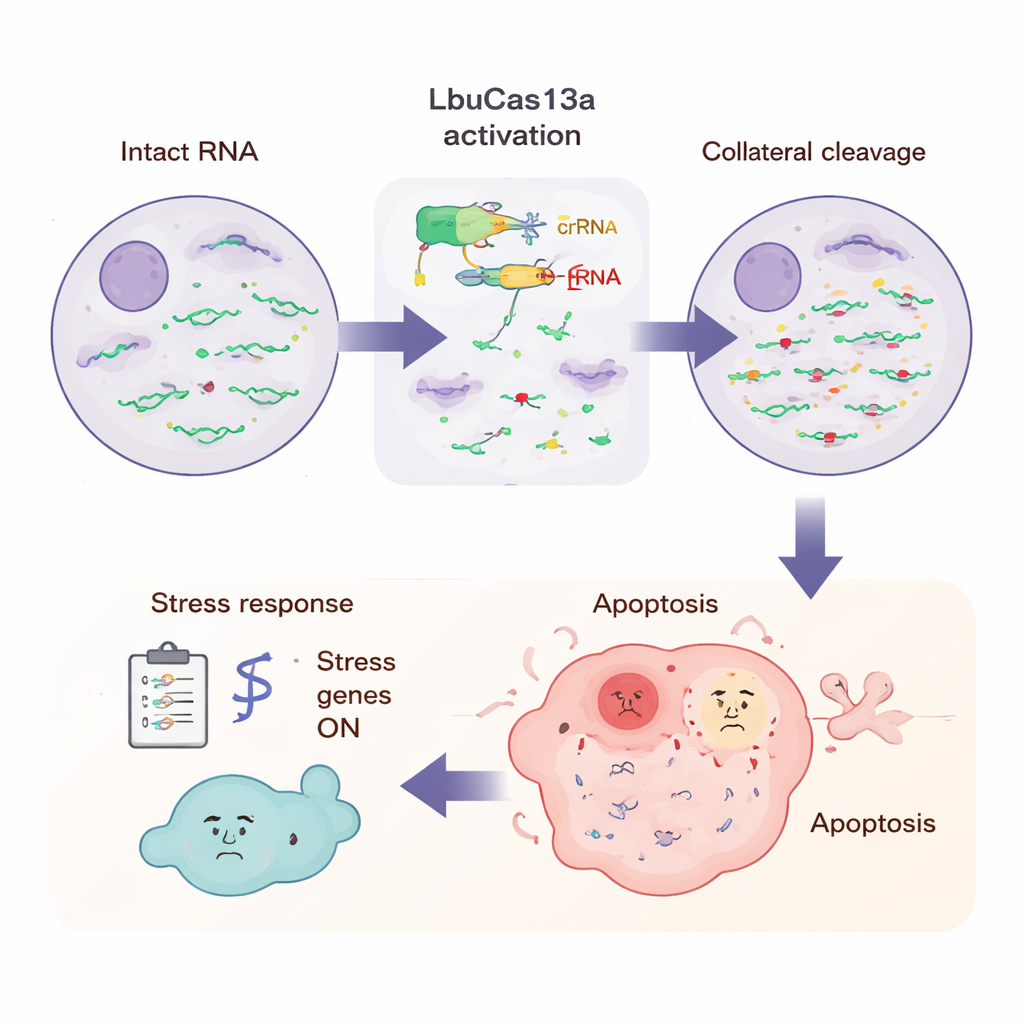
Vad cellen upplever under attacken
För att få en större bild mätte forskarna alla RNA i cellen vid flera tidpunkter efter LbuCas13a-aktivering. Genom att spika in kända RNA-standarder kunde de se att de flesta protein-kodande RNA i cytoplasman minskade med mer än hälften inom några timmar, medan vissa RNA — såsom mitokondriella budbärare och vissa nukleära icke-kodande RNA — i stort sett var förskonade. Långläst sekvensering avslöjade att klyvning skedde på upprepade, specifika nukleotidpositioner, ofta i flexibla loopregioner av RNA rika på basen uracil, vilket motsvarar mönster sedda i provrörsexperiment. Vid senare tidpunkter slog många stress- och medfödda immungener på, inklusive de kopplade till inflammatoriska signaler och antivirala försvar. Detta mönster tyder på att cellen känner av den plötsliga floden av brutna RNA-ändar ungefär som den skulle upptäcka en virusinfektion, och utlöser ett larmprogram som kulminerar i apoptos.
Varför detta är viktigt och vart det kan leda
Enkelt uttryckt visar studien att LbuCas13a kan göras till en RNA-styrd "dödsknapp" för celler: om en cell tillverkar för mycket av ett visst RNA, leder aktivering av LbuCas13a mot det RNA:t till nästan global RNA-förlust, ett immunliknande larm och därefter kontrollerad celldöd. Eftersom processen är starkt beroende av hur rikligt målet-RNA är, skulle den kunna användas för att eliminera celler som överuttrycker skadliga gener — såsom vissa cancerceller — eller för att rensa bort oönskade celler i blandade kulturer vid forskning eller vid tillverkning av cellterapier. Samtidigt är arbetet en varning: CRISPR-verktyg som riktar sig mot RNA kan ha kraftfulla bieffekter som måste hanteras noggrant. Att förstå när och hur kollateral RNA-klyvning uppstår är väsentligt för att säkert använda Cas13-teknologier i medicin och bioteknik.
Citering: Bot, J.F., Zhao, Z., Li, M. et al. Temporal dynamics of collateral RNA cleavage by LbuCas13a in human cells. Commun Biol 9, 233 (2026). https://doi.org/10.1038/s42003-026-09511-3
Nyckelord: CRISPR-Cas13, RNA-klyvning, celldöd, riktad cancerbehandling, verktyg för genredigering