Clear Sky Science · sv
Modifiering av mänskliga klass B1 GPCR av plasmamembranlipider
Fetter som finjusterar cellens mottagare
Våra celler förlitar sig på små proteiniantenner, kallade receptorer, för att känna av hormoner och signalsubstanser i hjärnan. Många storsäljande läkemedel verkar genom att rikta sig mot dessa receptorer. Denna studie visar att vanliga fetter i cellens yttre skikt gör mycket mer än att bara bilda en passiv bakgrund: de binder direkt och formar en hel familj av viktiga receptorer och styr subtilt hur signaler slås på eller av. Att förstå detta dolda kontrollskikt kan hjälpa till att designa smartare läkemedel med färre biverkningar.
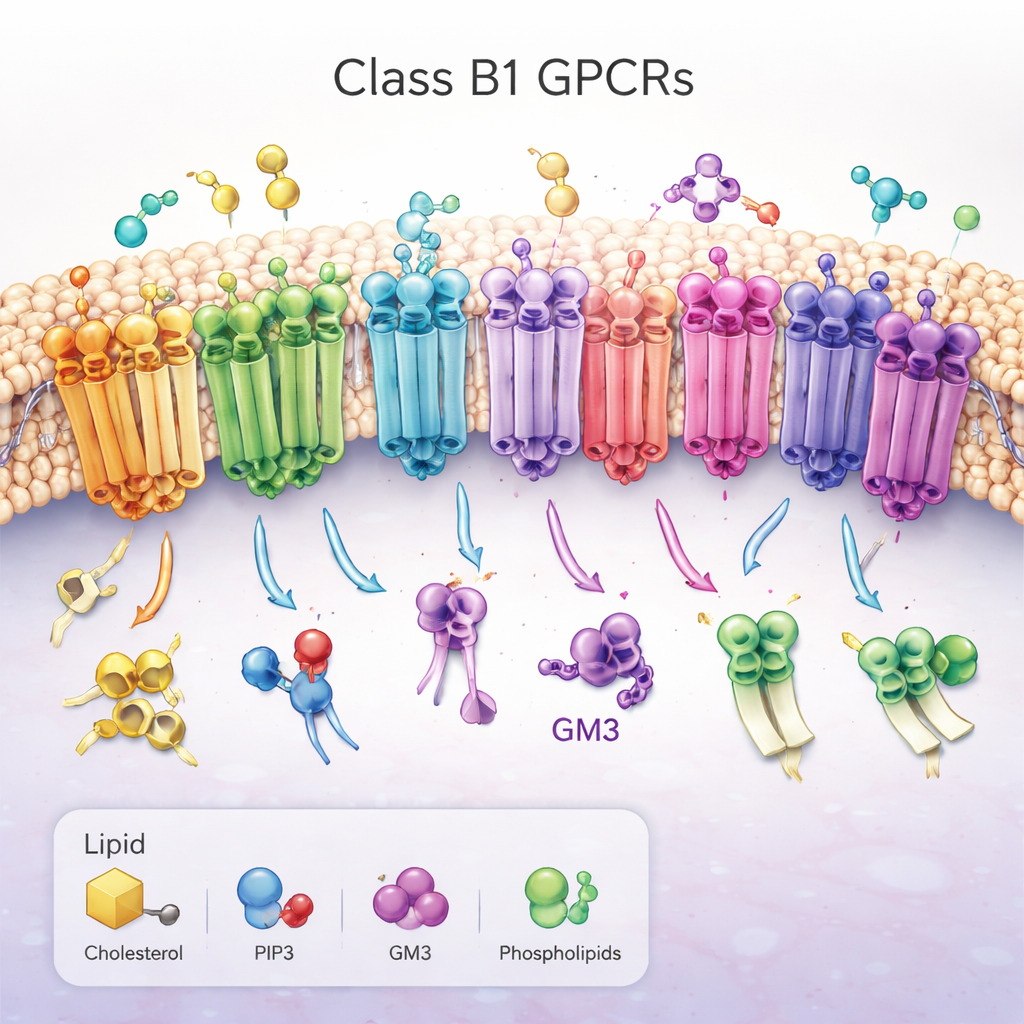
En familj av viktiga molekylantenner
Arbetet fokuserar på klass B1 G-proteinkopplade receptorer (GPCR), en grupp om 15 närbesläktade receptorer som hjälper till att kontrollera blodsocker, ämnesomsättning, tillväxt och stressreaktioner. De sitter tvärs över cellens yttre membran, med ett stort ”huvud” utanför cellen som fångar hormonliknande molekyler och en bunt av sju helixar som tränger genom det feta membranet. När de aktiveras ändrar dessa receptorer form på insidan av cellen, vilket öppnar en fåra som rekryterar partnerproteiner och utlöser signalvägar. På grund av deras centrala roll i sjukdomar som diabetes och fetma är klass B1 GPCR viktiga läkemedelsmål, men hur de omgivande membranlipiderna reglerar dem har till större delen förblivit mystiskt.
Simulera receptorer i deras naturliga kvarter
I stället för att studera receptorer i artificiella detergentbubblor placerade forskarna alla 15 mänskliga klass B1 GPCR i datorbyggda membran som efterliknar den komplexa blandningen av fetter i verkliga celler. Med en teknik kallad coarse-grained molekyldynamik körde de flera långa simuleringar av varje receptor i både aktivt och inaktivt tillstånd, sammanlagt ungefär en millisekund simulerad tid. De följde hur tre ”regulatoriska” lipider—kolesterol, signalsubstansen PIP2 och det sockerprydda fettet GM3—närmade sig, bundet till och lämnade olika regioner av varje receptor. För att andra ska kunna reproducera och bygga vidare på denna stora datamängd fångade de varje steg av uppsättningen och analysen med ett öppet arbetsflödesverktyg kallat aiida-gromacs, och de jämförde sina fysikbaserade resultat med förutsägelser från en ny AI-modell (Chai‑1) som gissar hur proteiner binder små molekyler.
Gömda fickor och ett bevarat lipidgrepp
Simuleringarna avslöjade återkommande bindningsmönster över hela receptorfamiljen. Kolesterol, mest känt från kostdiskussioner, sågs fastna inte bara i en tidigare känd plats på en av helixarna utan också i ”djupa membranfickor” mellan helixar, med sin polära huvudgrupp ovanligt djupt inbäddad i membranet. En receptor, sekretinreceptorn, visade särskilt långlivade kolesterolbindningar i distinkta fickor i sina aktiva respektive inaktiva former, vilket antyder att kolesterol kan starkt påverka hur den signalerar. PIP2 visade ett slående bevarat beteende: den klustrade runt receptorernas inre yta vid korsningen av två helixar och ett kort svanssegment (TM6, TM7 och H8), särskilt när receptorerna var i det aktiva tillståndet. På denna plats grep nätverk av positivt laddade aminosyror tag i PIP2:s negativt laddade huvudgrupp, vilket föreslår ett sätt som denna lipid skulle kunna stabilisera den aktiva formen eller hjälpa till att rekrytera signalpartner på insidan av cellen.
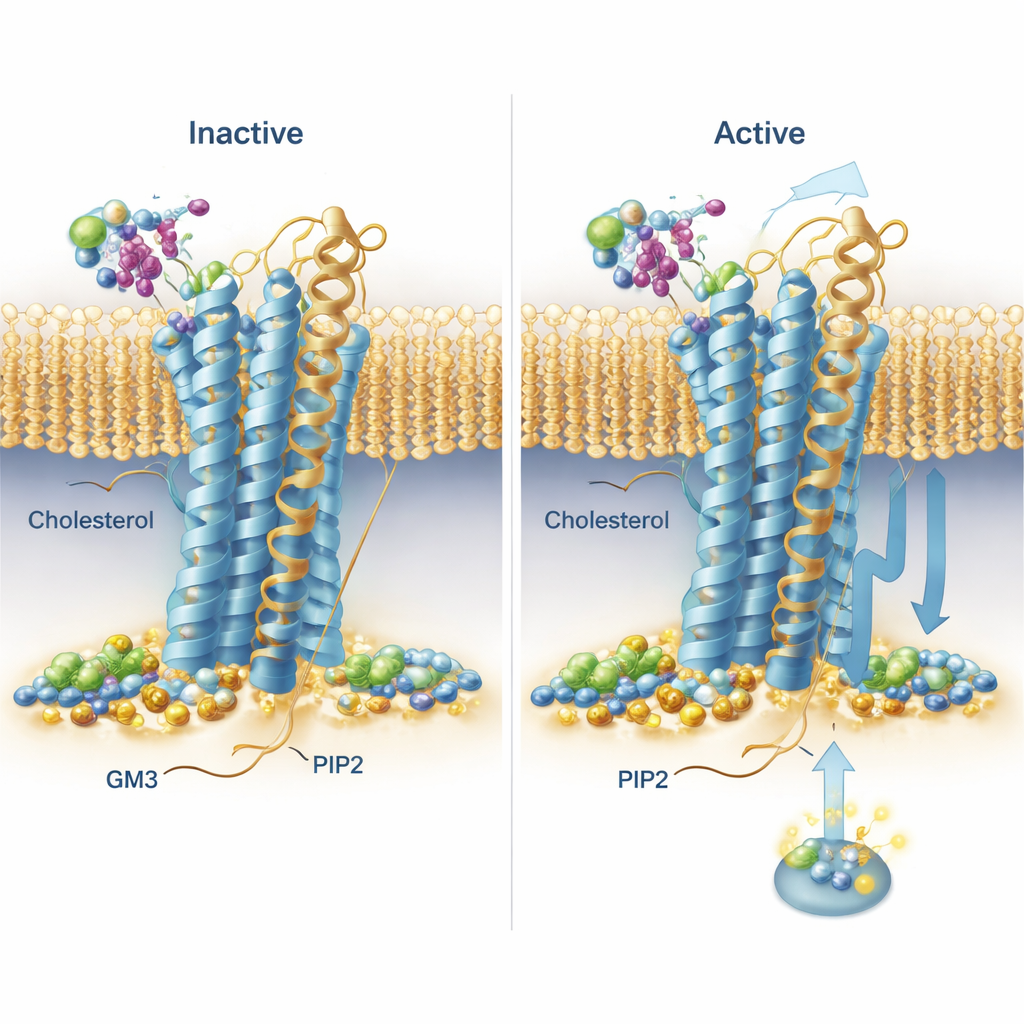
En sockerprydd lipid som knuffar på receptorernas rörelse
GM3, en komplex lipid med ett sockerhuvud, interagerade mest med receptorernas stora yttre huvuden. Teamet noterade att vissa receptorers yttre domäner svängde och böjde sig mycket i förhållande till membranet, medan andra var mer begränsade. För två läkemedelsrelevanta receptorer—GLP‑1R och GIPR—granskade de GM3:s roll i detalj. I simuleringar där GM3 var närvarande lade sig lipiden antingen vid basen av den yttre domänen och ligandbindningsfickan (GLP‑1R) eller fastnade vid den yttersta spetsen av den yttre domänen (GIPR), i båda fallen vilket påverkade hur fritt dessa domäner kunde röra sig. För att testa dessa förutsägelser i levande celler använde forskarna en ljusbasserad teknik (TR‑FRET) som rapporterar hur nära ett märkt receptorhuvud är membranet. När de sänkte GM3-nivåerna med en småmolekylär hämmare såg de mätbara förändringar i hur receptorhuvudena flyttade sig vid stimulering, i stort överensstämmande med idén att GM3 finjusterar receptorernas flexibilitet på ett receptor- och tillståndsspecifikt sätt.
Varför dessa lipid–receptorpartnerskap är viktiga
Tillsammans målar studien upp en bild av klass B1 GPCR som inte bara hormonbrytare utan som delar i en tätt koreograferad dans med omgivande lipider. Kolesterol kan ockupera dolda fickor och subtilt gynna vissa signalutfall, PIP2 bildar ett bevarat inre ”handtag” som kan låsa receptorer i deras aktiva former och vägleda partnerproteiner, och GM3 finjusterar hur receptorernas yttre regioner rör sig och möter sina ligander. För icke-specialister är huvudsaken att membranet är ett aktivt reglerande lager: små skillnader i lipidkomposition kan ändra hur samma receptor beter sig i olika vävnader eller sjukdomstillstånd. Genom att kartlägga dessa interaktioner i detalj och dela den underliggande simuleringsdatan lägger detta arbete en grund för att utforma framtida läkemedel som utnyttjar eller undviker specifika lipidsammanlagringar, vilket potentiellt kan göra behandlingar mer selektiva och effektiva.
Citering: Chao, K.W., Wong, L., Oqua, A.I. et al. Human class B1 GPCR modulation by plasma membrane lipids. Commun Biol 9, 317 (2026). https://doi.org/10.1038/s42003-025-09445-2
Nyckelord: G-proteinkopplade receptorer, membranlipider, kolesterol, PIP2, GM3