Clear Sky Science · sv
Strukturella insikter i metallklustertrafik i nitrogenasets monteringsstomme NifEN
Hur naturen bygger ett kraftfullt kemiskt verktyg
Kväve finns överallt i luften omkring oss, men de flesta levande organismer kan inte använda det i den formen. Ett speciellt enzym kallat nitrogenas löser detta genom att omvandla atmosfäriskt kväve till ammoniak, en nyckelingrediens för liv och för gödningsmedel. I centrum av nitrogenas sitter ett tätt metall"kluster" som utför den tuffa kemin, men hur celler bygger denna intrikata enhet har länge varit oklart. Denna artikel skådar in i byggprocessen och visar hur ett proteinstomme kallat NifEN fungerar som en flexibel lastkaj och transportsystem för klustrets metalllast.
En molekylär fabrik bakom gödningsmedel och bränslen
Nitrogenas är naturens motsvarighet till industriella processer som tillverkar ammoniak och flytande bränslen. Istället för jättelika reaktorer använder mikrober en kompakt proteinkomplex drivet av cellulär energi. Dess funktion beror på ett unikt komplext metallcentrum, uppbyggt av järn, svavel, molybden, kol och en organisk sidogrupp. Att montera denna kärna är för känsligt för att överlåtas åt slumpen, så cellerna använder en serie hjälpproteiner. Ett av de viktigaste är NifEN, som tar emot en nästan färdig heljärn‑prekursor (kallad L‑klustret), hjälper till att omvandla den till den mogna formen (M‑klustret) och sedan överlämnar den till det fungerande nitrogenasenzymet. Att förstå hur NifEN hanterar denna trafik kan ge insikter för att konstruera mikrober för renare gödningsmedelsproduktion eller nya kol‑baserade bränslen.
Att se en rörlig maskin med frusna ögonblicksbild
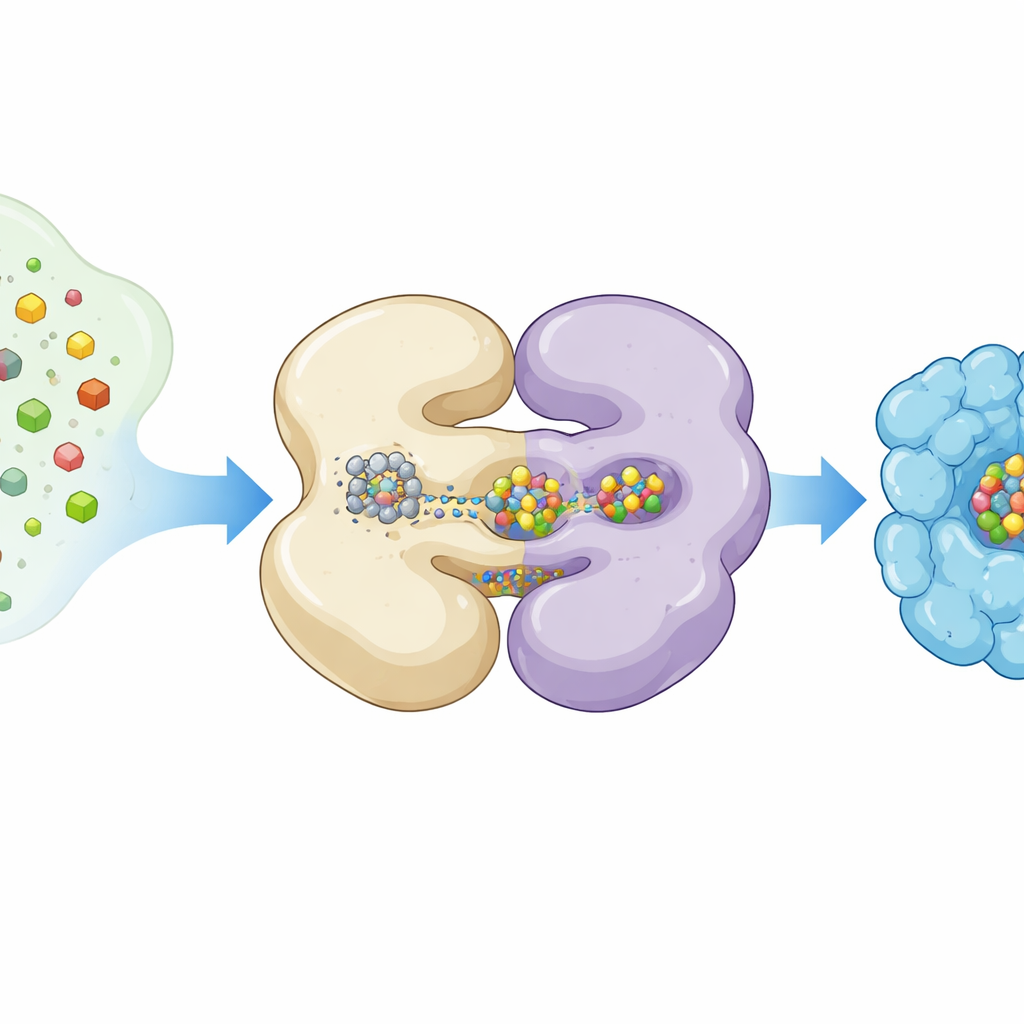
Författarna använde kryogen elektronmikroskopi, en teknik som avbildar proteiner vid mycket låga temperaturer, för att fånga NifEN i olika arbetspositioner. De uttryckte NifEN i laboratoriebakterier på ett sätt som gjorde att några proteinkopior bar på ett L‑kluster medan andra var tomma. Genom att sortera miljontals single‑particle‑bilder rekonstruerade de två huvudformer: en "apo"‑form utan det rörliga klustret och en "holo"‑form med klustret bundet på en intern plats. Båda formerna delar en kärna bestående av fyra subenheter ordnade som två par, men när L‑klustret är närvarande blir ena halvan av NifEN märkbart mer ordnad och flera helixar svänger inåt och spänner runt metalllasten.
En dold tunnel för metalllast
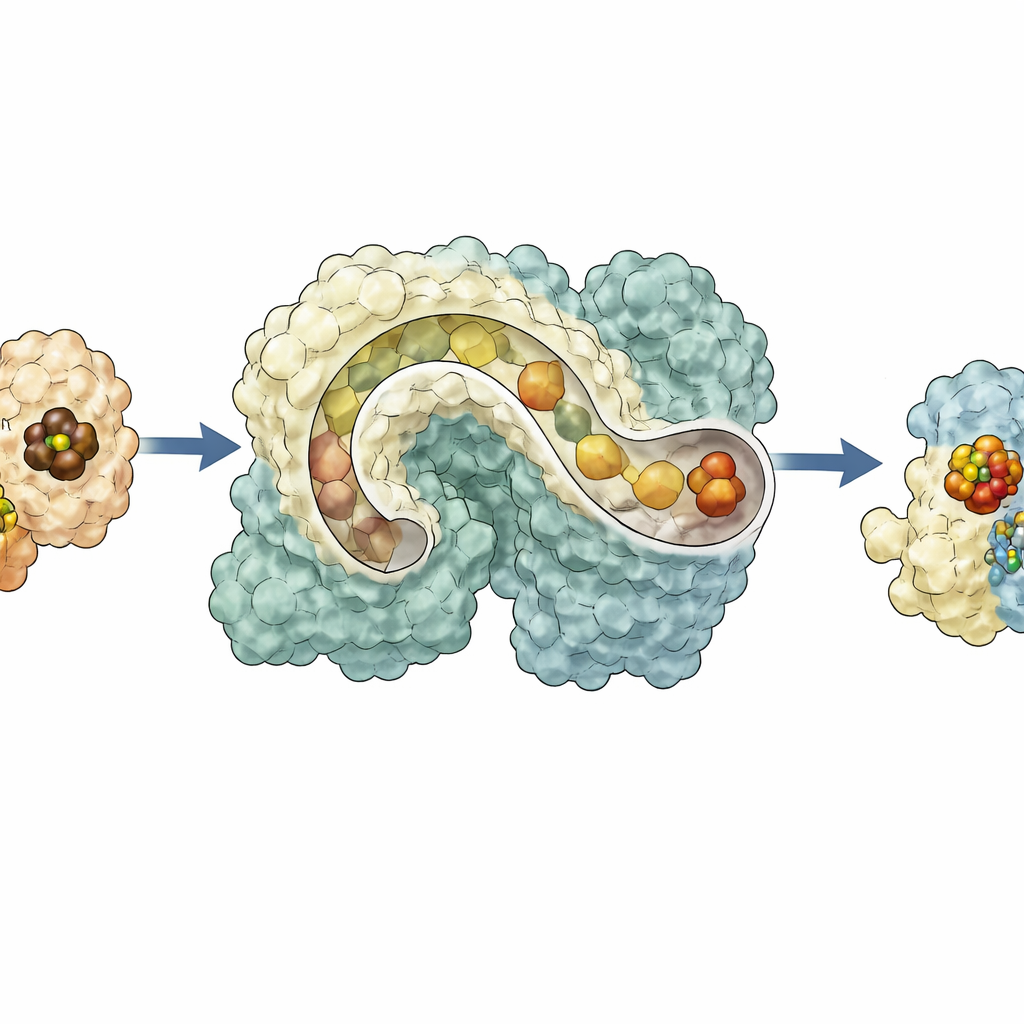
Jämförelsen mellan den tomma och den lastade strukturen avslöjade en slående egenskap: en lång tunnel som löper genom NifEN‑dimeren. I det tomma tillståndet är passagen bred och öppen; efter att klustret bundit smalnar den av när proteinet greppar sin passagerare. Tidigare kristallstrukturer hade visat en alternativ "utomhus" position för L‑klustret nära proteinytan. Genom att sätta samman alla vyer drog forskarna slutsatsen att klustret kan uppehålla sig på minst två stationer på NifEN — en begravd inuti och en exponerad — och förflytta sig mellan dem längs en krökt bana som öppnas och stängs av förskjutningar i en flexibel domän. Denna rörelse verkar vara mer avslappnad än i det slutgiltiga nitrogenasenzymet, vars aktiva kluster hålls stelt på plats, vilket föreslår att NifEN är byggt för överlämning snarare än långvarig katalys.
Dockningspartner och en kontinuerlig rutt
För att förstå hur NifEN kopplar till sina upstream‑ och downstream‑partner kombinerade teamet sina experimentella strukturer med AlphaFold 3‑datormodeller och elektronmikroskopi med lägre upplösning av proteinkomplex. Modellerna antyder att enzymet NifB, som bygger L‑klustret från mindre järn–svavel‑enheter, dockar i en fåra på ena ytan av NifEN. Där kan en kontinuerlig tunnel spåras från NifB:s egna metalcenter direkt in i NifEN‑tunneln och vidare till den interna L‑klusterstationen. På motsatt sida av NifEN rymmer en annan dockningsplats NifH, proteinet som inför molybden och en organisk sidogrupp för att slutföra kofaktorn. I denna konfiguration sitter L‑klustret vid ytan, idealiskt positionerat för modifiering. Mutationer av nyckelaminosyror som kantar den föreslagna rutten stör klusterinlastning, förflyttning eller mognad, vilket ger experimentellt stöd för denna transportbandsmodell.
Varför en flexibel stomme är viktig
Tillsammans målar resultaten upp NifEN som ett dynamiskt nav som tar emot en metallkärna från NifB på ena sidan, flyttar den till en inre upplagringsplats och sedan presenterar den på motsatt yta för färdigställande av NifH innan det mogna klustret styrs tillbaka inuti för leverans till nitrogenas. Detta konformationsstyrda trafikschema förklarar hur flera känsliga steg kan koordineras inom en enda proteinram och antyder hur uråldriga enzymer kan ha utvecklats från mer flexibla stommar till dagens högspecialiserade katalysatorer. För icke‑specialister visar arbetet att även på nanoskaliga nivåer förlitar sig naturen på monteringslinjer, tunnlar och rörliga delar för att bygga de molekylära verktyg som understöder globala cykler av kväve, livsmedelsproduktion och potentiellt framtida gröna teknologier.
Citering: Neumann, B., Brandon, K.A., Quechol, R. et al. Structural insights into metallocluster trafficking in the nitrogenase assembly scaffold NifEN. Nat Catal 9, 281–294 (2026). https://doi.org/10.1038/s41929-026-01489-9
Nyckelord: nitrogenas, montering av metallkluster, NifEN-stomme, kryoelektronmikroskopi, biologisk kvävefixering